
| A、Ca(OH)2═Ca2++2(OH)- |
| B、FeCl2═Fe2++3Cl- |
| C、H2SO4═H++SO42- |
| D、Al2(SO4)3═2Al3++3SO42- |


科目:高中化学 来源: 题型:
| A、在水溶液中和熔化状态下能导电的化合物 |
| B、在水溶液中或熔化状态下能导电的物质 |
| C、在水溶液中或熔化状态下能导电的化合物 |
| D、在水溶液中或熔化状态下导电的离子由原物质本身电离出来的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
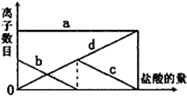 向一定的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生变化.如图所示,四条曲线与溶液中的离子的对应关系,完全正确的是( )
向一定的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生变化.如图所示,四条曲线与溶液中的离子的对应关系,完全正确的是( )| A、a:Cl-; b:K+; c:CO32-; d:HCO3- |
| B、a:K+; b:CO32-; c:Cl-; d:HCO3- |
| C、a:K+; b:CO32-; c:HCO3-; d:Cl- |
| D、a:K+; b:HCO3-;c:Cl-; d:CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.04 |
| B、0.04mol/L |
| C、0.04mol/(L?S) |
| D、0.8mol/(L?S) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸氢钙溶液中加入足量的苛性钠溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O | ||||
B、电解饱和食盐水:2Cl-+2H2O
| ||||
| C、氯气通入冷的氢氧化钠溶液中:2Cl2+2OH-=3Cl-+ClO-+H2O | ||||
| D、FeBr2溶液中通入足量的Cl2:2Fe2++Cl2=2Fe3++2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸氢钠溶液与氢氧化钠溶液:H++OH-=H2O |
| B、新制氯水跟溴化钾溶液反应:Cl2+2Br-=2Cl-+Br2 |
| C、钠与水:2Na+2H2O=2Na++2OH-+H2↑ |
| D、碳酸钙跟稀盐酸反应:CO32-+2H+=H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
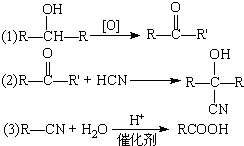
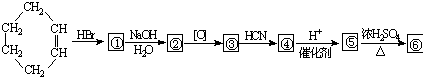
查看答案和解析>>
科目:高中化学 来源: 题型:
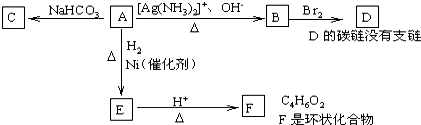
查看答案和解析>>
科目:高中化学 来源: 题型:
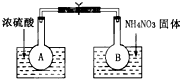
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com