
【题目】通常监测SO2含量是否达到排放标准的反应原理是SO2+H2O2+BaCl2=BaSO4↓+2HCl。设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.0.1molBaCl2晶体中所含离子总数为0.2NA
B.25℃时,pH=1的HC1溶液中含有H+的数目为0.1NA
C.17gH2O2中含有非极性键数目为0.5NA
D.生成2.33gBaSO4沉淀时,转移电子数目为0.01NA
科目:高中化学 来源: 题型:
【题目】硫化氢分解制取氢气和硫磺的反应原理为2H2S(g)![]() S2(g)+2H2(g),在2.0 L恒温恒容密闭容器中充入2.0 mol H2S,反应过程中的部分数据如下表所示:
S2(g)+2H2(g),在2.0 L恒温恒容密闭容器中充入2.0 mol H2S,反应过程中的部分数据如下表所示:
n/mol t/min | n(H2S) | n(S2) | n(H2) |
0 | 2.0 | 0 | 0 |
2 | 1.0 | ||
4 | 0.8 | ||
6 | 0.6 |
下列说法不正确的是( )
A.0~2min 生成H2的平均反应速率为0.25 mol·L-1·min-1
B.上述反应的平衡常数K=0.675
C.3分钟时,H2S的分解率一定小于60%
D.平衡后,向容器中通入少量O2,平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在25℃时,FeS、CuS的溶度积常数(Ksp)分别为6.3×10-18、1.3×10-36。常温时下列有关说法正确的是
A. 向H2S的饱和溶液中通入少量SO2气体溶液的酸性增强
B. 将足量的CuSO4溶解在0.1 mol/L的H2S溶液中,溶液中Cu2+的最大浓度为1.3×10-35mol/L
C. 因为H2SO4是强酸,所以反应:CuSO4十H2S=CuS↓+H2SO4不能发生
D. 除去工业废水中的Cu2+可以选用FeS作沉淀剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钻钼系催化剂主要用于石油炼制等工艺,从废钴钼催化剂(主要含有![]() 、CoS和
、CoS和![]() )中回收钴和钼的工艺流程如图:
)中回收钴和钼的工艺流程如图:
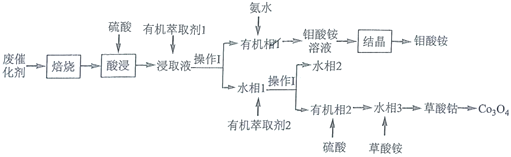
已知:浸取液中的金属离子主要为![]() 、
、![]() 、
、![]() 。
。
(1)钼酸铵![]() 中
中![]() 的化合价为________,
的化合价为________,![]() 在空气中高温焙烧产生两种氧化物:
在空气中高温焙烧产生两种氧化物:![]() 和________(填化学式)。
和________(填化学式)。
(2)为了加快酸浸速率,可采取的措施为________(任写一条)。
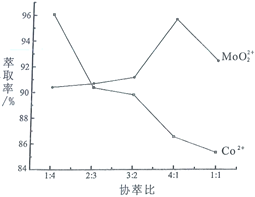
(3)若选择两种不同萃取剂按一定比例(协萃比)协同萃取![]() 和
和![]() ,萃取情况如图所示,当协萃比
,萃取情况如图所示,当协萃比![]() ________,更有利于
________,更有利于![]() 的萃取。
的萃取。
(4)操作Ⅰ的名称为________。
(5)向有机相1中滴加氨水,发生的离子方程式为________。
(6)![]() 萃取的反应原理为
萃取的反应原理为![]() ,向有机相2中加入
,向有机相2中加入![]() 能进行反萃取的原因是________(结合平衡移动原理解释)。
能进行反萃取的原因是________(结合平衡移动原理解释)。
(7)水相2中的主要溶质除了![]() ,还有________(填化学式)。
,还有________(填化学式)。
(8)![]() 可用作电极,若选用
可用作电极,若选用![]() 电解质溶液,通电时可转化为
电解质溶液,通电时可转化为![]() ,其电极反应式为________。
,其电极反应式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在密闭容器中进行反应:3SiCl4(g)+2N2(g)+6H2(g)![]() Si3N4(s)+12HCl(g)。不能表示上述反应达到化学平衡状态的是( )
Si3N4(s)+12HCl(g)。不能表示上述反应达到化学平衡状态的是( )
A.单位时间消耗2molN2,同时生成6molH2
B.c(HCl)保持不变
C.混合气体密度保持不变
D.c(N2):c(H2):c(HCl)=1:3:6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果酸的结构简式为HOOC![]() CH2—COOH,下列说法正确的是
CH2—COOH,下列说法正确的是
A. 苹果酸中能发生酯化反应的官能团有2种
B. 1mol苹果酸可与3mol NaOH发生中和反应
C. 1mol苹果酸与足量金属Na反应生成生成1mol H2
D. HOOC—CH2—CH(OH)—COOH与苹果酸互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究铁在某浓度H3PO4和H2O2的混合溶液中反应的情况,进行如下实验:
实验 | 操作 | 现象 |
Ⅰ | 将除去氧化膜的铁钉置于烧杯中,加入30mL1.0molL-1H3PO4和3mL30%H2O2的混合溶液(pH≈1)。 | 一段时间后铁钉表面突然产生大量气泡,随后停止产生气泡;一段时间后再产生大量气泡,再停止,出现周而往复的现象。过程中,溶液保持澄清。
|
Ⅱ | 将与实验Ⅰ相同的铁钉放入烧杯中,加入30mL1.0molL-1H3PO4和3mLH2O。 | 片刻后铁钉表面持续产生气泡,溶液保持澄清。 |
已知:Fe3(PO4)2难溶于水,Fe(H2PO4)2溶于水。
(1)用85%H3PO4配制100mL1.0mol·L-1H3PO4所用的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管、______。
(2)请结合实验Ⅱ中现象,分析铁钉与H3PO4反应的产物_______。
(3)探究实验Ⅰ中停止产生气泡的原因。
提出假设:铁钉表面形成了含有+3价铁的氧化膜将铁钉覆盖。甲同学进行实验Ⅲ,得出假设成立的结论。
实验Ⅲ:将洗净的实验Ⅰ中无气泡产生时的铁钉置于试管中,加入滴有KSCN溶液的稀H2SO4,振荡,静置,溶液呈红色。
乙同学认为实验Ⅲ无法证实假设成立,其理由是未排除O2的干扰,请解释O2是如何干扰实验的:_____。
乙同学通过改进实验证实了假设成立。
(4)铁钉表面突然产生大量气泡的可能原因是Fe2+迅速被H2O2氧化形成氧化膜,使聚集在铁钉表面的H2脱离铁钉表面。形成氧化膜(以Fe3O4计)的离子方程式是____。
(5)实验Ⅰ中周而往复的现象与铁钉表面氧化膜的生成和溶解密切相关,从反应的速率角度分析其原因:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由于电影《我不是药神》中对抗癌药物格列卫的关注,我国政府在2018年已经将格列卫等部分抗癌药物纳入医保用药,解决了人民群众用药负担。格列卫在其合成过程中的一种中间产物结构表示如下: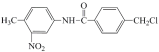 。下列有关该中间产物的说法不正确的是()
。下列有关该中间产物的说法不正确的是()
A. 该药物中间体属于芳香烃
B. 该药物中间体中含有三种官能团
C. 该药物中间体的所有碳原子可能共面
D. 该药物中间体可以发生加成反应和取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)Ge在周期表中的位置__________,基态Ge原子的核外电子排布式为[Ar] _______,有 __________个未成对电子。
(2)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Ge、O两元素电负性由大至小的顺序是 _________。
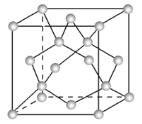
(3)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为 ________,微粒之间存在的作用力是___________。
(4)晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数a=565.76 pm(1pm=10-12m),其密度为_______g·cm-3(列出计算式即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com