
| 实验序号 | 固体质量 | 加入某浓度盐酸的体积/mL | 加入某浓度NaOH的体积/mL | 收集到气体体积/mL |
| 1 | 0.9 | 20.0 | ─ | 1008 |
| 2 | 0.9 | 30.0 | ─ | 1008 |
| 3 | 0.9 | ─ | 20.0 | 672 |
| 4 | 0.9 | ─ | 30.0 | 672 |
分析 根据实验1、2可知0.9g合金与盐酸完全反应最多生成1008mL氢气,根据实验3、4可知0.9g合金与氢氧化钠溶液反应最多生成672mL氢气,其中3、4的反应中,镁不与氢氧化钠溶液反应,只有铝反应,据此可计算出铝的物质的量、质量,从而可知合金中镁的质量,据此进行解答.
解答 解:(1)Al和NaOH溶液反应生成NaAlO2和H2,反应的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(2)根据实验3、4生成氢气的体积相等可知,氢氧化钠溶液是过量的,生成氢气的物质的量为:$\frac{0.672L}{22.4L/mol}$=0.03mol,根据反应2Al+2NaOH+2H2O=2NaAlO2+3H2↑可知合金中含有铝的物质的量为:0.03mol×$\frac{2}{3}$=0.02mol,质量为:27g/mol×0.02mol=0.54g,
则0.90g合金中镁的质量为:0.90g-0.54g=0.36g,物质的量为:$\frac{0.36g}{24g/mol}$=0.015mol,
答:每份样品中含有0.02mol铝、0.015mol镁.
点评 本题考查了混合物反应的计算,题目难度中等,根据实验3、4判断氢氧化钠溶液过量为解答关键,注意掌握物质的量与摩尔质量、气体摩尔体积之间的关系,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:解答题
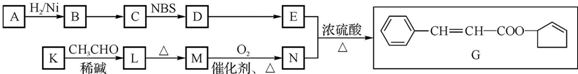
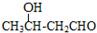
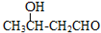 $\stackrel{△}{→}$CH3CH=CHCHO+H2O
$\stackrel{△}{→}$CH3CH=CHCHO+H2O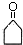 .
. .
.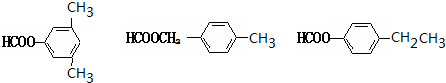 (其中两种).
(其中两种).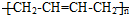 ).请设计合成路线(其他无机原料任选)并用如下方式表示:A$→_{反应条件}^{反应试剂}$B$→_{反应条件}^{反应试剂}$…目标产物HOCH2CH2CH2CH3$→_{△}^{浓H_{2}SO_{4}}$CH2=CHCH2CH3$\stackrel{NBS}{→}$CH2=CHCHBrCH3$→_{△}^{氢氧化钠醇溶液}$CH2=CHCH=CH2$\stackrel{催化剂}{→}$
).请设计合成路线(其他无机原料任选)并用如下方式表示:A$→_{反应条件}^{反应试剂}$B$→_{反应条件}^{反应试剂}$…目标产物HOCH2CH2CH2CH3$→_{△}^{浓H_{2}SO_{4}}$CH2=CHCH2CH3$\stackrel{NBS}{→}$CH2=CHCHBrCH3$→_{△}^{氢氧化钠醇溶液}$CH2=CHCH=CH2$\stackrel{催化剂}{→}$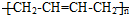 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔是把物质的质量和微观粒子数联系起来的一个基本物理量 | |
| B. | 1摩尔H2SO4的质量为98g/mol | |
| C. | 国际上规定,0.012 kg 碳原子所含有的碳原子数目为 1 mol | |
| D. | 1摩尔氢气分子可以表示为1mol H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾--Al2(SO4)3•12H2O | B. | 漂白粉--NaClO | ||
| C. | 苏打粉--NaHCO3 | D. | 水煤气--CO、H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | m=4 R2+是还原剂 | B. | m=n R3+是氧化产物 | ||
| C. | m=2 R2+是氧化剂 | D. | m=y R3+是还原产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3 mL | B. | 7.5 mL | C. | 15 mL | D. | 22.5 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Na2O2+2Mn2O7→4NaMnO4+O2↑ | B. | 2Na2O2+P2O3→Na4P2O7 | ||
| C. | 2Na2O2+2 N2O3→NaNO2+O2↑ | D. | 2 Na2O2+2 N2O5→4NaNO3+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com