
下列变化或数据与氢键无关的是( )
|
| A. | 水凝结成冰时,密度变小 |
|
| B. | 氨分子与水分子形成一水合氨 |
|
| C. | 水在2000℃时,只有4%的H2O发生分解 |
|
| D. | SbH3的沸点比PH3高 |
考点:
含有氢键的物质.
专题:
化学键与晶体结构.
分析:
F、O、N的电负性较强,对应的氢化物分子之间能形成氢键,氢键的存在,影响到物质的某些性质.如熔点、沸点,溶解度,粘度,密度等.
解答:
解:A、冰和水的密度不同主要是由于水分子间存在氢键,氢键在水液态是使一个水分子与4个水分子相连,而当水凝固时氢键会拉伸水分子 使水分子之间距离增大 体积也就增大了,密度也就小了,故A有关;
B、O、N的电负性较强,对应的氢化物分子之间能形成氢键,所以氨分子与水分子之间能形成氢键,故B有关;
C、水在2000℃时,只有4%的H2O发生分解,是因为水中氧和氢之间的共价键很牢固,不易断裂,所以与氢键无关,故C无关;
D、Sb和P同属第VA族,SbH3和PH3结构相似,而SbH3的相对分子质量比PH3大,分子间作用力强,导致SbH3的沸点比PH3高,与氢键无关,故D无关.
故选CD.
点评:
本题考查了氢键和共价键知识,侧重于氢键对物质的性质的影响,题目难度不大,学习中注意总结该部分知识.


科目:高中化学 来源: 题型:
有机物A是常用的食用油抗氧化剂,分子式为C10H12O5,可发生如下转化:

已知B的相对分子质量为60,分子中只含一个甲基.C的结构可表示为: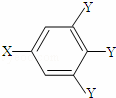 (其中:﹣X、﹣Y均为官能团).
(其中:﹣X、﹣Y均为官能团).
请回答下列问题:
(1)根据系统命名法,B的名称为 .
(2)官能团﹣X的名称为 ,高聚物E的链节为 .
(3)A的结构简式为 .
(4)反应⑤的化学方程式为 .
(5)C有多种同分异构体,写出其中2种符合下列要求的同分异构体的结构简式 (写出上述3个结构简式中的任意2个即可) .
i.含有苯环 ii.能发生银镜反应 iii.不能发生水解反应
(6)从分子结构上看,A具有抗氧化作用的主要原因是 (填序号).
a.含有苯环 b.含有羰基 c.含有酚羟基.
查看答案和解析>>
科目:高中化学 来源: 题型:
实验中的下列操作正确的是( )
A. 用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中
B. Ba(NO3)2溶于水,可将含有Ba(NO3)2的废液倒入水槽中,再用水冲入下水道
C. 用蒸发方法使NaCl 从溶液中析出时,应将蒸发皿中NaCl 溶液全部加热蒸干
D. 用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于丙烯(CH3﹣CH=CH2)的说法正确的( )
|
| A. | 丙烯分子有8个σ键,1个π键 |
|
| B. | 丙烯分子中3个碳原子都是sp3杂化 |
|
| C. | 丙烯分子不存在非极性键 |
|
| D. | 丙烯分子中3个碳原子在同一直线 |
查看答案和解析>>
科目:高中化学 来源: 题型:
第四周期元素的单质及化合物在工农业生产中应用广泛.
(1)第四周期元素中,基态原子的最外层只有1个电子的元素共有 种.元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.该元素的基态原子价电子排布为 .
(2)铂丝蘸取氯化钙在酒精灯上灼烧,火焰呈现砖红色,显色原因是 (填序号).
A.氯化钙受热挥发 B.氯化钙受热分解
C.钙离子中电子跃迁 D.氯离子中电子跃迁
(3)无水硫酸铜呈白色,吸水后形成胆矾,呈蓝色.科学家通过X射线测定出胆矾的结构,其结构可用如图表示.
①胆矾晶体中除共价键、配位键及微弱的范德华力外,还存在的两种作用力是 和 .
②胆矾晶体CuSO4•5H2O可以写出[Cu(H2O)4]SO4•H2O,其中配位原子是 ,配位数是 .
③铜离子形成胆矾中配位离子的离子方程式为 .
④CO、NH3等也能与Cu+形成配合物.[Cu(NH3)n]+溶液可用于吸收合成氨原料气中的CO,加热吸收CO后的溶液又将放出CO.加热分解放出CO的过程中,必须克服微粒间的哪类作用力? .
⑤过渡金属配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n= .
(4)Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据如右表.据表判断Mn2+和Fe2+再失去﹣个电子的难易,并从原子结构的角度简述其原因 .
| 元素 | Mn | Fe |
|
| 电离能kJ•mol﹣1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 |

查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | 1 mol物质的质量就是该物质的摩尔质量 |
|
| B. | 1 mol气体的体积就是气体摩尔体积 |
|
| C. | 1 mol任何粒子的相应粒子数叫做阿伏加德罗常数 |
|
| D. | 1 mol HCl溶于1 L水中,所得盐酸的物质的量浓度为1 mol•L﹣1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
完成下列反应的离子方程式:
①碳酸钙溶于醋酸中 ;
②向稀氨水中加入稀盐酸 ;
③向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式: ;在以上中性溶液中继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
如图为元素周期表中短周期的一部分,四种元素中只有一种是金属,下列说法错误的是( )

|
| A. | 气态氢化物稳定性:R>Q |
|
| B. | 元素T的离子结构示意图为 |
|
| C. | 与w同主族的某元素形成的18电子的氢化物分子中只有共价键没有离子键 |
|
| D. | Q可形成多种含氧酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com