
【题目】已知X、Y、Z、W四种物质存在如图转化关系,下列判断正确的是
![]()
A.若W是一种常见的金属单质,则X可能为![]()
B.若W为强碱,Y为白色难溶于水的固体,则工业上可以电解X的水溶液来制取其中所含的金属
C.若W固体俗称干冰,则Y晶体中的阴、阳离子个数比为1∶1
D.若W是![]() ,则Y一定是酸性氧化物
,则Y一定是酸性氧化物
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某相对分子质量为40的链状不饱和烃A,能发生如下转化:
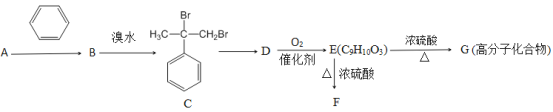
已知:①羟基所连接的碳原子上无氢原子时,难以发生催化氧化;②E能与NaHCO3溶液反应产生气体;③F为酯类化合物。
(1)A的分子式为_____________,A转化为B的反应类型为______________,C转化为D的反应条件为_________________。
(2)B中所含有的官能团的名称为_____________,B中共平面的原子最多有________个。
(3)写出D转化为E的化学方程式:__________________
(4)与E互为同分异构体的芳香族化合物K,已知:①K与E具有相同的官能团;②K不能与FeCl3溶液发生显色反应;③K有二个取代基,则符合上述条件的K共有_________。(填字母代号)
a.3种 b.6种 c. 9种 d.12种
(5)F的结构简式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.在锌与某浓度的盐酸反应的实验中,实验员得到下面的结果:
锌的质量(g) | 锌的形状 | 温度(℃) | 溶解于酸花的时间(s) | |
A | 2 | 薄片 | 5 | 400 |
B | 2 | 薄片 | 15 | 200 |
C | 2 | 薄片 | 25 | 100 |
D | 2 | 薄片 | 35 | 50 |
E | 2 | 薄片 | 45 | 25 |
F | 2 | 粉末 | 15 | 5 |
(1)写出实验中发生反应的离子方程式:___________,该反应是_____反应(填“放热”或“吸热”);
(2)仔细观察A~F的实验数据对比,你可以得到关于温度影响反应速率结论,用此结论,计算:55℃时,2g锌薄片溶解于酸中需花____ s。
(3)对比结果B与F,解释结果F那么快的原因:________
Ⅱ.某可逆反应在某体积为5L的密闭容器中进行,在从0~4分钟各物质的量的变化情况如图所示(X、Y、Z均为气体)。
(1)该反应的的化学方程式为_______;
(2)反应开始至2分钟时,X的平均反应速率为______;
(3)能说明该反应已达到平衡状态的是______;
a.每消耗3molX,同时消耗1molY
b.容器内压强保持不变
c.Z的浓度不再变化
d.容器内混合气体的密度保持不变
(4)由下图求得平衡时Y的转化率为_____。
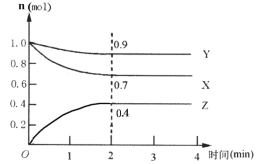
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学化学常见物质A~I的转化关系如框图所示,其中A为化合物,B为常见金属单质,H的焰色反应为黄色,Y不使品红溶液褪色。(部分反应条件、溶剂及产物已略去)
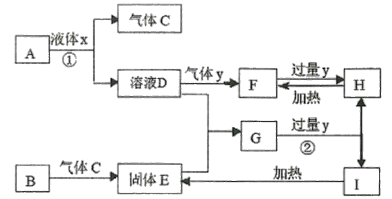
(1)反应①、②的离子方程式________________、__________。
(2)现有含0.10 mol H的溶液,要使其转化成含0.10 mol F的溶液,则:
①若只能加入0.050 mol的某物质,该物质可能是_________________ (填化学式,写1种)。
②若只能加入0.10 mol的某物质,该物质可能是_________________ (填化学式,写1种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁与稀硝酸的反应为:Mg+ HNO3(稀)—— Mg(NO3)2+ NO↑+ H2O
(1)配平上述化学方程式并用“双线桥法”表示该反应中电子转移的方向和数目。________
(2)该反应中,还原产物是_________,HNO3表现了______________(选填“还原性”、“氧化性”、“酸性”、“碱性”)。
(3)若反应过程中转移的电子为0.6 mol,则被还原的硝酸物质的量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芜湖即将成为安徽省第二个拥有轨道交通的城市。芜湖轨道交通(如图)采用单轨系统,当单轨电车开动时,车上裸露的“电刷”沿架空电线滑动,这种运行方式具有便捷、污染小的特点。下列有关说法不正确的一项是

A.“电刷”材料中很有可能含有石墨
B.“电刷”材料一定含有导电性、润滑性极好的材料
C.采用单轨系统提高了能量的利用效率,符合绿色化学的要求
D.单轨列车运行时,供电原理与原电池类似
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家哈迈德·泽维尔研究运用激光技术观察化学反应时分子中原子的运动,在研究中证实光可诱发如图所示的变化。下列叙述不正确的是

A.两物质的分子式相同
B.两物质均可发生加成反应
C.两物质分子中所有原子不可能处于同一平面上
D.两物质都不能生成高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I)我国化工专家侯德榜的“侯氏制碱法” 又叫“联合制碱法”以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱Na2CO3,有关反应的化学方程式:
(1)____;
(2)____。
(II).取一定量的酸性KMnO4溶液依次进行下列实验,有关现象记录如下:①滴加适量H2O2,紫红色褪去,并有气泡产生;②再加入适量的PbO2固体,固体溶解,溶液又变为紫红色; ③最后通入足量的SO2气体。请回答下列问题:
(1)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为__;
(2)实验③中的现象为__;
(3)实验①、②中反应的离子方程式分别是__、___。
(III)铝与NaOH溶液反应同温同压下,在体积和浓度均为100mL2mol·L1的盐酸和NaOH溶液中各加入等质量的Al,产生气体的体积之比为5∶6,则所加Al的质量为__g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲酸(HCOOH)是还原性酸,又称作蚁酸,常用于橡胶、医药、染料、皮革等工业生产。某化学兴趣小组在分析甲酸的组成和结构后,对甲酸的某些性质进行了探究。请回答下列问题。
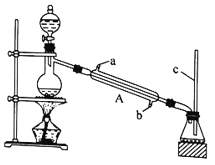
I.甲酸能与醇发生酯化反应
该兴趣小组用如上图所示装置进行甲酸(HCOOH)与甲醇(CH3OH)的酯化反应实验:
有关物质的性质如下:
沸点/℃ | 密度(g·cm-3) | 水中溶解性 | |
甲醇 | 64.5 | 0.79 | 易溶 |
甲酸 | 100.7 | 1.22 | 易溶 |
甲酸甲酯 | 31.5 | 0.98 | 易溶 |
(1)装置中,仪器A的名称是_________________,长玻璃管c的作用是__________________________。
(2)甲酸和甲醇进行酯化反应的化学方程式为____________________________________________。
(3)要从锥形瓶内所得的混合物中提取甲酸甲酯,可采用的方法为__________________________________。
II.甲酸能脱水制取一氧化碳

(1)利用上图装置制备并收集CO气体,其正确的连接顺序为a→__________(按气流方向从左到右,用小写字母表示)。
(2)装置B的作用是__________________________________。
(3)一定条件下,CO能与NaOH固体发生反应:CO+NaOH ![]() HCOONa。
HCOONa。
①为了证明“CO与NaOH固体发生了反应”,设计下列定性实验方案:取固体产物,配成溶液,___________。
②测定产物中甲酸钠(HCOONa)的纯度:准确称取固体产物8,0g配制成100mL溶液,量取20.00mL该溶液于锥形瓶中,再加入___________作指示剂,用1.5mol/L的盐酸标准溶液滴定剩余的NaOH,平行滴定三次,平均消耗盐酸的体积为5.05mL,则产物中甲酸钠的质量分数为_______(计算结果精确到0.1%)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com