
| A. | 若X、Y原子序数相差l,Y为IIA族,则X一定是IIIA族 | |
| B. | 若Y(OH)m易溶于水,则X(OH)n一定不溶于水 | |
| C. | 若HnXOm为强酸,则X的氢化物溶液于水一定显酸性 | |
| D. | 若Y元素形成的单质是气体,则X元素形成的单质一定也是气体 |
分析 X原子的半径比Y的半径小,且具有相同的电子层数,说明二者在周期表中同一周期,根据同周期从左到右原子半径逐渐减小,可知X的原子序数比Y的大,在周期表中Y的右侧,Y还可以是IIIB族,不一定是IIIA,以此进行判断.
解答 解:X原子的半径比Y的半径小,且具有相同的电子层数,说明二者在周期表中同一周期,根据同周期从左到右原子半径逐渐减小,可知X的原子序数比Y的大,在周期表中Y的右侧,
A.XY原子序数不一定相差1,可以相差2或更多,如Na与Mg或Al或S等,Y还可以是IIIB族,不一定是IIIA,故A错误;
B.若Y(OH)m易溶于水,则X(OH)n可能溶于水,如第四周期中K、Ca元素形成的碱KOH和Ca(OH)2,故B错误;
C.如X为N元素,则X的氢化物为NH3溶液于水呈碱性,故C错误;
C、若Y元素形成的单质是气体,则Y可能是N或O,X可能为O或F元素,则X元素形成的单质一定是气体,故D正确;
故选D.
点评 本题考查同周期元素单质及其化合物的性质,题目难度中等,把握同周期元素的性质递变规律是本题的关键.


科目:高中化学 来源: 题型:填空题
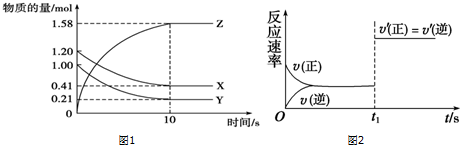
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
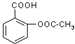 试根据阿斯匹林的结构回答;
试根据阿斯匹林的结构回答; ,其分子式为C7H6O3,则B的结构简式为CH3COOH;
,其分子式为C7H6O3,则B的结构简式为CH3COOH;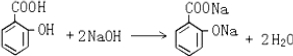 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 CuI是一种不溶于水的白色固体,它可以由反应2Cu2++4I-═2CuI↓+I2而得到.如图所示装置中,a、b都是惰性电极,通电一段时间后,在KI淀粉溶液中阳极周围变蓝色,则下列说法正确的是( )
CuI是一种不溶于水的白色固体,它可以由反应2Cu2++4I-═2CuI↓+I2而得到.如图所示装置中,a、b都是惰性电极,通电一段时间后,在KI淀粉溶液中阳极周围变蓝色,则下列说法正确的是( )| A. | 若b极变红,则在Cu极上:Cu-2e-═Cu2+,Cu2+显蓝色 | |
| B. | 若a极变红,则在Pt电极上:2I--2e-═I2,淀粉遇碘变蓝 | |
| C. | 若a极变红,则在Cu电极上:开始Cu+I--e-═CuI,一段时间后2I--2e-═I2,淀粉遇碘变蓝 | |
| D. | 若b极变红,则在Pt电极上:4OH--4e-═2H2O+O2↑,O2将I-氧化为I2,淀粉遇碘变蓝 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | 试剂 | 分离方法 | |
| ① | 硝酸钾(氯化钠) | 蒸馏水 | 降温结晶 |
| ② | Na2SO4(NH4Cl) | 加入升华 | |
| ③ | 乙醇(水) | 金属钠 | 蒸馏 |
| ④ | NaCl溶液(Na2S) | AgCl | 过滤 |
| A. | ①③ | B. | ①④ | C. | 只有② | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中可能含有非极性键 | B. | 分子晶体中的分子内不含有离子键 | ||
| C. | 原子晶体中可能含有非极性键 | D. | 分子晶体中的分子内一定有共价键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com