
已知下列热化学方程式
Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g)
ΔH1=-25 kJ·mol-1 ①
3Fe2O3(s)+CO(g)===2Fe3O4(s)+CO2(g)
ΔH2=-47 kJ·mol-1 ②
Fe3O4(s)+CO(g)===3FeO(s)+CO2(g)
ΔH3=19 kJ·mol-1 ③
写出FeO(s)被CO还原成Fe和CO2的热化学方程式____________________________
________________________________________________________________________。
 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案科目:高中化学 来源: 题型:
能源和资源是维系人类发展的重要前提之一。目前人类使用的主要能源还是化石燃料。请回答下列问题:
(1)化石燃料包括煤、石油、 (写出另外一种化石燃料的名称)。煤炭开采过程中,若采取的措施不当,容易发生瓦斯爆炸事故,导致生命财产损失,用化学方程式解释在煤矿中频频发生瓦斯爆炸的原因:
。
(2)煤的气化可以缓解石油危机,而目前煤的气化主要是煤中的碳和水蒸气的反应:C+H2O(g)===CO+H2,该反应是一个吸热反应,反应所需的能量一般是由间歇进行的碳的燃烧(氧气用空气代替)来提供的:C+O2===CO2。
①有人认为上述第一个反应需要吸热,所以煤的气化从能量角度来看,得不偿失。请你解释这种观点的错误所在:
。
②煤的气化可以为工业合成氨提供原料气。氢气来源于 ,氮气来源于 ,还可以采用 工艺得到空气中的氮气。
(3)我国煤炭资源相对石油和天然气资源丰富,煤制油有一定的资源保障。煤液化的重要方法是间接液化法,首先将煤气化为H2、CO和CH4,然后通过催化剂将气态物质转化为液态。通过间接法制备的燃油中含有饱和烷烃和不饱和烯烃,请完成下列粗煤气合成烯烃和烷烃的化学方程式:
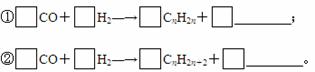
查看答案和解析>>
科目:高中化学 来源: 题型:
银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故。根据电化学原理可进行如下处理:在铝质容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色会褪去。下列说法正确的是
A.处理过程中银器一直保持恒重
B.银器为正极,Ag2S被还原生成单质银
C.该过程中总反应为
D.黑色褪去的原因是黑色Ag2S转化为白色AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
根据元素周期表中第四周期元素的相关知识,回答下列问题:
(1)第四周期元素的基态原子的电子排布中4s轨道上只有1个电子的元素有一种;
写出的核外电子排布式_________。
 (2)按电子排布,可将周期表里的元素划分成五个区域,第四周期元素中属于s区的元素有___________种,属于d区的元素有________种。
(2)按电子排布,可将周期表里的元素划分成五个区域,第四周期元素中属于s区的元素有___________种,属于d区的元素有________种。
(3)Ca0晶胞如右图所示,Ca0晶体中Ca2+的
配位数为________;Ca0的焰色反应为砖红色,许多
金属或它们的化合物都可以发生焰色反应,其原因
是________。
(4)由叠氮化钾(KN3)热分解可得纯 ,下列有关说法正
,下列有关说法正
确的是________(填选项字母)。
A.NaN3与KN3结构类似,前者晶格能较小
B.晶体钾的晶胞结构如右图所示,每个晶胞中分摊2个钾原子
C.氮的第一电离能大于氧
D.氮气常温下很稳定,是因为氮的电负性小
(5)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂。O2在其催化作用下,可将CN-氧化成CNO-。CN-的电子式为________,CNO-的中心原子的杂化方式为____________。
(6)在CrCl3溶液中,一定条件下存在组成为 (n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:
(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:

将含0.0015mol 的溶液,与R-H完全交换后,中和生成的需浓度为
的溶液,与R-H完全交换后,中和生成的需浓度为
0.1200 mol NaOH溶液25.00 mL,则该配离子的化学式为____________。
NaOH溶液25.00 mL,则该配离子的化学式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
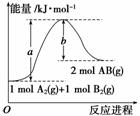
已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,请写出该反应的热化学方程式:________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
能源问题是现代社会发展的三大基本问题之一,能源家族中:①煤炭、②核能、③石油、④天然气、⑤水能、⑥风能、⑦地热能等,属于不可再生的是________;属于新能源的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变为H2、CO。其过程如下:
mCeO2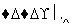 (m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+xH2O+xCO2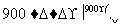 mCeO2+xH2+xCO
mCeO2+xH2+xCO
下列说法不正确的是 ( )
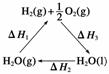 A.该过程中CeO2没有消耗
A.该过程中CeO2没有消耗
B.该过程实现了太阳能向化学能的转化
C.右图中ΔH1=ΔH2+ΔH3
D.以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH--2e-===CO +2H2O
+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
请参考题中图表,已知E1=134 kJ·mol-1、E2=368 kJ·mol-1,根据要求回答问题:
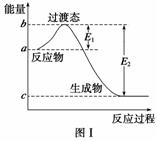

(1)图Ⅰ是1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是________(填“增大”、“减小”或“不变”,下同),ΔH的变化是________。请写出NO2和CO反应的热化学方程式:________________________________。
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应的热化学方程式如下:
①CH3OH(g)+H2O(g)===CO2(g)+3H2(g)
ΔH=49.0 kJ·mol-1
②CH3OH(g)+ O2(g)===CO2(g)+2H2(g)
O2(g)===CO2(g)+2H2(g)
ΔH=-192.9 kJ·mol-1
又知③H2O(g)===H2O(l) ΔH=-44 kJ·mol-1,则甲醇蒸气燃烧为液态水的热化学方程式为________________________________________________________________________。
(3)下表是部分化学键的键能参数:
| 化学键 | P—P | P—O | O===O | P===O |
| 键能/kJ·mol-1 | a | b | c | x |
已知白磷的燃烧热为d kJ·mol-1,白磷及其完全燃烧的产物的结构如图Ⅱ所示,则表中x=________ kJ·mol-1(用含a、b、c、d的代表数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com