
| A. | 工业采用火法炼铜:Cu2S+O2=2Cu+SO2 每生成2mol铜,反应共转移4NA个电子 | |
| B. | 7.8g过氧化钠粉末与足量二氧化硫反应转移的电子数为0.1NA | |
| C. | CO2通过Na2O2使其增重bg时,反应中转移的电子数为$\frac{b{N}_{A}}{44}$ | |
| D. | 0.01molMg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数目为0.02NA |
分析 A.C依据Cu2S+O2$\frac{\underline{\;高温\;}}{\;}$2Cu+SO2中,Cu元素的化合价由+1价降低为0,O元素的化合价由0降低为-2价,S元素的化合价由-2价升高为+4价判断解答;
B.求出过氧化钠的物质的量,然后根据过氧化钠与二氧化硫反应时,过氧化钠中氧元素的价态由-1价变为-2价来分析;
C.二氧化碳与过氧化钠的反应中,固体增重的部分为CO的质量,根据n=$\frac{m}{M}$计算出二氧化碳的物质的量,再计算出生成氧气的量及转移的电子数;
D.镁与氧气、氮气反应生成物质中,镁都是+2价,依据反应的镁失去电子数计算.
解答 解;A.每生产1molCu,0.5molS失去电子,需转移0.5mol×[4-(-2)]=3mol电子,则每生成2mol铜,反应共转移6NA个电子,故A错误;
B.7.8g过氧化钠的物质的量为0.1mol,而过氧化钠与二氧化硫反应时,过氧化钠做氧化剂,氧元素的价态由-1价变为-2价,故0.1mol过氧化钠转移0.2mol电子即0.2NA个,故B错误;
C.将二氧化碳通过过氧化钠固体,固体增加的质量相当于是CO的质量,根据C原子守恒,参加反应的二氧化碳的物质的量为:$\frac{bg}{28g/mol}$=$\frac{b}{28}$mol,$\frac{b}{28}$mol二氧化碳完全反应转移了$\frac{b}{28}$mol电子,反应中转移电子数为$\frac{b}{28}$NA,故C错误;
D.0.01mol Mg在空气中完全燃烧生成MgO和Mg3N2,依据反应的镁失去电子数计算转移的电子数目为0.02NA,故D正确;
故选:D.
点评 本题考查阿伏加德罗常数的综合应用,题目难度中等,主要考查氧化还原反应的电子守恒,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确过氧化钠与二氧化碳反应实质是解题关键.


科目:高中化学 来源: 题型:推断题
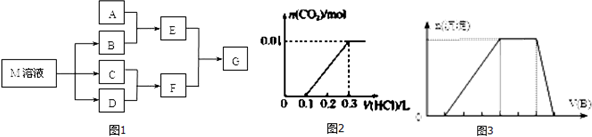
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两原子N层上都有1个s电子,一个原子有d电子,另一个原子无d电子 | |
| B. | 最外层电子排布为2s22p6的原子和最外层电子排布为2s22p6的离子 | |
| C. | 原子核外M层上的s、p轨道都充满电子,而d轨道上没有电子的两种原子 | |
| D. | 两原子的核外全部都是s电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
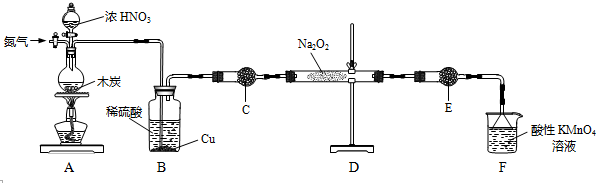
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法,有机物 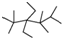 的命名为2,3,3,5,5五甲基-4,4-二乙基己烷 的命名为2,3,3,5,5五甲基-4,4-二乙基己烷 | |
| B. |  主链上的碳原子数是5 主链上的碳原子数是5 | |
| C. | 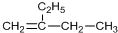 加氢后可以得到3-甲基戊烷 加氢后可以得到3-甲基戊烷 | |
| D. |  的名称是1,3,4-三甲基苯 的名称是1,3,4-三甲基苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
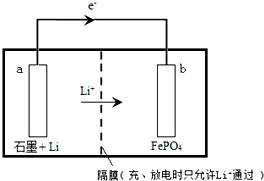 LiFePO4用于锂离子二次电池的电极材料,可由LiI和FePO4制备.
LiFePO4用于锂离子二次电池的电极材料,可由LiI和FePO4制备.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
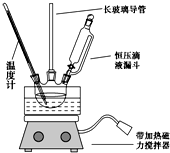 硝基苯是重要的精细化工原料,是医药和染料的中间体,还可作有机溶剂.
硝基苯是重要的精细化工原料,是医药和染料的中间体,还可作有机溶剂. HNO3(浓)$→_{98%浓H_{2}SO_{4}}^{50~60℃}$
HNO3(浓)$→_{98%浓H_{2}SO_{4}}^{50~60℃}$ +H2O
+H2O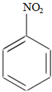 +HNO3(浓)$→_{98%浓H_{2}SO_{4}}^{95℃}$
+HNO3(浓)$→_{98%浓H_{2}SO_{4}}^{95℃}$ +
+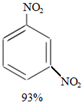 +
+
| 物质 | 熔点/℃ | 沸点/℃ | 密度(20℃) | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 1,3二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
| 浓硝酸[来] | - | 83 | 1.4 | 易溶于水 |
| 浓硫酸 | - | 338 | 1.84 | 易溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 X、Y、Z、W为短周期的主族元素,其原子序数依次增大.X元素形成的单质是自然界中含量最多的气体.Y是电负性最大的元素.W的原子最外层电子数与核外电子总数之比为3:8.X的原子序数是Z的原子序数的一半.U是第四周期11列元素.
X、Y、Z、W为短周期的主族元素,其原子序数依次增大.X元素形成的单质是自然界中含量最多的气体.Y是电负性最大的元素.W的原子最外层电子数与核外电子总数之比为3:8.X的原子序数是Z的原子序数的一半.U是第四周期11列元素.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
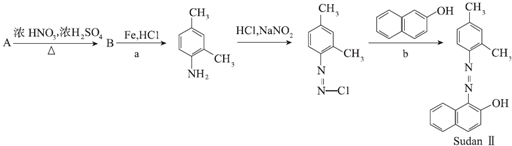
 .
.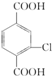 +4NaOH→
+4NaOH→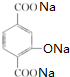 +NaCl+3H2O.②E→F
+NaCl+3H2O.②E→F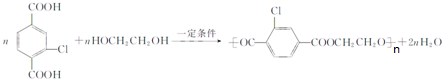 .
.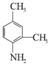 和另一种含氮有机分子G,G分子既能与氢氧化钠溶液反应,也能与盐酸反应.G分子中氮元素的质量分数为8.8%.
和另一种含氮有机分子G,G分子既能与氢氧化钠溶液反应,也能与盐酸反应.G分子中氮元素的质量分数为8.8%.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com