
| A. | X、Y、Z三种元素中的两种或三种只能生成2种18电子的分子 | |
| B. | Z2X4可作为火箭发动机的燃料 | |
| C. | WX2中只含离子键 | |
| D. | Z的氢化物比Y的氢化物更稳定 |
分析 前20号的四种元素X、Y、Z、W,原子序数依次增大.Y形成的化合物种类最多,Y为C元素;X和Y可形成原子个数比为1:1和2:1的二元化合物,如C2H2、C2H4,可知X为H;Z元素形成的单质是空气中的主要成分,X和Z可形成化合物Z2X4,Z为N元素;化合物WX2为离子化合物,可与水反应生成气体,W元素的含量在地壳中排在第五位,W为Ca元素,以此来解答.
解答 解:由上述分析可知,X为H,Y为C,Z为N,W为Ca,
A.X、Y、Z三种元素中的两种或三种可形成N2H4、C2H6、CH3NH2等18电子的分子,故A错误;
B.Z2X4为N2H4,与氧化剂N2O4反应生成N2和水蒸气,释放能量,可作为火箭发动机的燃料,故B正确;
C.CaH2为离子化合物,只含离子键,故C正确;
D.非金属性N>C,则Z的氢化物比Y的氢化物更稳定,故D正确;
故选A.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子序数、元素化合物知识来推断元素为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用及18电子分子的判断,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 反应中MnO2是还原剂 | |
| B. | 电池工作时,海水起导电作用,其中NaCl浓度保持不变 | |
| C. | Ag为负极,电极反应为Ag-e-+Cl-=AgCl | |
| D. | 每生成1 mol Na2Mn5Ol0转移1mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤炭经蒸馏、气化和液化等过程,可获得清洁能源和重要的化工原料 | |
| B. | 医药中常用酒精来消毒,是因为酒精能够使细菌蛋白发生变性 | |
| C. | “海水淡化”可以解决淡水供应危机,向海水中加入明矾可以使海水淡化 | |
| D. | 新型材料聚酯纤维、光导纤维都属于有机高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | CO、SO2、SO3均是酸性氧化物 | |
| B. | 图示转化反应均为氧化还原反应 | |
| C. | 工业上用氯气和石灰乳制取漂白粉的反应中原子利用率为100% | |
| D. | 严禁用工业酒精勾兑饮用酒是因为工业酒精中含有有毒的甲醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.0 mol•L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- | |
| B. | 饱和氯水中:NH4+、SO32-、AlO2-、Cl- | |
| C. | 与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- | |
| D. | c(H+)=1.0×10-13mol/L溶液中:K+、Na+、CH3COO-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素Q是短周期非金属性最强的元素 | |
| B. | Y、Z形成的化合物中只有一种属于酸性氧化物 | |
| C. | Y、Z、Q分别与W形成的化合物中,Z形成的化合物的沸点最低 | |
| D. | X分别与Y、Z、W形成的化合物中可能既含离子键又含共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在强碱溶液中:Na+.K+.AlO2-.CO32- | |
| B. | 在含大量Fe3+的溶液中:NH4+.Na+.Cl-.SCN- | |
| C. | 在c(H+)=10-13mol/L 的溶液中:NH4+.Al3+.SO42-.NO3- | |
| D. | 在pH=1的溶液中:K+.Fe2+.Cl-.NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
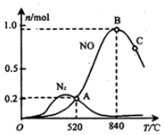 (1)科学家寻找高效催化剂,通过如下反应实现大气污染物转化:
(1)科学家寻找高效催化剂,通过如下反应实现大气污染物转化:| 化学键 | N≡N | O=O | NO中氮氧键 |
| 键能(kJ/mol) | 945 | 498 | 630 |
| 时间(min) | 0 | 5 | 10 | 15 | 20 | 25 |
| c(NH3)/mol•L-1 | 1.00 | 0.36 | 0.12 | 0.08 | 0.0072 | 0.0072 |
| c(O2)/mol•L-1 | 2.00 | 1.20 | 0.90 | 0.85 | 0.84 | 0.84 |
 ,羟胺是一种还原剂,现用25.00mL 0.049mol/L的羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+恰好与24.50mL0.020mol/L的KMnO4酸性溶液完全作用,则在上述反应中,羟胺的氧化产物是N2O.
,羟胺是一种还原剂,现用25.00mL 0.049mol/L的羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+恰好与24.50mL0.020mol/L的KMnO4酸性溶液完全作用,则在上述反应中,羟胺的氧化产物是N2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
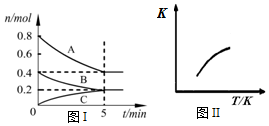 固定容积为2L的密闭容器中发生反应xA(g)+yB(g)?zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系.结合图象判断,下列结论正确的是( )
固定容积为2L的密闭容器中发生反应xA(g)+yB(g)?zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系.结合图象判断,下列结论正确的是( )| A. | 200℃时,反应从开始到平衡的平均速率v(A)=0.08 mol•L-1•min-1 | |
| B. | 200℃时,若在第6 min再向体系中充入1 mol He,此时v(正)>v(逆) | |
| C. | 若0~5 min内容器与外界的热交换总量为m kJ,则该反应的热化学方程式可表示为:2A(g)+B(g)?C(g)△H=+5m kJ/mol | |
| D. | 200℃时,平衡后再充入2 mol C,则再次达到平衡时,C的体积分数等于0.25 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com