
| A. | 非金属性:X<W<Y<Z | |
| B. | X的简单阴离子和Z、W的简单离子均能促进水的电离 | |
| C. | 原子半径:Z<Y<W,而简单离子半径:W<Y<Z | |
| D. | Y的最高价氧化物对应的水化物与W的单质反应可制备X的单质 |
分析 原子序数依次增大的X、Y、Z、W四种短周期元素,X、W原子的最外层电子数与其电子层数相等,满足条件的元素有:H、Be、Al,X能够形成气体甲,则X只能为H;气体甲由X、Y两种元素组成,其在标准状况下的密度为0.76g•L-1,甲的摩尔质量为:M=0.76g/L×22.4L/mol=17.0g/mol,则甲为NH3,则Y为N元素;W原子的最外层电子数与其电子层数相等且原子序数大于N,所以W是Al元素;X、Z的最外层电子数之和与Y、W的最外层电子数之和相等,所以Z的最外层电子数为:5+3-1=7,则Z为F元素;根据分析可知,X为H、Y为N、Z为F、W为Al元素,结合物质的结构和性质解答.
解答 解:原子序数依次增大的X、Y、Z、W四种短周期元素,X、W原子的最外层电子数与其电子层数相等,满足条件的元素有:H、Be、Al,X能够形成气体甲,则X只能为H;气体甲由X、Y两种元素组成,其在标准状况下的密度为0.76g•L-1,甲的摩尔质量为:M=0.76g/L×22.4L/mol=17.0g/mol,则甲为NH3,则Y为N元素;W原子的最外层电子数与其电子层数相等且原子序数大于N,所以W是Al元素;X、Z的最外层电子数之和与Y、W的最外层电子数之和相等,所以Z的最外层电子数为:5+3-1=7,则Z为F元素,
A.根据分析可知,X为H、Y为N、Z为F、W为Al元素,非金属性:W<X<Y<Z,故A错误;
B.X的简单阴离子为H-离子,H-离子与水电离的氢离子反应生成氢气,促进了水的电离;Z、W的简单离子分别为氟离子、铝离子,二者都能够水解,均能促进水的电离,故B正确;
C.电子层越多,原子半径越大,电子层相同时核电荷数越大,原子半径越小,则原子半径Z<Y<W,离子半径大小为:W<Z<Y,故C错误;
D.Y为N,其最高价氧化物对应的水合物为硝酸,硝酸与Al反应不会生成氢气,故D错误;
故选B.
点评 本题考查了原子结构与元素周期律的关系,题目难度中等,推断元素为解答关键,注意掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的灵活应用能力.


 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:选择题
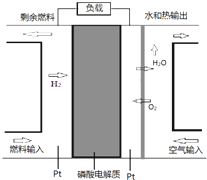 某种PAFC是以磷酸为电解质、Pt为电极的燃料电池(如图所示),具有电解质稳定、构造简单等特点.浓磷酸的凝固点是42°C,PAFC的工作温度通常在150-220°C.以下说法错误的是( )
某种PAFC是以磷酸为电解质、Pt为电极的燃料电池(如图所示),具有电解质稳定、构造简单等特点.浓磷酸的凝固点是42°C,PAFC的工作温度通常在150-220°C.以下说法错误的是( )| A. | 电池中H+向空气输入端的电极移动 | |
| B. | 正极电极反应式:O2+2H2O+4e-═4OH- | |
| C. | 常温下使用该燃料电池性能将降低 | |
| D. | 若以甲醇做燃料,负极电极反应式:CH3OH+H2O-6e-═CO2↑+6H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向稀盐酸中加入少量钠粒:2Na+2H2O→2Na++2OH-?+H2↑ | |
| B. | NaHSO4溶液与Ba(OH)2溶液混合呈中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O | |
| C. | 用漂白粉溶液吸收尾气中SO2:Ca2++2ClO-+SO2+H2O→CaSO3↓+2HClO | |
| D. | 向含氯化铝的氯化镁溶液中加入氧化镁:2Al3++3MgO+3H2O=2Al(OH)3↓+3Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池工作时,电子由正极通过外电路流向负极 | |
| B. | 电池正极的电极反应式为:MnO2(s)+H2O(l)+e-═MnOOH(s)+OH-(aq) | |
| C. | 电池工作时,锌发生氧化反应 | |
| D. | 当电路中通过0.2mol电子,锌的质量理论上减小6.5g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
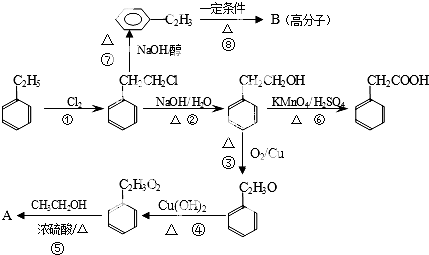
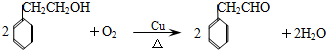
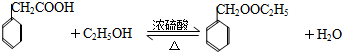
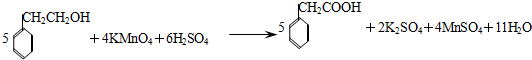

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol N2所含有的原子数为NA | |
| B. | 标准状况下,22.4 L水中含有的水分子数为NA | |
| C. | 24 g O2分子和24 g O3分子所含的氧原子数目相等 | |
| D. | 1mol•L-1的盐酸中氯离子为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有羟基的有机物都能与醋酸发生酯化反应 | |
| B. | 氨基酸、乙酸和苯酚都能与氢氧化钠溶液反应 | |
| C. | 醇类、卤代烃都能发生消去反应 | |
| D. | 除饱和烃之外的其他烃都能发生聚合反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
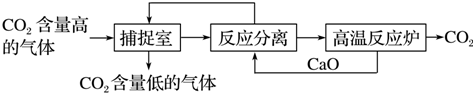
| A. | 生产过程中,可循环利用的物质有CaO和NaOH | |
| B. | 该方法涉及了化合、分解和复分解等反应类型 | |
| C. | 该方法通过化学变化,分离、提纯并利用CO2,可以减少碳的排放 | |
| D. | “反应分离”环节中,分离物质的基本操作是蒸发、结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用S制备H2SO4 | B. | 用CaCO3、Na2CO3、SiO2生产玻璃 | ||
| C. | 将海水中的MgSO4转变为金属Mg | D. | 用NO2生产HNO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com