
| A£® | ŅŃÖŖA-+H2B£Ø¹żĮ棩ØTHA+HB-£¬Ōņ½įŗĻH+µÄÄÜĮ¦£ŗHB-£¼A-£¼B2- | |
| B£® | ŌŚ0.1 mol?L-1µÄ°±Ė®ÖŠµĪ¼Ó0.1 mol?L-1ŃĪĖį£¬Ē”ŗĆĶźČ«ÖŠŗĶŹ±ČÜŅŗµÄpH=a£¬ŌņÓÉĖ®µēĄė²śÉśµÄc£ØOH-£©=10-a mol?L-1 | |
| C£® | ½«c mol?L-1µÄ“×ĖįČÜŅŗÓė0.02 mol?L-1NaOHČÜŅŗµČĢå»ż»ģŗĻŗóČÜŅŗĒ”ŗĆ³ŹÖŠŠŌ£¬ÓĆŗ¬cµÄ“śŹżŹ½±ķŹ¾CH3COOHµÄµēĄė³£ŹżKa=$\frac{{2”Į1{0^{-9}}}}{c-0.02}$ | |
| D£® | ½«0.2 mol•L-1ŃĪĖįÓė0.1 mol•L-1µÄKAlO2ČÜŅŗµČĢå»ż»ģŗĻ£¬ČÜŅŗÖŠĄė×ÓÅضČÓɓ󵽊”µÄĖ³Šņ£ŗ c£ØCl-£©£¾c£ØK+£©£¾c£ØAl3+£©£¾c£ØH+£©£¾c£ØOH-£© |
·ÖĪö A£®H2B+A-=HB-+HA£¬ŌņĖįŠŌ£ŗH2B£¾HB-£¾HA£¬ĖįŠŌŌ½Ē棬ĘäŅõĄė×ÓĖ®½āÄÜĮ¦Ō½Čõ£¬½įŗĻÖŹ×ÓµÄÄÜĮ¦Ō½Čõ£»
B£®Ē”ŗĆĶźČ«·“Ó¦Ź±ČÜŅŗµÄpH=a£¬·“Ӧɜ³ÉĀČ»Æļ§£¬Ė®½āĻŌĖįŠŌ£»
C£®³£ĪĀĻĀĮ½ČÜŅŗ·“Ó¦ŗó³ŹÖŠŠŌ£¬Ōņc£ØH+£©=c£ØOH-£©=10-7mol/L£¬c£ØNa+£©=c£ØCH3COO-£©=0.01mol/L£¬¾Ż“Ė½įŗĻ“×ĖįµÄµēĄėĘ½ŗā³£Źż±ķ“ļŹ½¼ĘĖć£»
D£®½«0.2 mol•L-1ŃĪĖįÓė0.1 mol•L-1µÄKAlO2ČÜŅŗµČĢå»ż»ģŗĻÉś³ÉµÄĒāŃõ»ÆĀĮ²æ·ÖČܽāÉś³ÉĀČ»ÆĀĮČÜŅŗ£¬ĀĮĄė×ÓĖ®½āČÜŅŗĻŌĖįŠŌ£®
½ā“š ½ā£ŗA£®ĖįŠŌ£ŗH2B£¾HB-£¾HA£¬ĖįŠŌŌ½Ē棬ĘäŅõĄė×Ó½įŗĻÖŹ×ÓµÄÄÜĮ¦Ō½Čõ£¬ŌņA-£¾B2-£¾HB-£¬¹ŹA“ķĪó£»
B£®ŌŚ0.1mol•L-1°±Ė®ÖŠµĪ¼Ó0.1mol•L-1ŃĪĖį£¬øÕŗĆĶźČ«ÖŠŗĶÉś³ÉĀČ»Æļ§£¬ļ§øłĄė×ÓĖ®½ā“Ł½ųĮĖĖ®µÄµēĄė£¬“ĖŹ±pH=a£¬ŌņČÜŅŗÖŠĖ®µēĄėµÄc£ØOH-£©=c£ØH+£©=10-amol•L-1£¬¹ŹBÕżČ·£»
C£®·“Ó¦ŗóČÜŅŗ³ŹÖŠŠŌ£¬Ōņc£ØH+£©=c£ØOH-£©=10-7mol/L£¬c£ØNa+£©=c£ØCH3COO-£©=0.01mol/L£¬øł¾ŻĪļĮĻŹŲŗć£¬·“Ó¦ŗóČÜŅŗÖŠ“×ĖįµÄÅضČĪŖ£ŗ£Ø$\frac{c}{2}$-0.1£©mol/L£¬
ĖłŅŌÓĆŗ¬cµÄ“śŹżŹ½±ķŹ¾CH3COOHµÄµēĄė³£ŹżĪŖ£ŗKa=$\frac{1{0}^{-7}”Į0.01}{\frac{c}{2}-0.01}$=$\frac{2”Į1{0}^{-9}}{c-0.02}$£¬¹ŹCÕżČ·£»
D£®½«0.2 mol•L-1ŃĪĖįÓė0.1 mol•L-1µÄKAlO2ČÜŅŗµČĢå»ż»ģŗĻÉś³ÉµÄĒāŃõ»ÆĀĮ²æ·ÖČܽāÉś³ÉĀČ»ÆĀĮČÜŅŗ£¬ĀĮĄė×ÓĖ®½āČÜŅŗĻŌĖįŠŌ£¬ČÜŅŗÖŠHCl+NaAlO2+H2O=Al£ØOH£©3+KCl£¬Al£ØOH£©3+3HCl=AlCl3+3H2O£¬ČÜŅŗÖŠĄė×ÓÅضČĪŖ£ŗc£ØCl-£©£¾c£ØK+£©£¾c£ØAl3+£©£¾c£ØH+£©£¾c£ØOH-£©£¬¹ŹDÕżČ·£»
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éĮĖČõµē½āÖŹµēĄėĘ½ŗā”¢ĖįŠŌ±Č½Ļ”¢ŃĪĄąĖ®½āµČ£¬ÕĘĪÕ»ł“”ŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®


 ŠĀæĪ±ź½×ĢŻŌĶĮѵĮ·ĻµĮŠ“š°ø
ŠĀæĪ±ź½×ĢŻŌĶĮѵĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¶žŃõ»ÆĮņÄÜŹ¹øßĆĢĖį¼ŲĖįŠŌČÜŅŗŃøĖŁĶŹÉ« | |
| B£® | æÉŅŌÓĆ³ĪĒåŹÆ»ŅĖ®¼ų±š¶žŃõ»ÆĮņŗĶ¶žŃõ»ÆĢ¼ | |
| C£® | Įņ·ŪŌŚ¹żĮæµÄ“æŃõÖŠČ¼ÉÕæÉŅŌÉś³ÉČżŃõ»ÆĮņ | |
| D£® | ÉŁĮ涞Ńõ»ÆĮņĶØČėÅصÄĀČ»ÆøĘČÜŅŗÖŠÄÜÉś³É°×É«³Įµķ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µŚ¢ńA×åŌŖĖŲ“ÓÉĻµ½ĻĀ£¬µ„ÖŹµÄČŪµćÖš½„½µµĶ | |
| B£® | ¶ąµē×ÓŌ×ÓÖŠ£¬ŌŚĄėŗĖ½Ļ½üµÄĒųÓņÄŚŌĖ¶ÆµÄµē×ÓÄÜĮæ½ĻµĶ | |
| C£® | ĖłÓŠÖ÷×åŌŖĖŲŌ×ÓµÄ×īĶā²ćµē×ÓŹż¶¼µČÓŚŌŖĖŲµÄ×īøßÕż»ÆŗĻ¼Ū | |
| D£® | ŌŖĖŲÖÜĘŚ±ķÖŠĪ»ÓŚ½šŹōŗĶ·Ē½šŹō·Ö½ēĻßø½½üµÄŌŖĖŲŹōÓŚ¹ż¶ÉŌŖĖŲ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
 ÓŠ»śĪļ A ŹĒŅ»ÖÖ“æ¾»µÄĪŽÉ«š¤³ķŅŗĢ壬Ņ×ČÜÓŚĖ®£®ĪŖŃŠ¾æ A µÄ×é³ÉÓė½į¹¹£¬½ųŠŠĮĖČēĻĀŹµŃ飬ŹµŃé²½Öč£ŗ
ÓŠ»śĪļ A ŹĒŅ»ÖÖ“æ¾»µÄĪŽÉ«š¤³ķŅŗĢ壬Ņ×ČÜÓŚĖ®£®ĪŖŃŠ¾æ A µÄ×é³ÉÓė½į¹¹£¬½ųŠŠĮĖČēĻĀŹµŃ飬ŹµŃé²½Öč£ŗ £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øŹÓĶ×÷»¤·ō±£ŹŖ¼ĮŹĒŅņĪŖøŹÓĶÓŠ»¹ŌŠŌ | |
| B£® | ·žÓĆøõŗ¬Į泬±źµÄŅ©ÓĆ½ŗÄŅ»į¶ŌČĖ¶Ō½”æµŌģ³ÉĪ£ŗ¦ | |
| C£® | ”°ŃŖŅŗĶøĪö”±ĄūÓĆĮĖ½ŗĢåµÄŠŌÖŹ | |
| D£® | ĘĻĢŃÖŠµÄ»ØĒąĖŲŌŚ¼īŠŌ»·¾³ĻĀĻŌĄ¶É«£¬¹ŹæÉÓĆĖÕ“ņ·Ū¼ģŃé¼Łŗģ¾Ę |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĪŖĮĖøųČĖĄąŅ»øöĆĄŗĆĄ¶Ģģ£¬»Æ¹¤ĘóŅµĶĘ½ųĶŃĮņ”¢ĶŃĻõ”¢³ż³¾µČÉ菩øÄŌģ£¬ÄÜ“óĮæ¼õÅÅSO2”¢NO2 | |
| B£® | ”°PM2.5”±ŹĒÖø“óĘųÖŠÖ±¾¶Š”ÓŚ»ņµČÓŚ2.5”Į10-6mµÄĻøŠ”æÅĮ£Īļ£¬ÕāŠ©æÅĮ£Ą©É¢ŌŚæÕĘųÖŠŠĪ³É½ŗĢå | |
| C£® | ŹµŃé³”ĖłŃĻ½ūŠÆ“ųŹ³Īļ£»½ūÖ¹ÓĆŅūĮĻĘæ×°»ÆѧŅ©Ę·£¬·ĄÖ¹ĪóŹ³ | |
| D£® | Ī÷·Ē¹ś¼Ņ±¬·¢µÄ°£²©ĄŅßĒé³Ź¼ÓĖŁĀūŃÓÖ®ŹĘ£¬ŅŃÖŖøĆ²”¶¾¶Ō»ÆѧŅ©Ę·ĆōøŠ£¬Ė«ŃõĖ®”¢”°84”±Ļū¶¾Ņŗ¾łæÉŅŌ½«²”¶¾Ńõ»Æ¶ų“ļµ½Ļū¶¾µÄÄæµÄ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā

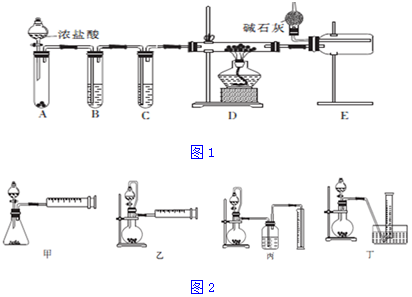
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 ÓėNaOHĖ®ČÜŅŗ¹²ČČ£¬Éś³ÉµÄÓŠ»śĪļµÄ½į¹¹¼ņŹ½ĪŖ
ÓėNaOHĖ®ČÜŅŗ¹²ČČ£¬Éś³ÉµÄÓŠ»śĪļµÄ½į¹¹¼ņŹ½ĪŖ £®
£® £»ČōøĆÓŠ»śĪļÓŠŅ»øö·“Ź½Ņģ¹¹Ģ壬ĒŅÄÜÓėĒāĘų¼Ó³ÉÉś³É2-¼×»łĪģĶ飬ŌņøĆÓŠ»śĪļµÄ½į¹¹¼ņŹ½ĪŖ
£»ČōøĆÓŠ»śĪļÓŠŅ»øö·“Ź½Ņģ¹¹Ģ壬ĒŅÄÜÓėĒāĘų¼Ó³ÉÉś³É2-¼×»łĪģĶ飬ŌņøĆÓŠ»śĪļµÄ½į¹¹¼ņŹ½ĪŖ £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com