
ŅŃÖŖ£ŗ95”ꏱ£¬KW=1.0”Į10£12.ŌŚøĆĪĀ¶ČĻĀ,²āµĆ0.1mol”¤L£1Na2AČÜŅŗPH=6,ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®H2AŌŚĖ®ČÜŅŗÖŠµÄµēĄė·½³ĢŹ½ĪŖ£ŗH2A 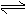 H++HA-£¬HA£
H++HA-£¬HA£ 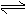 H++A2-
H++A2-
B£®£ØNH4£©2AČÜŅŗÖŠ“ęŌŚĄė×ÓÅØ¶Č¹ŲĻµ£ŗc£ØNH4+£©>c£ØA2-£©>c(H+£©>c£ØOH££©
C£®0.0lmol”¤L-lµÄH2AČÜŅŗpH=2
D£®µČĢå»żµČÅØ¶ČµÄŃĪĖįÓėH2AČÜŅŗ·Ö±šÓė5.6g Zn·“Ó¦£¬H2AČÜŅŗ²śÉśµÄH2¶ą
”¾ÖŖŹ¶µć”æĖ®µÄĄė×Ó»ż³£Źż”¢ČÜŅŗpHÖµ”¢ŃĪČÜŅŗÖŠĄė×ÓÅØ¶Č H1 H2 H3
”¾“š°ø½āĪö”æB½āĪö£ŗøł¾Ż95”ꏱ£¬KW=1.0”Į10£12.ŌŚøĆĪĀ¶ČĻĀ,²āµĆ0.1mol·L£1Na2AČÜŅŗPH=6,æÉÖŖČÜŅŗ³ŹÖŠŠŌ£¬Na2AĪŖĒæĖįĒæ¼īŃĪ”£A”¢H2AĪŖĒæĖįŌŚĖ®ČÜŅŗÖŠĶźČ«µēĄė£¬¹ŹA“ķĪó£»B”¢£ØNH4£©2AĪŖĒæĖįČõ¼īŃĪ£¬ČÜŅŗ³ŹĖįŠŌ£¬ČÜŅŗÖŠ“ęŌŚĄė×ÓÅØ¶Č¹ŲĻµ£ŗc£ØNH4+£©>c£ØA2-£©>c(H+£©>c£ØOH££©£¬¹ŹBÕżČ·£»C”¢0.0lmol·L-lµÄH2AČÜŅŗĒāĄė×ÓÅضČĪŖ0.02mol·L-l£¬pH²»µČÓŚ2£¬¹ŹC“ķĪó£»D”¢µČĢå»żµČÅØ¶ČµÄŃĪĖįÓėH2AČÜŅŗ·Ö±šÓė5.6g Zn·“Ó¦£¬ČōĖį¶¼¹żĮ棬Į½ČÜŅŗ²śÉśµÄH2Ņ»Ńł¶ą£¬¹ŹD“ķĪó”£
¹Ź“š°øŃ”B
”¾Ė¼Ā·µć²¦”æ±¾Ģāæ¼²éĮĖĖ®µÄĄė×Ó»ż³£Źż”¢ČÜŅŗpHÖµ”¢ŃĪČÜŅŗÖŠĄė×ÓÅØ¶ČµČĪŹĢā£¬×ŪŗĻŠŌĒ棬¹Ų¼üŹĒĄūÓĆ95”ꏱ£¬KW=1.0”Į10£12ŗĶŌŚøĆĪĀ¶ČĻĀ0.1mol·L£1Na2AČÜŅŗPH=6,ÅŠ¶ĻH2AŹĒĒæĖį”£


 ĆūŹ¦Öøµ¼ĘŚÄ©³å“Ģ¾ķĻµĮŠ“š°ø
ĆūŹ¦Öøµ¼ĘŚÄ©³å“Ģ¾ķĻµĮŠ“š°ø æŖŠÄĶÜæŚĖćĢāæØĻµĮŠ“š°ø
æŖŠÄĶÜæŚĖćĢāæØĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠČÜŅŗÖŠ£¬ø÷×éĄė×ÓæÉÄÜ“óĮæ¹²“ęµÄŹĒ (””””)
A£®pH£½7µÄČÜŅŗÖŠ£ŗK£«”¢Fe3£«”¢Cl£”¢NO3”Ŗ
B£®ĒæĖįŠŌČÜŅŗÖŠ£ŗCu2£«”¢ClO£”¢Cl£”¢Ba2£«
C£®0.1 mol”¤L£1 µÄNaHCO3ČÜŅŗÖŠ£ŗK£«”¢Al3£«”¢Fe3£«”¢NO3”Ŗ
D£®ÓÉĖ®µēĄė³öµÄc(H£«)£½10£13 mol”¤L£1µÄČÜŅŗÖŠ£ŗAl3£«”¢K£«”¢NO3”Ŗ”¢SO42”Ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Įņ“śĮņĖįÄĘ£ØNa2S2O3”¤5H2O£©Ė×Ćū”°“óĖÕ“ņ”±£¬ÓÖ³ĘĪŖ”°ŗ£²Ø”±£¬æÉÓĆÓŚÕÕĻąŅµ×÷¶ØÓ°¼Į£¬Ņ²æÉÓĆÓŚÖ½½¬ĘÆ°××÷ĶŃĀČ¼ĮµČ”£ĖüŅ×ČÜÓŚĖ®£¬ÄŃČÜÓŚŅŅ“¼£¬¼ÓČČ”¢ÓöĖį¾łŅ×·Ö½ā”£¹¤ŅµÉĻ³£ÓĆŃĒĮņĖįÄĘ·Ø”¢Įņ»Æ¼ī·ØµČÖʱø”£Ä³ŹµŃéŹŅÄ£Äā¹¤ŅµĮņ»Æ¼ī·ØÖĘČ”Įņ“śĮņĖįÄĘ£¬Ę䷓ӦװÖĆ¼°ĖłŠčŹŌ¼ĮČēĻĀĶ¼£ŗ
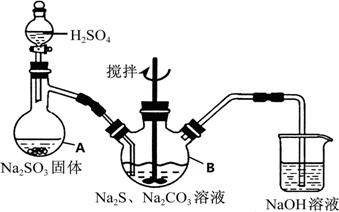
ŹµŃé¾ßĢå²Ł×÷²½ÖčĪŖ£ŗ
¢ŁæŖĘō·ÖŅŗĀ©¶·£¬Ź¹ĮņĖįĀżĀżµĪĻĀ£¬ŹŹµ±µ÷½Ś·ÖŅŗµÄµĪĖŁ£¬Ź¹·“Ó¦²śÉśµÄSO2ĘųĢå½Ļ¾łŌȵŲ
ĶØČėNa2SŗĶNa2CO3µÄ»ģŗĻČÜŅŗÖŠ£¬Ķ¬Ź±æŖĘōµē¶Æ½Į°čĘ÷½Į¶Æ£¬Ė®Ō”¼ÓČČ£¬Ī¢·Š”£
¢ŚÖ±ÖĮĪö³öµÄ»ė×Ē²»ŌŁĻūŹ§£¬²¢æŲÖĘČÜŅŗµÄpH½Ó½ü7Ź±£¬Ķ£Ö¹ĶØČėSO2ĘųĢ唣
¢Ū³ĆČČ¹żĀĖ£¬½«ĀĖŅŗ¼ÓČČÅØĖõ£¬ĄäČ“Īö³öNa2S2O3”¤5H2O”£
¢ÜŌŁ¾¹żĀĖ”¢Ļ“µÓ”¢øÉŌļ£¬µĆµ½ĖłŠčµÄ²śĘ·”£
£Ø1£©Š“³öŅĒĘ÷AµÄĆū³Ę ²½Öč¢ÜÖŠĻ“µÓŹ±£¬ĪŖĮĖ¼õÉŁ²śĪļµÄĖšŹ§ÓƵďŌ¼ĮæÉŅŌŹĒ ”£
£Ø2£©ĪŖĮĖ±£Ö¤Įņ“śĮņĖįÄĘµÄ²śĮ棬ŹµŃéÖŠ²»ÄÜČĆČÜŅŗpH<7£¬ĒėÓĆĄė×Ó·½³ĢŹ½½āŹĶŌŅņ ”£
£Ø3£©Š“³öČż¾±ÉÕĘæBÖŠÖĘČ”Na2S2O3·“Ó¦µÄ×Ü»Æѧ·“Ó¦·½³ĢŹ½
ӣ
£Ø4£©×īŗóµĆµ½µÄ²śĘ·ÖŠæÉÄÜŗ¬ÓŠNa2SO4ŌÓÖŹ”£ĒėÉč¼ĘŹµŃé¼ģ²ā²śĘ·ÖŠŹĒ·ń“ęŌŚNa2SO4£¬¼ņŅŖĖµĆ÷ŹµŃé²Ł×÷£¬ĻÖĻóŗĶ½įĀŪ£ŗ
ӣ
 £Ø5£©²ā¶Ø²śĘ·“æ¶Č
£Ø5£©²ā¶Ø²śĘ·“æ¶Č
×¼Č·³ĘČ”1.00 g²śĘ·£¬ÓĆŹŹĮæÕōĮóĖ®Čܽā£¬ŅŌµķ·Ū×÷ÖøŹ¾¼Į£¬ÓĆ0£®100 0 mol”¤L£1µāµÄ±ź×¼ČÜŅŗµĪ¶Ø”£·“Ó¦ŌĄķĪŖ2S2O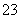 £«I2===S4O
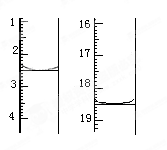
£«I2===S4O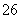 £«2I£”£µĪ¶ØĘšŹ¼ŗĶÖÕµćµÄŅŗĆęĪ»ÖĆČēĶ¼£ŗ
£«2I£”£µĪ¶ØĘšŹ¼ŗĶÖÕµćµÄŅŗĆęĪ»ÖĆČēĶ¼£ŗ
ŌņĻūŗĵāµÄ±ź×¼ČÜŅŗĢå»żĪŖ_______mL”£²śĘ·µÄ“æ¶ČĪŖ
%ӣ
£Ø6£©Na2S2O3³£ÓĆ×÷ĶŃĀČ¼Į£¬ŌŚČÜŅŗÖŠŅ×±»Cl2Ńõ»Æ³ÉSO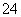 £¬øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ______________________________”£
£¬øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ______________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
V L Fe2(SO4)3ČÜŅŗÖŠŗ¬ÓŠa g SO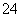 £¬Č”“ĖČÜŅŗ0.5V L£¬ÓĆĖ®Ļ”ŹĶÖĮ2V L£¬ŌņĻ”ŹĶŗóČÜŅŗÖŠFe3£«µÄĪļÖŹµÄĮæÅضČĪŖ(””””)
£¬Č”“ĖČÜŅŗ0.5V L£¬ÓĆĖ®Ļ”ŹĶÖĮ2V L£¬ŌņĻ”ŹĶŗóČÜŅŗÖŠFe3£«µÄĪļÖŹµÄĮæÅضČĪŖ(””””)
A.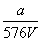 mol·L£1 B.
mol·L£1 B.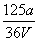 mol·L£1
mol·L£1
C.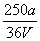 mol·L£1 D.
mol·L£1 D.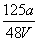 mol·L£1
mol·L£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ć¾”¢ĀĮŗĻ½š3 gÓė100 mLĻ”H2SO4Ē”ŗĆĶźČ«·“Ó¦£¬½«·“Ó¦ŗóĖłµĆČÜŅŗÕōøÉ£¬µĆĪŽĖ®ĮņĖįŃĪ17.4 g£¬ŌņŌĮņĖįČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ(””””)
A£®1.5 mol·L£1 B£®1 mol·L£1
C£®2.5 mol·L£1 D£®2 mol·L£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ķ¬Ī»ĖŲŹ¾×Ł·ØæÉÓĆÓŚ·“Ó¦»śĄķµÄŃŠ¾æ£¬ĻĀĮŠ·“Ó¦»ņ×Ŗ»ÆÖŠĶ¬Ī»ĖŲŹ¾×Ł±ķŹ¾ÕżČ·µÄŹĒ £Ø £©
A£®2Na218O2 + 2H2O = 4Nal8OH + O2”ü
B£®NH4Cl + 2H2O  NH3·2H2O + HCl
NH3·2H2O + HCl
C£®2KMnO4 + 5H218O2 + 3H2SO4= K2SO4 + 2MnSO4 + 518O2”ü + 8H2O
D£®K37ClO3 + 6HCl = K37Cl + 3Cl2”ü + 3H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
³£ĪĀĻĀ£¬¶ŌpH=10µÄNaHCO3ČÜŅŗÖŠ£¬ø÷Ī¢Į£µÄĪļÖŹµÄĮæÅØ¶Č·ÖĪöÕżČ·µÄŹĒ£Ø £©
A£®c(CO32—)£¾c(H2CO3)
B£®c(Na£«)£¾c(HCO3—)£¾c(OH”Ŗ)£¾c(H£«)
C£®c(Na£«)£«c(H£«)£½c(HCO3—)£«c(CO32—)£«c(OH”Ŗ)
D£®c(Na£«)£½c(HCO3—)£«c(CO32—)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÖŲøõĖįÄĘ(Na2Cr2O7”¤2H2O)Ė׳Ęŗģ·ÆÄĘ£¬ŌŚ¹¤Ņµ·½ĆęÓŠ¹ć·ŗÓĆĶ¾”£ĪŅ¹śÄæĒ°Ö÷ŅŖŹĒŅŌøõĢśæó£ØÖ÷ŅŖ³É·ŻĪŖFeO”¤Cr2O3£¬»¹ŗ¬ÓŠAl2O3”¢MgO”¢SiO2µČŌÓÖŹ£©ĪŖÖ÷ŅŖŌĮĻ½ųŠŠÉś²ś£¬ĘäÖ÷ŅŖ¹¤ŅÕĮ÷³ĢČēĻĀ£ŗ
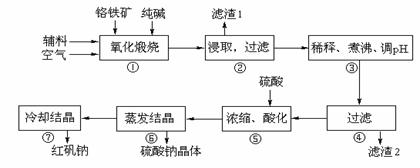
¢ŁÖŠÉę¼°µÄÖ÷ŅŖ·“Ó¦ÓŠ£ŗ
Ö÷·“Ó¦£ŗ4FeO”¤Cr2O3£«8Na2CO3£«7O2  8Na2CrO4£«2Fe2O3£«8CO2
8Na2CrO4£«2Fe2O3£«8CO2
ø±·“Ó¦£ŗSiO2£«Na2CO3 Na2SiO3£«CO2”ü”¢Al2O3£«Na2CO3
Na2SiO3£«CO2”ü”¢Al2O3£«Na2CO3 2NaAlO2£«CO
2NaAlO2£«CO 2”ü
2ӟ
²æ·ÖŃōĄė×ÓŅŌĒāŃõ»ÆĪļŠĪŹ½ĶźČ«³ĮµķŹ±ČÜŅŗµÄpH£ŗ
| ³ĮµķĪļ | Al(OH)3 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 |
| ĶźČ«³ĮµķŹ±ČÜŅŗpH | 4.7 | 3.7 | 11.2 | 5.6 |
ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
¢Å”°¢Ł”±ÖŠ·“Ó¦ŹĒŌŚ»Ų×ŖŅ¤ÖŠ½ųŠŠ £¬·“Ó¦Ź±Šč²»¶Ļ½Į°č£¬Ęä×÷ÓĆŹĒ
£¬·“Ó¦Ź±Šč²»¶Ļ½Į°č£¬Ęä×÷ÓĆŹĒ
¢Ę ”°¢Ū”±ÖŠµ÷½ŚpHÖĮ4.7£¬ÄæµÄŹĒ ”£
¢Ē ”°¢Ż”±ÖŠ¼ÓĮņĖįĖį»ÆµÄÄæµÄŹĒŹ¹CrO42£×Ŗ»ÆĪŖCr2O72££¬ĒėŠ“³öøĆĘ½ŗā×Ŗ»ÆµÄĄė×Ó·½³ĢŹ½£ŗ ”£
£Ø 4£©³ĘČ”ÖŲøõĖįÄĘŹŌŃł2.5000 gÅä³É250 mLČÜŅŗ£¬Č”³ö25.00 mLÓŚµāĮæĘæÖŠ£¬¼ÓČė10 mL 2 mol”¤L£1H2SO4ŗĶ×ćĮæµā»ÆÄĘ£ØøõµÄ»¹Ō²śĪļĪŖCr3£«)£¬·Å
4£©³ĘČ”ÖŲøõĖįÄĘŹŌŃł2.5000 gÅä³É250 mLČÜŅŗ£¬Č”³ö25.00 mLÓŚµāĮæĘæÖŠ£¬¼ÓČė10 mL 2 mol”¤L£1H2SO4ŗĶ×ćĮæµā»ÆÄĘ£ØøõµÄ»¹Ō²śĪļĪŖCr3£«)£¬·Å ÓŚ°µ“¦5 min£¬Č»ŗó¼ÓČė100 mLĖ®£¬¼ÓČė3 mLµķ·ŪÖøŹ¾¼Į£¬ÓĆ0.1200 mol”¤L£1Na2S2O3±ź×¼ČÜŅŗµĪ¶Ø£ØI2£«2S2O32£=2I££«S4O62££©”£
ÓŚ°µ“¦5 min£¬Č»ŗó¼ÓČė100 mLĖ®£¬¼ÓČė3 mLµķ·ŪÖøŹ¾¼Į£¬ÓĆ0.1200 mol”¤L£1Na2S2O3±ź×¼ČÜŅŗµĪ¶Ø£ØI2£«2S2O32£=2I££«S4O62££©”£
¢ŁÅŠ¶Ļ“ļµ½µĪ¶ØÖÕµćµÄŅĄ¾ŻŹĒ£ŗ____________________________________£»
¢ŚČōŹµŃéÖŠ¹²ÓĆČ„Na2S2O3±ź×¼ČÜŅŗ40.00 mL£¬ĖłµĆ²śĘ·µÄÖŠÖŲøõĖįÄʵēæ¶Č£ØÉčÕūøö¹ż³ĢÖŠĘäĖüŌÓÖŹ²»²ĪÓė·“Ó¦£©__________________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŠæŗĶ¶žŃõ»ÆĆĢŹĒµē³Ų¹¤ŅµÖŠµÄÖ÷ŅŖŌĮĻ,ĘäÖŠŅ»ÖÖZn”Ŗ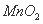 Ķ¬²Ūµē½āµÄ¹¤ŅµÉś²śŹŌŃ鹤ŅÕĮ÷³ĢÉę¼°µÄÖ÷ŅŖ·“Ó¦ÓŠ: ¢Ł
Ķ¬²Ūµē½āµÄ¹¤ŅµÉś²śŹŌŃ鹤ŅÕĮ÷³ĢÉę¼°µÄÖ÷ŅŖ·“Ó¦ÓŠ: ¢Ł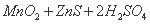 ===
===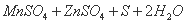
 ¢Ś
¢Ś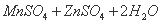
 ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ( )
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ( )
A.¢ŁÖŠ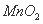 ŹĒŃõ»Æ¼Į
ŹĒŃõ»Æ¼Į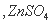 ŹĒ»¹Ō²śĪļ
ŹĒ»¹Ō²śĪļ
B.¢ŁÖŠĆæ²śÉś16 g SŹ±×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ2 mol
C.°“ÕÕ¢Śµē½āŹ±,Éś³É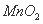 µÄµē¼«ĪŖŅõ¼«
µÄµē¼«ĪŖŅõ¼«
D.øĆ¹¤ŅÕĮ÷³ĢÖŠ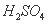 æÉŃ»·
æÉŃ»·
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com