

| A、从能量转换角度来看,框图中的氯碱工业是一个将电能转化为化学能量的过程 |
| B、过程①中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
| C、过程②中结晶出的MgCl2?6H2O要在HCl氛围中加热脱水制得无水MgCl2 |
| D、在过程③⑤中溴元素均被氧化 |


科目:高中化学 来源: 题型:
| A、都正确 | B、都错误 |
| C、甲对乙错 | D、甲错乙对 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ag+、Al3+、K+ |
| B、SiO32-、AlO2-、K+ |
| C、Ag+、Cu2+、Na+ |
| D、Ag+、Ba2+、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、臭氧比氧气的氧化性更强,常温下能将银、汞等较不活泼的金属氧化 |
| B、臭氧是比氯水更好的消毒剂,因为它在消灭细菌后变成O2,无污染 |
| C、臭氧和活性炭一样,能够吸附有机色素,是种很好的漂白剂 |
| D、臭氧和氧气在一定条件下可以相互转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 浓硫酸和2mol?L-1的稀硫酸,在实验室中敞口放置.它们的质量和放置天数的关系如图,分析a、b曲线变化的原因是( )
浓硫酸和2mol?L-1的稀硫酸,在实验室中敞口放置.它们的质量和放置天数的关系如图,分析a、b曲线变化的原因是( )| A、a升华、b冷凝 |
| B、a挥发、b吸水 |
| C、a蒸发、b潮解 |
| D、a冷凝、b吸水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
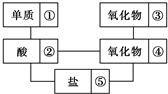 在稀硫酸、小苏打、二氧化碳、铜片、食盐、生石灰、三氧化钨、铁片和木炭粉9种物质中,存在下面的相互关系,选择①~⑤为适当的物质,使有连线的两种物质能发生反应.
在稀硫酸、小苏打、二氧化碳、铜片、食盐、生石灰、三氧化钨、铁片和木炭粉9种物质中,存在下面的相互关系,选择①~⑤为适当的物质,使有连线的两种物质能发生反应.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com