
| A£® | ÄÜČÜÓŚĖ® | |
| B£® | ÄÜŹ¹×ĻÉ«ŹÆČļŹŌŅŗ±äŗģ | |
| C£® | Äܱ»Čõ¼ī°±Ė®ÖŠŗĶ | |
| D£® | ³£ĪĀĻĀ£¬0.1 mol•L-1“×ĖįČÜŅŗÖŠµÄc£ØH+£©ĪŖ1.32”Į10-3mol•L-1 |
·ÖĪö ĒæČõµē½āÖŹµÄøł±¾Ēų±šŹĒµēĄė³Ģ¶Č£¬ĶźČ«µēĄėµÄµē½āÖŹŹĒĒæµē½āÖŹ£¬²æ·ÖµēĄėµÄµē½āÖŹŹĒČõµē½āÖŹ£¬Ö»ŅŖÄÜĖµĆ÷“×Ėį²æ·ÖµēĄė¾ĶÄÜÖ¤Ć÷“×ĖįŹĒČõµē½āÖŹ£¬¾Ż“Ė·ÖĪö½ā“š£®
½ā“š ½ā£ŗA£®µē½āÖŹµÄČܽā¶Č“󊔲»ÄÜČ·¶Øµē½āÖŹĒæČõ£¬ČēAgClÄŃČÜÓŚĖ®µ«AgClŹĒĒæµē½āÖŹ£¬ĖłŅŌ²»ÄÜøł¾Ż“×ĖįÄÜČÜÓŚĖ®¶ųÅŠ¶Ļ“×ĖįŹĒČõµē½āÖŹ£¬¹ŹA“ķĪó£»
B£®ÄÜŹ¹×ĻÉ«ŹÆČļŹŌŅŗ±äŗģÉ«£¬ĖµĆ÷“×ĖįµēĄė³öĒāĄė×Ó¶ųŹ¹ČÜŅŗ³ŹĖįŠŌ£¬µ«²»ÄÜĖµĆ÷“×Ėį²æ·ÖµēĄė£¬ĖłŅŌ²»ÄÜÖ¤Ć÷“×ĖįŹĒČõµē½āÖŹ£¬¹ŹB“ķĪó£»
C£®Äܱ»Čõ¼ī°±Ė®ÖŠŗĶ£¬ĖµĆ÷“×ĖįŹĒĖį£¬µ«²»ÄÜĖµĆ÷“×Ėį²æ·ÖµēĄė£¬ĖłŅŌ²»ÄÜÖ¤Ć÷“×ĖįŹĒČõµē½āÖŹ£¬¹ŹC“ķĪó£»
D£®³£ĪĀĻĀ£¬0.1 mol•L-1“×ĖįČÜŅŗÖŠµÄc£ØH+£©ĪŖ1.32”Į10-3mol•L-1£¬ĒāĄė×ÓÅØ¶ČŠ”ÓŚ“×ĖįÅØ¶Č£¬ĖµĆ÷“×Ėį²æ·ÖµēĄė£¬ŌņÖ¤Ć÷“×ĖįŹĒČõµē½āÖŹ£¬¹ŹDÕżČ·£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éµē½āÖŹĒæČõÅŠ¶Ļ£¬ĪŖøßĘµæ¼µć£¬Ć÷Č·µē½āÖŹĒæČõøł±¾Ēų±šŹĒ½ā±¾Ģā¹Ų¼ü£¬²»ÄÜøł¾Żµē½āÖŹČܽā¶Č“󊔼°µē½āÖŹČÜŅŗµ¼µēŠŌĒæČõÅŠ¶Ļµē½āÖŹĒæČõ£¬ĪŖŅדķµć£®


 ĒįĖÉæĪĢƵ„ŌŖ²āŹŌAB¾ķĻµĮŠ“š°ø
ĒįĖÉæĪĢƵ„ŌŖ²āŹŌAB¾ķĻµĮŠ“š°ø Š”Ģāæń×öĻµĮŠ“š°ø
Š”Ģāæń×öĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ·“Ó¦ | ·“Ó¦Īļ | Ńõ»Æ²śĪļŗĶ»¹Ō²śĪļ |
| ·“Ó¦¢Ł | Cl2”¢FeI2 | FeCl3”¢FeCl2”¢I2 |
| ·“Ó¦¢Ś | MnO4-”¢Cl- | Cl2”¢Mn2+ |
| A£® | ·“Ó¦¢ŁÖŠCl2Óė FeI2µÄĪļÖŹµÄĮæÖ®±ČĪŖ2£ŗ1 | |
| B£® | ·“Ó¦¢ŁÖŠ·¢ÉśµÄĄė×Ó·½³ĢŹ½æÉÄÜĪŖ£ŗ2Cl2+2Fe2++2I-”śI2+2Fe3++4Cl- | |
| C£® | ·“Ó¦¢ŚÖŠĆæÉś³É1molCl2£¬µē×Ó×ŖŅĘŹżÄæĪŖ10mol | |
| D£® | Ńõ»ÆŠŌÓÉĒæµ½ČõĖ³ŠņĪŖMnO4-£¾Cl2£¾Fe3+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | øĆ¹ż³ĢŹĒ»ÆѧÄÜ×Ŗ»ÆĪŖµēÄܵĹż³Ģ | |
| B£® | Ņ»¶ĪŹ±¼äŗ󣬢Ł³ŲÖŠn£ØKHCO3£©²»±ä | |
| C£® | Ņ»¶ĪŹ±¼äŗ󣬢Ś³ŲÖŠČÜŅŗµÄpHŅ»¶ØŌö“ó | |
| D£® | Ķµē¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗCO2+6H2O+8e-ØTCH4+8 OH- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
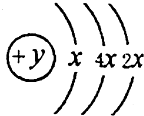 A”¢B”¢C”¢DĖÄÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬Ō×ÓŠņŹżD£¾A£¾B£¾C£¬ĒŅA”¢BĶ¬ÖÜĘŚ£¬C”¢DĶ¬Ö÷×壬AµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼ČēĶ¼£¬B”¢CæÉŠĪ³ÉĄė×Ó»ÆŗĻĪļB2C»ņB2C2£¬¾Ż“ĖĢīæÕ£ŗ
A”¢B”¢C”¢DĖÄÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬Ō×ÓŠņŹżD£¾A£¾B£¾C£¬ĒŅA”¢BĶ¬ÖÜĘŚ£¬C”¢DĶ¬Ö÷×壬AµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼ČēĶ¼£¬B”¢CæÉŠĪ³ÉĄė×Ó»ÆŗĻĪļB2C»ņB2C2£¬¾Ż“ĖĢīæÕ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ŠņŗÅ | ¢Ł | ¢Ś | ¢Ū | ¢Ü | ¢Ż |
| ¼× | CO2 | HCl | CO2 | NO2 | CO2 |
| ŅŅ | SO2 | CO2 | SO2 | SO2 | NH3 |
| ±ū | ŹÆ»ŅĖ® | ŹÆ»ŅĖ® | Ba£ØNO3£©2 | BaCl2 | CaCl2 |
| A£® | ¢Ś¢Ū¢Ü | B£® | ¢Ł¢Ś¢Ū¢Ü | C£® | ¢Ł¢Ū¢Ü | D£® | ¢Ś¢Ū¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.1mol•L-1Ļ”ĮņĖįÖŠŗ¬ÓŠĮņĖįøłøöŹżĪŖ0.1NA | |
| B£® | 7.8g¹żŃõ»ÆÄĘÓė×ćĮæĖ®³ä·Ö·“Ó¦×ŖŅʵē×Ó0.1NA | |
| C£® | 2.4g½šŹōĆ¾Óė×ćĮæµÄŃĪĖį·“Ó¦£¬Éś³ÉĒāĘųµÄĢå»żĪŖ2.24L | |
| D£® | ±ź×¼×“æöĻĀ£¬0.5NAøöĖ®·Ö×ÓĖłÕ¼Ģå»żŹĒ11.2L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŃÖŖŌŚ1”Į105Pa£¬298KĢõ¼žĻĀ£¬2molĒāĘųČ¼ÉÕÉś³ÉĖ®ÕōĘų·Å³ö484kJČČĮ棬ČČ»Æѧ·½³ĢŹ½ŹĒ 2H2£Øg£©+O2£Øg£©ØT2H2O£Øl£©”÷H=-484kJ•mol-1 | |
| B£® | ŗ¬20.0 g NaOHµÄĻ”ČÜŅŗÓėĻ”ŃĪĖįĶźČ«ÖŠŗĶ£¬·Å³ö28.7 kJµÄČČĮ棬ŌņĻ”“×ĖįŗĶĻ”NaOHČÜŅŗ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗNaOH£Øaq£©+CH3COOH£Øaq£©ØTCH3COONa£Øaq£©+H2O£Øl£©”÷H=-57.4 kJ/mol | |
| C£® | 1 g±ūĶé£ØC3H8£©Ķź³ÉČ¼ÉÕÉś³ÉCO2ĘųĢåŗĶŅŗĢ¬Ė®£¬·Å³ö50.405 kJČČĮæC3H8£Øg£©+5O2£Øg£©ØT3CO2£Øg£©+4H2O£Øl£©”÷H=-2 217.82 kJ/mol | |
| D£® | 1 mol SĶźČ«Č¼ÉÕ·ÅČČ297.3 kJ£¬ĘäČČ»Æѧ·½³ĢŹ½ĪŖ£ŗS+O2ØTSO2”÷H=-297.3 kJ/mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NH4+”¢Na+”¢NO3-”¢Cl- | B£® | K+”¢Ba2+”¢Cl-”¢NO3- | ||
| C£® | HCO3-”¢Ca2+”¢Na+”¢NO3- | D£® | Cu2+”¢Cl-”¢K+”¢NO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com