
下列操作中,能使电离平衡H2O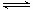 H++OH-向右移动且溶液呈酸性的是
H++OH-向右移动且溶液呈酸性的是
A.向水中加入NaHSO4溶液 B.向水中加入Al2(SO4)3固体
C.向水中加入Na2CO3溶液 D.将水加热到100℃,使pH=6
B
【解析】
试题分析:A NaHSO4=Na++H++SO42-.加入NaHSO4溶液后,C(H+)
增大,水的电离平衡向逆向移动。错误。B.向水中加入Al2(SO4)3固体
,发生反应Al3++3H2O Al(OH)3+3H+
.由于消耗了水电离生成的OH-,使平衡正向移动,产生的OH-又被消耗。当最终达到电离平衡时,C(H+)>C(OH-)。正确。C.向水中加入Na2CO3溶液发生反应:CO32-+H2O
Al(OH)3+3H+
.由于消耗了水电离生成的OH-,使平衡正向移动,产生的OH-又被消耗。当最终达到电离平衡时,C(H+)>C(OH-)。正确。C.向水中加入Na2CO3溶液发生反应:CO32-+H2O HCO3-+OH-。.由于消耗了水电离生成的H+,使平衡正向移动,产生的H+-又被消耗。当最终达到电离平衡时,C(OH-)
> C(H+)。错误。
HCO3-+OH-。.由于消耗了水电离生成的H+,使平衡正向移动,产生的H+-又被消耗。当最终达到电离平衡时,C(OH-)
> C(H+)。错误。
考点:考查外界条件对水的电离平衡的影响的知识。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014届福建省高二第二次月考化学试卷(解析版) 题型:选择题
下列操作中,能使电离平衡H2O H++OH-,向右移动且溶液呈碱性的是( )
H++OH-,向右移动且溶液呈碱性的是( )
A. 向水中加入NaHSO4溶液 B. 向水中加入少量金属钠
C. 向水中加入NaOH溶液 D. 将水加热到100℃,使pH=6
查看答案和解析>>
科目:高中化学 来源:2011-2012年湖南省高二上学期期中考试化学试卷 题型:选择题
下列操作中,能使电离平衡H2O H++OH-,向右移动且溶液呈酸性的是( )
H++OH-,向右移动且溶液呈酸性的是( )
A.向水中加入NaHSO4溶液 B.向水中加入Al2(SO4)3固体
C.向水中加入Na2CO3溶液 D.将水加热到100℃,使pH=6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com