
| A. | 一定条件下,增加反应物的量,必定加快反应速率 | |
| B. | 升高温度正反应速率增大,则逆反应速率也一定增大 | |
| C. | 可逆反应的特征是正反应速率总是和逆反应速率相等 | |
| D. | 使用催化剂一定会加快反应速率 |
分析 A.一定条件下,如果反应物是固体或纯液体,固体或纯液体反应物量的多少不影响反应速率;
B.升高温度,正逆反应速率都增大;
C.逆反应的特征是正反应和逆反应都在同时发生,同时进行;
D.一般情况下,催化剂可加快反应速率,但此题要考虑负催化剂的作用.
解答 解:A.一定条件下,如果反应物是固体或纯液体,固体或纯液体反应物量的多少不影响反应速率,所以增大反应物的量不一定加快反应速率,故A错误;
B.升高温度,增大活化分子百分数,所以正逆反应速率都增大,故B正确;
C.逆反应的特征是正反应和逆反应都在同时发生,同时进行,化学平衡状态的特征之一是正反应速率和逆反应速率相等的状态,故C错误;
D.催化剂可加快反应速率,也可减缓反应速率,如负催化剂可减缓反应速率,故D错误;
故选B.
点评 本题考查化学反应速率影响因素,为高频考点,明确浓度、温度、催化剂等因素对化学反应速率影响原理是解本题关键,注意这些影响因素适用范围,易错选项是D.


科目:高中化学 来源: 题型:选择题
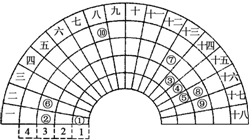 元素周期表的形式多种多样,下图是扇形元素周期表前四周期的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )
元素周期表的形式多种多样,下图是扇形元素周期表前四周期的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )| A. | ②、⑧、⑨对应原子半径依次增大 | |
| B. | ②、⑨的氢化物晶体类型相同 | |
| C. | 元素⑩处于常见周期表第四周期第VIIIB族 | |
| D. | ①、③、④、⑤形成的某种化合物中既含有共价键又含有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12 | B. | 13 | C. | 16 | D. | 19 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g);△H=-1367.0 kJ/mol(燃烧热) | |
| B. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=+57.3 kJ/mol(中和热) | |
| C. | S(s)+O2(g)═SO2(g);△H=-296.8 kJ/mol(反应热) | |
| D. | 2NO2═O2+2NO;△H=116.2 kJ/mol(反应热) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第ⅠA族的元素都是碱金属元素 | |
| B. | 稀有气体元素原子的最外层电子数均为8 | |
| C. | 原子序数为16的元素位于元素周期表的第3周期VIA族 | |
| D. | 第二周期ⅣA族元素的原子核电荷数和中子数一定为6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2(g)+O2(g)=2H2O(l)△H1; 2H2(g)+O2(g)=2H2O(g)△H2 | |
| B. | S(g)+O2(g)=SO2(g)△H1; S(s)+O2(g)=SO2(g)△H2 | |
| C. | C(s)+$\frac{1}{2}$O2(g)=CO(g)△H1; C(s)+O2(g)=CO2(g)△H2 | |
| D. | H2(g)+Cl2(g)=2HCl(g)△H1; $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)=HCl(g)△H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com