
| A. | 质量数为198 | B. | 中子数为140 | C. | 质子数为82 | D. | 核外电子数为58 |
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
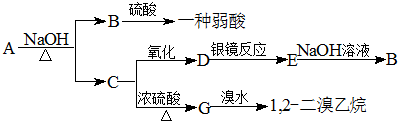
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
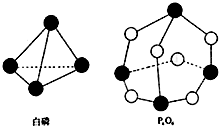 化学反应的本质是旧健的断裂和新键的形成过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ•mol-1)P-P:198 P-O:360 O=O:498,则反应P4(白磷)+3O2→P4O6的能量变化为( )
化学反应的本质是旧健的断裂和新键的形成过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ•mol-1)P-P:198 P-O:360 O=O:498,则反应P4(白磷)+3O2→P4O6的能量变化为( )| A. | 吸收126kJ的能量 | B. | 释放126kJ的能量 | ||
| C. | 吸收1638kJ的能量 | D. | 释放1638kJ的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | ||
| Z | W |
| A. | 钠与Y只能形成Na2Y | |
| B. | Z形成的单质易溶于由X与Z形成的化合物 | |
| C. | Z得电子能力比W强 | |
| D. | X有多种同素异形体,而Y不存在同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷、一氯甲烷、二氯甲烷等均属于烷烃 | |
| B. | 乙醇不与任何酸反应 | |
| C. | 乙酸不能与金属Na反应 | |
| D. | 乙酸乙酯能发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
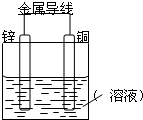 将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如图所示装置.试回答下列问题:
将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如图所示装置.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | ①能使溴的四氯化碳溶液褪色; ②能与水在一定条件下反应生成C ③比例模型为: 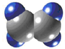 |
| B | ①由C、H两种元素组成; ②球棍模型为: 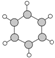 |
| C | ①由C、H、O三种元素组成; ②能与Na反应,但不能与NaOH溶液反应; ③能与E反应生成相对分子质量为100的酯. |
| D | ①相对分子质量比C少2; ②能由C氧化而成; |
| E | ①由C、H、O三种元素组成; ②球棍模型为:  |
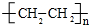 .
.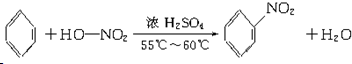 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com