
| A.乙醇 | B.丙醇 | C.丁醇 | D.甲醇 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
| A.钠块沉在乙醇液面的下面 | B.钠块熔化成小球 |
| C.钠块在乙醇的液面上游动 | D.乙醇溶液变红 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
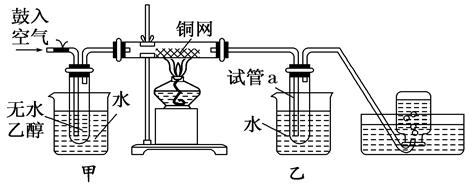
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
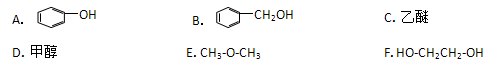
| A.乙醇不能和酸性高锰酸钾溶液发生氧化还原反应 |
| B.交警用橙色的酸性重铬酸钾溶液检查司机是否酒后驾车 |
| C.黄酒中某些微生物使乙醇氧化为乙酸,于是酒就变酸了 |
| D.陈年的酒很香是因为乙醇和乙醇被氧化生成的乙酸发生酯化反应生成了乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③ | B.①②④ | C.①③④ | D.②③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
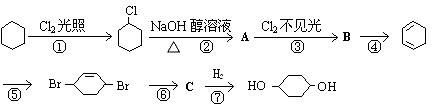
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com