
某混合金属粉末,除Mg外还含有Al、Zn中的一种或两种,含量都在10%以上。某研究小组设计实验探究该混合金属粉末中铝、锌元素的存在。
所用试剂:样品、pH试纸、稀H2SO4、NaOH溶液、稀NH3·H2O。
该小组探究过程如下:
●查阅资料:
|
①镁、铝、锌都是银白色的金属 ②锌(Zn)可以与NaOH溶液反应生成H2 ③Zn(OH)2为白色固体,难溶于水,可溶于强碱及NH3·H2O ④Zn2+易形成络合物如[Zn(NH3)4]2+,该络合物遇强酸分解生成Zn2+、NH4+ |
●提出假设:
(1)假设①:该混合金属粉末中除镁外还含有铝元素;
假设②:该混合金属粉末中除镁外还含有锌元素;
假设③: 。
●实验探究:
甲同学基于假设③设计实验方案如下:

乙同学同样基于假设3设计另一实验方案如下:

(2)试剂M是________________;沉淀B是 。
(3)丙同学认为乙同学的方案比甲同学的好,理由是 。
(4)丁同学研究了甲、乙两同学的方案后,在其中一种方案的基础上用最简便方法测定了Wg样品中金属镁(Mg)的质量,他的方法是 。
(5)操作Ⅰ的主要过程是:在滤液中逐滴加入 ,直至生成的沉淀刚好溶解,再加入足量的 。
(6)某溶液中含有Zn2+、Al3+、NH4+和SO42-等离子,向其中逐滴加入NaOH溶液,则生成沉淀的物质的量与加入NaOH溶液体积关系的图像正确的是__________。
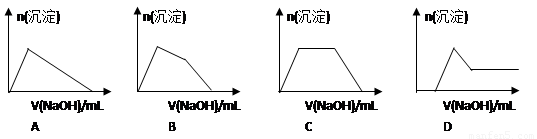
(1)该混合金属粉末中除镁外还含有铝、锌元素 (2)NaOH溶液;Al(OH)3
(3)步骤简单,节约试剂;(4)将沉淀C洗涤、小心干燥后称量;(5)稀硫酸;稀氨水;(6)B
【解析】
试题分析:(1)由于混合金属粉末,除Mg外还含有Al、Zn中的一种或两种,实验根据假设①②可知,假设③应该是该混合金属粉末中除镁外还含有铝、锌元素。
(2)样品与稀硫酸反应生成相应的硫酸盐。由于氢氧化锌、氢氧化铝均能和氢氧化钠溶液反应,所以首先加入过量的氢氧化钠溶液得到氢氧化镁沉淀,而锌离子和铝离子分别是生成相应的偏铝酸盐,即M是氢氧化钠溶液,沉淀A是氢氧化镁。由于Zn(OH)2为白色固体,难溶于水,可溶于强碱及NH3·H2O,但氢氧化铝不能溶于氨水中,所以可以向滤液中先加入酸将偏铝酸盐转化为锌离子和铝离子,然后加入过量的氨水得到氢氧化铝白色沉淀,而锌离子转化为[Zn(NH3)4]2+,所以沉淀B是氢氧化铝。由于Zn2+易形成络合物如[Zn(NH3)4]2+,该络合物遇强酸分解生成Zn2+、NH4+,所以向滤液中加入稀硫酸即可生成Zn2+、NH4+,最后加入适量的氢氧化钠溶液生成氢氧化锌沉淀。
(3)由于锌(Zn)、铝均可以与NaOH溶液反应生成H2,所以在乙方案中首先加入过量的氢氧化钠溶液,将锌和铝溶解,而镁不溶解,即沉淀C是镁。而后续的操作与甲方案是相同的,所以乙同学的方案比甲同学的好,理由是步骤简单,节约试剂。
(4)由于在乙方案中沉淀C就是镁,所以只需要将沉淀C洗涤、小心干燥后称量即可得出镁的含量。
(5)根据以上分析可知,操作Ⅰ的主要过程是:在滤液中逐滴加入稀硫酸,直至生成的沉淀刚好溶解,最后再加入足量的氨水即可生成氢氧化铝白色沉淀。
(6)某溶液中含有Zn2+、Al3+、NH4+和SO42-等离子,向其中逐滴加入NaOH溶液,则首先生成氢氧化锌、氢氧化铝沉淀。由于氢氧化锌能溶解在氨水中,所以加入的氢氧化钠首先溶解氢氧化锌,然后氢氧化钠再与溶液中的NH4+反应,最后加入的氢氧化钠再和氢氧化铝反应而使其溶解,因此生成沉淀的物质的量与加入NaOH溶液体积关系的图像正确的是B。
考点:考查实验方案设计与评价;物质的分离与提纯;以及沉淀生成与溶解的图像分析与判断


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
| ①镁、铝、锌都是银白色的金属 ②锌(Zn)可以与NaOH溶液反应生成H2 ③Zn(OH)2为白色固体,难溶于水,可溶于强碱及NH3?H2O ④Zn2+易形成络合物如[Zn(NH3)4]2+,该络合物遇强酸分解生成Zn2+、NH4+●提出假设: (1)假设①:该混合金属粉末中除镁外还含有 Al Al 元素假设②:该混合金属粉末中除镁外还含有 Zn Zn 元素假设③:该混合金属粉末中除镁外还含有铝、锌元素 ●实验探究: 甲同学基于假设③设计实验方案如下:乙同学同样基于假设③设计另一实验方案如下: 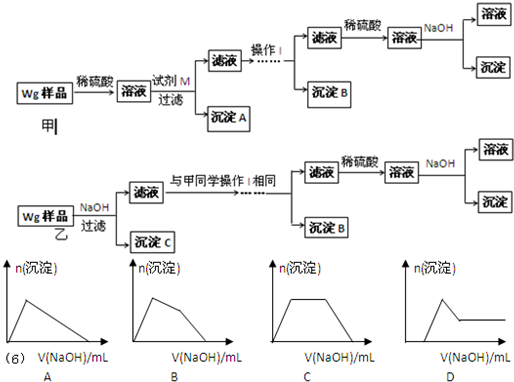 (2)试剂M是 NaOH溶液 NaOH溶液 ;沉淀B是Al(OH)3 Al(OH)3 .(3)丙同学认为乙同学的方案比甲同学的好,理由是 步骤简单,节约试剂 步骤简单,节约试剂 .(4)丁同学研究了甲、乙两同学的方案后,在其中一种方案的基础上用最简便方法测定了Wg样品中金属镁(Mg)的质量,他的方法是 将沉淀C洗涤、小心干燥后称量 将沉淀C洗涤、小心干燥后称量 .(5)操作Ⅰ的主要过程是:在滤液中逐滴加入 稀硫酸 稀硫酸 ,直至生成的沉淀刚好溶解,再加入足量的稀氨水 稀氨水 .(6)某溶液中含有Zn2+、Al3+、NH4+和SO42-等离子,向其中逐滴加入NaOH溶液,则生成沉淀的物质的量与加入NaOH溶液体积关系的图象正确的是 B B .
查看答案和解析>> 科目:高中化学 来源: 题型: 某混合金属粉末,除Mg外,还含有Al、Zn中的一种或两种,含量都在 10%以上。某研究小组设计实验探究该混合金属粉末中铝、锌元素的存在。 所用试剂:样品、pH试纸、稀H2SO4、NaOH溶液、稀NH3·H2O。 该小组探究过程如下: ● 查阅资料:
● 提出假设: (1)假设①:该混合金属粉末中除镁外还含有________元素 假设②:该混合金属粉末中除镁外还含有________元素 假设③:该混合金属粉末中除镁外还含有铝、锌元素 ● 实验探究: 甲同学基于假设③设计实验方案如下: 乙同学同样基于假设3设计另一实验方案如下: (2)试剂M是________________;沉淀B是 。 (3)丙同学认为乙同学的方案比甲同学的好,理由是 。 (4)丁同学研究了甲、乙两同学的方案后,在其中一种方案的基础上用最简便方法测定了Wg样品中金属镁(Mg)的质量,他的方法是 。 (5)操作Ⅰ的主要过程是:在滤液中逐滴加入 ,直至生成的沉淀刚好溶解,再加入足量的 。 (6)某溶液中含有Zn2+、Al3+、NH4+和SO42-等离子,向其中逐滴加入NaOH溶液, 则生成沉淀的物质的量与加入NaOH溶液体积关系的图像正确的是__________。
查看答案和解析>> 科目:高中化学 来源:2012届上海市闵行区高三上学期期末质量抽测化学试卷 题型:填空题 某混合金属粉末,除Mg外,还含有Al、Zn中的一种或两种,含量都在10%以上。某研究小组设计实验探究该混合金属粉末中铝、锌元素的存在。所用试剂:样品、pH试纸、稀H2SO4、NaOH溶液、稀NH3·H2O。
查看答案和解析>> 科目:高中化学 来源:2013-2014学年黑龙江省高三上学期第三次验收考试化学试卷(解析版) 题型:实验题 某混合金属粉末,除Fe外,还含有Al、Zn中的一种或两种,含量都在10%以上。某研究小组设计实验探究该混合金属粉末中铝、锌元素的存在,探究过程如下: 【查阅资料】①Zn可以与NaOH溶液反应生成H2 ②Zn(OH)2为白色固体,难溶于水,可溶于强碱及NH3·H2O ③Zn2+易形成络合物如[Zn(NH3)4]2+,该络合物遇强酸生成Zn2+、NH4+ 【提出假设】假设①:该混合金属粉末中除Fe外还含有Al元素 假设②:该混合金属粉末中除Fe外还含有Zn元素 假设③:该混合金属粉末中除Fe外还含有Al、Zn元素 【实验探究】所用试剂:样品、pH试纸、稀H2SO4、NaOH溶液、稀NH3·H2O。 甲同学基于假设③设计实验方案如下:
乙同学同样基于假设③设计另一实验方案如下:
(1)Fe元素在周期表中的位置是第 周期 族。 (2)试剂M是 ;沉淀B是 。 (3)你认为甲、乙同学的方案 (填“甲”或“乙”)比较好,理由是 。 (4)操作Ⅰ的主要过程是:在滤液中逐滴加入 ,直至生成的沉淀刚好溶解,再加入足量的 。 (5)乙同学将沉淀C洗涤、烘干、冷却后称重,质量为m1g,经计算即可得到样品中铁的质量分数,你认为 (填“是”或“否”)准确,原因是 。 (6)电解法制金属铝的化学方程式是 。 以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是 。
查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |