
下列反应属于取代反应的组合是
①CH3CH=CH2+Br2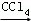 CH3CHBrCH2Br
CH3CHBrCH2Br
②CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
③2CH3CH2OH+O2 2CH3CHO+2H2O
2CH3CHO+2H2O
④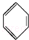 +Br2
+Br2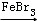
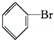 +HBr.
+HBr.
A.①② B.③④ C.①③ D.②④
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案科目:高中化学 来源:2015-2016学年黑龙江大庆铁人中学高二上9月考化学试卷(解析版) 题型:选择题
现有下列热化学方程式:
①C(s)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol-1
②2CO(g)+O2(g)===2CO2(g) ΔH2=-566 kJ·mol-1
③CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH3=-890 kJ·mol-1
④CH3CH2OH(l)+3O2(g)===2CO2(g)+3H2O(l) ΔH4=-1 367 kJ·mol-1
下列说法正确的是________。
A.CO(g)的燃烧热比C(s)的燃烧热大
B.ΔH4>ΔH3>ΔH2>ΔH1
C.CO(g)具有的能量比CO2(g)高
D.1 mol C2H5OH蒸气完全燃烧生成CO2和液态水,放出大于1 367 kJ的热量
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省佛山市高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列离子在指定条件下能大量共存的是
A.在酸性溶液中:Ba2+、K+、SO42―、Cl―
B.含有大量Al3+的溶液中:K+、Na+、NH4+、SO42―
C.使甲基橙变黄的溶液中:Na+、I―、CO32―、OH―
D.无色溶液中:K+、Cl―、Cr2O72-、HCO3―
查看答案和解析>>
科目:高中化学 来源:2016届山东省滕州市高三第一学期开学初检测化学试卷(解析版) 题型:填空题
煤化工中两个重要反应为①C(s)+H2O(g)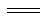 H2(g)+CO(g)ΔH=+131.3 kJ·mol-1,②CO(g)+ H2O(g)
H2(g)+CO(g)ΔH=+131.3 kJ·mol-1,②CO(g)+ H2O(g) CO2(g)+ H2(g)。
CO2(g)+ H2(g)。
(1)下列说法正确的是 。
A.当反应①的容器中混合气体的密度不再变化时反应达到最大限度
B.反应②的熵变△S>0
C.反应①中增加C固体的量能增大反应速率
D.在反应中②及时分离出产生的H2对正反应速率无影响
(2)若工业上要增加反应①的速率,最经济的措施为 。
(3)现将不同量的CO(g)和H2O(g)分别通入2L恒容密闭容器中进行反应,得到如下三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/ min | ||
CO | H2O | H2 | CO2 | |||
I | 650 | 4 | 2 | 1.6 | 1.6 | 5 |
Ⅱ | 900 | 2 | 1 | 0.5 | 0.5 | 3 |
Ⅲ | 900 | a | b | c | d | t |
①实验I中,从反应开始到反应达到平衡时,H2O的平均反应速率为___。
②CO(g)和H2O(g)反应的△H 0(填“大于”、“小于”或“等于”)
③实验III中,若平衡时,CO的转化率大于水蒸气,则a、b必须满足的关系是______,与实验Ⅱ相比,化学平衡常数 (填“增大”、“减小”或“不变”)。
④若在900℃时,实验II反应达到平衡后,向此容器中再加入1 mol CO、0.5 mol H2O、0.2 mol CO2、0.5 mol H2,平衡向__________方向移动(填“正反应”、“逆反应”“不移动”)。
(4)CO、H2可用于甲醇和甲醚,其反应为(m、n均大于0):
反应①:CO(g)+2H2(g) CH3OH(g)ΔH= -mkJ·mol-1
CH3OH(g)ΔH= -mkJ·mol-1
反应②: 2CO(g)+4 H2(g) CH3OCH3(g)+H2O(g)ΔH=-nkJ·mol-1
CH3OCH3(g)+H2O(g)ΔH=-nkJ·mol-1
反应③:2CH3OH(g) CH3OCH3(g)+ H2O(g)△H<0
CH3OCH3(g)+ H2O(g)△H<0
则m与n的关系为 。
查看答案和解析>>
科目:高中化学 来源:2016届贵州省贵阳市高三8月摸底考试化学试卷(解析版) 题型:选择题
下列关于①苯②乙醇③乙酸④葡萄糖等有机物的叙述中,不正确的是
A、可用新制的氢氧化铜鉴别③与④ B.只有③能与金属钠反应
C、①、②、③均能发生取代反应 D.一定条件下,④可以转化为②
查看答案和解析>>
科目:高中化学 来源:2016届安徽省等六校教研会高三第一次联考化学试卷(解析版) 题型:选择题
茉莉香醇是一种具有甜香味的物质,是合成香料的重要原料,其结构简式如下,下列有关茉莉香醇的叙述正确的是
A、茉莉香醇的分子式为C9H14O2
B、不能使溴的四氯化碳溶液褪色
C、能与FeCl3溶液发生显色反应
D、能发生加成反应而不能发生取代反应
查看答案和解析>>
科目:高中化学 来源:2016届四川省高三秋季零诊考试化学试卷(解析版) 题型:填空题
(15分)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A原子核外有三个未成对电子;元素B的氢化物能用于刻蚀玻璃; C元素是地壳中含量最高的金属元素;D原子核外的M层中有两对成对电子;E原子核外最外层只有1个电子,其余各层电子均充满。请根据以上信息,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)E的核外电子排布式是___________,A、B、C、D的第一电离能由小到大的顺序为__________。
(2)化合物CA的熔点远高于C的氯化物的熔点,理由是______________;
(3)A的最高价含氧酸根离子中,其中心原子采取_____杂化,D的低价氧化物分子的空间构型是_______。
(4)B2与NaOH溶液反应的产物之一是OB2,该反应的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源:2016届贵州省高三第一次模拟化学试卷(解析版) 题型:实验题
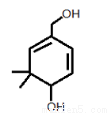
(14分)某化学小组用下列装置制取收集纯净的氯气,并研究其性质。请回答下列问题。
(1)装置甲中仪器A的名称是________,丙中应装的溶液是 ,甲装置中发生反应的离子方程
式为 。制取收集纯净氯气的装置接口连接顺序是a→ …→g(补充完整) 。
(2)制备反应会因盐酸浓度下降而停止,为测定反应残余液中盐酸的浓度,探究小组同学提出下列实验方案:
I方案:与足量AgNO3溶液反应,称量生成的AgCl质量。
Ⅱ方案:采用酸碱中和滴定法测定。
Ⅲ方案:与已知量CaCO3(过量)反应,称量剩余的CaCO3质量。
继而进行下列判断和实验:
①判定I方案不可行,理由是__________________;
②进行Ⅱ方案实验:准确量取残余清液稀释一定倍数后作为试样。
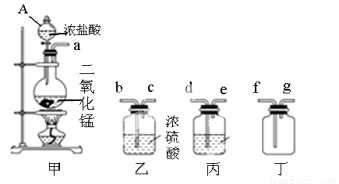
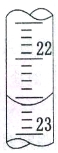
a.量取试样20.00mL于锥形瓶中,若锥形瓶中存有少量水,对实验结果是否有影响? (填“是”或“无”)。用0.10 mol•L-1 NaOH标准溶液滴定,消耗NaOH标准溶液的体积如右图所示 ,其读数为 mL.
b.平行滴定后获得实验结果
③判断Ⅲ方案的实验结果_______(填“偏大”、“偏小”或“准确”)。[已知:Ksp(CaCO3 )=2.8×10-9、Ksp(MnCO3)=2.3×10-11
(3)某同学认为上述方案缺少尾气吸收装置,请在下面的方框中画出该装置并注明试剂。

查看答案和解析>>
科目:高中化学 来源:2016届山东省枣庄市高三9月阶段性学情检测化学试卷(解析版) 题型:选择题
下列各组离子中,因发生氧化还原反应而不能大量共存的是
A.K+、H+、I﹣、MnO4﹣ B.Fe3+、Fe2+、SO42﹣、NO3﹣
C.Al3+、Na+、SO42﹣、CO32﹣ D.Fe3+、H+、SO42﹣、ClO﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com