
 £®C2A4µÄĖ®ČÜŅŗ³Ź¼ī£ØĢī”°Ėį”±”°¼ī”±»ņ”°ÖŠ”±£©ŠŌ£¬1mol C2A4×ī¶ąæÉŅŌÓė2mol HCl»ņNaOH·¢ÉśÖŠŗĶ·“Ӧɜ³ÉÕżŃĪ£®C2A4 ŗĶA2D2 ¼Č¾ßÓŠŃõ»ÆŠŌ£¬ÓÖ¾ßÓŠ»¹ŌŠŌ£¬“Ó»ÆŗĻ¼ŪµÄ½Ē¶Č½āŹĶC2A4 ŗĶA2D2 ¼Č¾ßÓŠŃõ»ÆŠŌÓÖ¾ßÓŠ»¹ŌŠŌµÄŌŅņN2H4ÖŠNĻŌ-2£¬H2O2ÖŠOĻŌ-1£¬¾łĪŖĻąÓ¦ŌŖĖŲµÄÖŠ¼ä¼ŪĢ¬£¬ĖłŅŌ¼ČÓŠŃõ»ÆŠŌ£¬ÓÖÓŠ»¹ŌŠŌ
£®C2A4µÄĖ®ČÜŅŗ³Ź¼ī£ØĢī”°Ėį”±”°¼ī”±»ņ”°ÖŠ”±£©ŠŌ£¬1mol C2A4×ī¶ąæÉŅŌÓė2mol HCl»ņNaOH·¢ÉśÖŠŗĶ·“Ӧɜ³ÉÕżŃĪ£®C2A4 ŗĶA2D2 ¼Č¾ßÓŠŃõ»ÆŠŌ£¬ÓÖ¾ßÓŠ»¹ŌŠŌ£¬“Ó»ÆŗĻ¼ŪµÄ½Ē¶Č½āŹĶC2A4 ŗĶA2D2 ¼Č¾ßÓŠŃõ»ÆŠŌÓÖ¾ßÓŠ»¹ŌŠŌµÄŌŅņN2H4ÖŠNĻŌ-2£¬H2O2ÖŠOĻŌ-1£¬¾łĪŖĻąÓ¦ŌŖĖŲµÄÖŠ¼ä¼ŪĢ¬£¬ĖłŅŌ¼ČÓŠŃõ»ÆŠŌ£¬ÓÖÓŠ»¹ŌŠŌ £¬øĆ»ÆŗĻĪļÓėCA3ŗĶA2DµÄČŪµćÓÉøßµ½µĶµÄĖ³ŠņĪŖH2O£¾NH3£¾CH4£ØÓĆ»ÆѧŹ½±ķŹ¾£©£®
£¬øĆ»ÆŗĻĪļÓėCA3ŗĶA2DµÄČŪµćÓÉøßµ½µĶµÄĖ³ŠņĪŖH2O£¾NH3£¾CH4£ØÓĆ»ÆѧŹ½±ķŹ¾£©£® £®CA3”¢A2D”¢EA3µÄČČĪČ¶ØŠŌÓÉĒæµ½ČõµÄĖ³ŠņĪŖH2O£¾NH3£¾PH3£ØÓĆ»ÆѧŹ½±ķŹ¾£©£®
£®CA3”¢A2D”¢EA3µÄČČĪČ¶ØŠŌÓÉĒæµ½ČõµÄĖ³ŠņĪŖH2O£¾NH3£¾PH3£ØÓĆ»ÆѧŹ½±ķŹ¾£©£® ·ÖĪö AŹĒÖÜĘŚ±ķÖŠŌ×Ó°ė¾¶×īŠ”µÄŌŖĖŲ£¬BŹĒŠĪ³É»ÆŗĻĪļÖÖĄą×ī¶ąµÄŌŖĖŲ£¬ŌņBĪŖC£¬AĪŖH£»a+b=c£¬c=1+6=7£¬¼“CĪŖN£»a+c=d£¬d=1+7=8£¬¼“DĪŖO£»c+d=e£¬e=7+8=15£¬¼“EĪŖP£¬ÓÉ“Ė·ÖĪö½ā“š£®
½ā“š ½ā£ŗ£Ø1£©N2H4µÄµē×ÓŹ½ĪŖ £»N2H4ÖŠµŖÓėĖ®µēĄė³öµÄĒāĄė×ÓŠĪ³ÉÅäĪ»¼ü£¬µ¼ÖĀĖ®ČÜŅŗÖŠĒāŃõøłĄė×Ó“óÓŚĒāĄė×ÓµÄÅØ¶Č£¬ŌņĖ®ČÜŅŗĻŌ¼īŠŌ£¬1molN2H4ÖŠµÄ2molNŌ×ÓÉĻµÄ¹Āµē×Ó¶ŌÄÜÓėH+½įŗĻ£¬Ōņ1molN2H4Óė2molHCl·“Ӧɜ³ÉÕżŃĪ£¬ÓÉ»ÆŗĻ¼ŪæÉÖŖ£¬N2H4ÖŠNĻŌ-2£¬H2O2ÖŠOĻŌ-1£¬¾łĪŖĻąÓ¦ŌŖĖŲµÄÖŠ¼ä¼ŪĢ¬£¬ĖłŅŌ¼ČÓŠŃõ»ÆŠŌ£¬ÓÖÓŠ»¹ŌŠŌ£¬
£»N2H4ÖŠµŖÓėĖ®µēĄė³öµÄĒāĄė×ÓŠĪ³ÉÅäĪ»¼ü£¬µ¼ÖĀĖ®ČÜŅŗÖŠĒāŃõøłĄė×Ó“óÓŚĒāĄė×ÓµÄÅØ¶Č£¬ŌņĖ®ČÜŅŗĻŌ¼īŠŌ£¬1molN2H4ÖŠµÄ2molNŌ×ÓÉĻµÄ¹Āµē×Ó¶ŌÄÜÓėH+½įŗĻ£¬Ōņ1molN2H4Óė2molHCl·“Ӧɜ³ÉÕżŃĪ£¬ÓÉ»ÆŗĻ¼ŪæÉÖŖ£¬N2H4ÖŠNĻŌ-2£¬H2O2ÖŠOĻŌ-1£¬¾łĪŖĻąÓ¦ŌŖĖŲµÄÖŠ¼ä¼ŪĢ¬£¬ĖłŅŌ¼ČÓŠŃõ»ÆŠŌ£¬ÓÖÓŠ»¹ŌŠŌ£¬
¹Ź“š°øĪŖ£ŗ £»¼ī£»2£»N2H4ÖŠNĻŌ-2£¬H2O2ÖŠOĻŌ-1£¬¾łĪŖĻąÓ¦ŌŖĖŲµÄÖŠ¼ä¼ŪĢ¬£¬ĖłŅŌ¼ČÓŠŃõ»ÆŠŌ£¬ÓÖÓŠ»¹ŌŠŌ£»
£»¼ī£»2£»N2H4ÖŠNĻŌ-2£¬H2O2ÖŠOĻŌ-1£¬¾łĪŖĻąÓ¦ŌŖĖŲµÄÖŠ¼ä¼ŪĢ¬£¬ĖłŅŌ¼ČÓŠŃõ»ÆŠŌ£¬ÓÖÓŠ»¹ŌŠŌ£»
£Ø2£©AŗĶBŠĪ³ÉµÄ×ī¼ņµ„»ÆŗĻĪļĪŖ¼×Ķ飬ĘäŠĪ³É¹ż³ĢĪŖ £¬ĘųĢ¬Ēā»ÆĪļµÄĻą¶Ō·Ö×ÓÖŹĮæŌ½“󣬷ŠµćŌ½øߣ¬Ė®”¢°±Ęų·Ö×ÓÖ®¼äŗ¬ÓŠĒā¼ü£¬ČŪ·Šµćøüøߣ¬ŌņČŪµćÓÉøßµ½µĶµÄĖ³ŠņĪŖH2O£¾NH3£¾CH4£¬¹Ź“š°øĪŖ£ŗ
£¬ĘųĢ¬Ēā»ÆĪļµÄĻą¶Ō·Ö×ÓÖŹĮæŌ½“󣬷ŠµćŌ½øߣ¬Ė®”¢°±Ęų·Ö×ÓÖ®¼äŗ¬ÓŠĒā¼ü£¬ČŪ·Šµćøüøߣ¬ŌņČŪµćÓÉøßµ½µĶµÄĖ³ŠņĪŖH2O£¾NH3£¾CH4£¬¹Ź“š°øĪŖ£ŗ £»H2O£¾NH3£¾CH4£»
£»H2O£¾NH3£¾CH4£»
£Ø3£©A”¢B”¢D×é³ÉµÄŅ»ÖÖČÕ³£Éś»īÖŠ×ī³£¼ūµÄÓŠ»śĪļĪŖŅŅ“¼£¬ŅŅ“¼ÓėŃõĘų·“Ó¦Ź±Ģ¼ŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøߣ¬±»Ńõ»Æ·¢ÉśŃõ»Æ·“Ó¦£¬Ōµē³ŲµÄøŗ¼«·“Ó¦ĪŖŃõ»Æ·“Ó¦£¬¼īŠŌĢõ¼žĻĀ£¬ĒāŃõøłĄė×Ó²ĪÓėøŗ¼«·“Ó¦£¬Ōņøŗ¼«·“Ó¦Ź½ĪŖCH3CH2OH-12e-+16OH-ØT2CO32-+11H2O£¬¹Ź“š°øĪŖ£ŗCH3CH2OH-12e-+16OH-ØT2CO32-+11H2O£»
£Ø4£©EµÄĶ¬ĖŲŅģŠĪĢåÖŠÓŠŅ»ÖÖĶس£ĒéæöĻĀ²»ĪČ¶Ø£¬ŌŚæÕĘųÖŠ¼«Ņ××ŌČ¼£¬EĪŖ°×Į×£¬Ęä½į¹¹Ź½ĪŖ £¬·Ē½šŹōŠŌO£¾N£¾P£¬ŌņĪČ¶ØŠŌÓÉĒæµ½ČõµÄĖ³ŠņĪŖH2O£¾NH3£¾PH3£¬
£¬·Ē½šŹōŠŌO£¾N£¾P£¬ŌņĪČ¶ØŠŌÓÉĒæµ½ČõµÄĖ³ŠņĪŖH2O£¾NH3£¾PH3£¬
¹Ź“š°øĪŖ£ŗ £»H2O£¾NH3£¾PH3£®
£»H2O£¾NH3£¾PH3£®
µćĘĄ ±¾Ģāæ¼²éĪ»ÖĆ”¢½į¹¹”¢ŠŌÖŹµÄÓ¦ÓĆ£¬Ć÷Č·Ģ¼”¢ĒāµÄ»ÆŗĻĪļÖÖĄą¶ąŹ±½ā“š±¾ĢāµÄ¹Ų¼ü£¬ŹģĻ¤ŌŖĖŲµÄ³£¼ūµÄĶ¬ĖŲŅģŠĪĢåµČĶĘ³öBĪŖĢ¼ŹĒĶ»ĘĘæŚ£¬æ¼²éÖŖŹ¶µć½Ļ¶ą£¬ÄѶȏŹÖŠ£®


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | SO3+H2OØTH2SO4 | B£® | 2Na2O2+2H2OØT4NaOH+O2”ü | ||
| C£® | 2H2O$\frac{\underline{\;µē½ā\;}}{\;}$2H2”ü+O2”ü | D£® | 3NO2+H2OØT2HNO3+NO |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 100mL1mol/LµÄNa2CO3ČÜŅŗÖŠŗ¬ÓŠ6.02”Į1022øöCO32- | |
| B£® | ×ćĮæĢś·ŪŌŚ0.05molC12ÖŠ³ä·ÖČ¼ÉÕ£¬·“Ó¦Ź±×ŖŅĘ6.02x1022øöµē×Ó | |
| C£® | ½«4gNaOHČÜÓŚ100gÕōĮóĖ®£¬ĖłµĆČÜŅŗĪļÖŹµÄĮæÅØ¶ČŹĒ1mol/L | |
| D£® | ³£ĪĀĻĀ£¬½«9gĀĮʬĶ¶Čė500mL18.4mol•L-1µÄĮņĖįÖŠ£¬²śÉśH2±Č11.2L¶ą |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
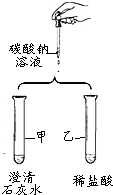 ČēĶ¼ŹĒijŠ”×éŃéÖ¤Ģ¼ĖįÄĘŠŌÖŹµÄŹµŃé·½°ø£®
ČēĶ¼ŹĒijŠ”×éŃéÖ¤Ģ¼ĖįÄĘŠŌÖŹµÄŹµŃé·½°ø£®| ŹµŃé²½Öč | ŹµŃéĻÖĻó | ½įĀŪ |
| ȔɣĮæµÄ·ĻŅŗÓŚŹŌ¹ÜÖŠ£¬µĪ¼Ó2”«3µĪŹÆČļŹŌŅŗ£¬Õńµ“£® | ĪŽĻÖĻó | ·ĻŅŗµÄpH=7£» ²ĀĻė¢ń³ÉĮ¢£® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaCl”¢HCl”¢H2O”¢NaOH | B£® | Cl2”¢Na2S”¢HCl”¢CO2 | ||
| C£® | HBr”¢CCl4”¢H2O”¢CO2 | D£® | Na2O2”¢H2O2”¢H2O”¢O2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĪŽÉ«ČÜŅŗ£ŗCu2+”¢H+”¢Cl-”¢HSO3- | |
| B£® | ÄÜŹ¹pHŹŌÖ½³ŹŗģÉ«µÄČÜŅŗ£ŗFe2+”¢Na+”¢Cl-”¢NO3- | |
| C£® | Na2CO3ČÜŅŗ£ŗK+”¢NO3-”¢Cl-”¢Al3+ | |
| D£® | $\frac{{K}_{W}}{c£ØH£©}$=0.1mol/LµÄČÜŅŗ£ŗNa+”¢K+”¢SiO32-”¢NO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬22.4L H20ÖŠŗ¬ÓŠµÄ·Ö×ÓŹżĪŖNA | |
| B£® | ŗ¬2.3g Na+µÄNa2OŗĶNa2O2µÄ»ģŗĻĪļÖŠ£¬ŅõĄė×Ó×ÜŹżµČÓŚ0.05NA | |
| C£® | 7£®lgCl2 Óė×ćĮæµÄĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦×ŖŅʵĵē×ÓŹżŅ»¶ØĪŖ0.2 NA | |
| D£® | 1L lmol/L CaCl2ČÜŅŗÖŠŗ¬ÓŠµÄĀČĄė×ÓŹżĪŖNA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
| ×°ÖĆ | 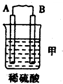 | 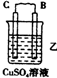 |  |
| ĻÖĻó | ¶ž¼Ū½šŹōA²»¶ĻČܽā | CµÄÖŹĮæŌö¼Ó | AÉĻÓŠĘųĢå²śÉś |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com