
“脑黄金”可谓是家喻户晓,其实脑黄金(DHA)就是从深海鱼油中提取出的不饱和程度很高的脂肪酸,它的分子中有6个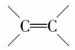 ,称为二十六碳六烯酸,则其甘油酯的结构简式为
,称为二十六碳六烯酸,则其甘油酯的结构简式为
( )
A.(C25H51COO)3C3H5 B.(C25H39COO)3C3H5
C.(C26H41COO)3C3H5 D.(C26H47COO)3C3H5
科目:高中化学 来源: 题型:
原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关,下列说法中不正确的是( )
A.由Al、Cu、稀H2SO4组成原电池,放电时SO42-向Al电极移动
B.由Mg、Al、NaOH溶液组成原电池,其负极反应式为:
Al-3e-+4OH-=AlO2-+2H2O
C.由Fe、Cu、NaCl溶液组成原电池,其负极反应式为:
Cu - 2e-= Cu2+
D.由Al、Cu、浓硝酸组成原电池作电源,用石墨电极来电解硝酸银溶液,当析出1 mol Ag时,消耗Cu电极32g
查看答案和解析>>
科目:高中化学 来源: 题型:
amolNa2O2和bmolNaHCO3混合置于密闭容器中,加热至300℃使其充分反应。密闭容器内固体为Na2CO3和NaOH混合物时,a和b的比值可能是
A. 0.8 B. 1.1 C. 1.8 D. 2.2
查看答案和解析>>
科目:高中化学 来源: 题型:
元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p 轨道上有4个电子。元素Z 的原子最外层电子数是其内层的3倍。
(1)X与Y所形成化合物晶体的晶胞如图所示。
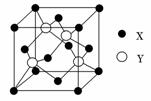
①在1个晶胞中,X离子的数目为________。
②该化合物的化学式为________。
(2)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是________。
(3)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是________。
(4)Y与Z可形成YZ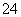 。
。
①YZ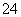 的空间构型为________(用文字描述)。
的空间构型为________(用文字描述)。
②写出一种与YZ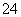 互为等电子体的分子的化学式:________。
互为等电子体的分子的化学式:________。
(5)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1 mol该配合物中含有σ键的数目为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于油脂的说法中,不正确的是
( )
A.所有的油脂都能发生皂化反应
B.为了便于油脂的运输,工业上常常把液态油进行氢化
C.油脂都比水轻,浮在水面上
D.纯净的花生油不饱和度高,具有固定的熔、沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
右图为硬脂酸甘油酯在碱性条件下水解的装置图。进行皂化反应时的步骤如下:
(1)在圆底烧瓶中加入8 g硬脂酸甘油酯,然后加入2 g氢氧化钠、5 mL水和10 mL酒精,加入酒精的作用是_____________________________________。
(2)隔着石棉网给反应物加热约10分钟,皂化反应基本完成,所得的
混合物为________(填“悬浊液”、“乳浊液”、“溶液”或“胶体”)。
(3)向所得混合物中加入________,静置一段时间后,溶液分为上下两层,肥皂在________层,这个操作称为________。
(4)图中长玻璃导管的作用为________。
(5)日常生活中用加热的纯碱溶液来洗涤粘有油脂的器皿的原因是__________________________________________________________________
________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
①钠、氢气都能在氯气中燃烧生成白色烟雾
②铜丝在氯气中燃烧,生成蓝绿色的氯化铜
③液氯就是氯气的水溶液,它能使干燥的有色布条褪色
④久置的氯水,因氯气几乎完全挥发掉,剩下的只有水
A.① B.①和② C.①和④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
同种物质中同一价态的元素部分被氧化,部分被还原的氧化还原反应是
( )
A.3Br2+6KOH====5KBr+KBrO3+3H2O
B.MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
C.2KNO3 2KNO2+O2↑
2KNO2+O2↑
D.NH4NO3 N2O↑+2H2O
N2O↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路。
其化学原理为:2FeCl3 + Cu→ 2FeCl2 + CuCl2。某实验小组的同学对该厂生产印刷电路后所得的废液进行了分析:取50.00 mL 废液,向其中加入足量的AgNO3溶液,析出沉淀43.05g(假设反应前后溶液的体积变化均忽略不计)。试回答:
(1)该厂使用的FeCl3溶液(原的)物质的量浓度________________;
(2)若向250.00 mL废液中加入足量的铜粉,充分反应后,铜粉质量减轻9.6g。
① 充分反应后的溶液中Cu2+的物质的量为 ;
② 原废液中各金属阳离子的物质的量浓度之比为: ;
(书写时须将离子符号和物质的量浓度做一一对应)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com