
 ),水杨酸(
),水杨酸( )、硝基苯与苯酚四种有机物的乙醚溶液,按如下流程利用物质的酸碱性依次分离,假设每一步分离都是完全的.(已知苯胺是一种难溶于水,具有弱碱性的有机物.)
)、硝基苯与苯酚四种有机物的乙醚溶液,按如下流程利用物质的酸碱性依次分离,假设每一步分离都是完全的.(已知苯胺是一种难溶于水,具有弱碱性的有机物.)
 ,请写出两种能鉴别乙酰水杨酸和水杨酸的化学试剂
,请写出两种能鉴别乙酰水杨酸和水杨酸的化学试剂 ),水杨酸(
),水杨酸( )、硝基苯与苯酚加入碳酸氢钠溶液,只有水杨酸反应,则水层1含有
)、硝基苯与苯酚加入碳酸氢钠溶液,只有水杨酸反应,则水层1含有 ,加入稀硫酸酸化,蒸馏可得物质1为
,加入稀硫酸酸化,蒸馏可得物质1为 ,乙醚层1含有
,乙醚层1含有 、硝基苯与苯酚,加入氢氧化钠,只有苯酚反应,则水层2为苯酚钠,通入二氧化碳气体可得苯酚,即物质2,乙醚层2含有
、硝基苯与苯酚,加入氢氧化钠,只有苯酚反应,则水层2为苯酚钠,通入二氧化碳气体可得苯酚,即物质2,乙醚层2含有 、硝基苯,加入盐酸,
、硝基苯,加入盐酸, 与盐酸反应,物质3为
与盐酸反应,物质3为 ,乙醚层3含有硝基苯、乙醚,蒸馏可得到乙醚和硝基苯,以此解答该题.
,乙醚层3含有硝基苯、乙醚,蒸馏可得到乙醚和硝基苯,以此解答该题. ),水杨酸(
),水杨酸( )、硝基苯与苯酚加入碳酸氢钠溶液,只有水杨酸反应,则水层1含有
)、硝基苯与苯酚加入碳酸氢钠溶液,只有水杨酸反应,则水层1含有 ,加入稀硫酸酸化,蒸馏可得物质1为
,加入稀硫酸酸化,蒸馏可得物质1为 ,乙醚层1含有
,乙醚层1含有 、硝基苯与苯酚,加入氢氧化钠,只有苯酚反应,则水层2为苯酚钠,通入二氧化碳气体可得苯酚,即物质2,乙醚层2含有
、硝基苯与苯酚,加入氢氧化钠,只有苯酚反应,则水层2为苯酚钠,通入二氧化碳气体可得苯酚,即物质2,乙醚层2含有 、硝基苯,加入盐酸,
、硝基苯,加入盐酸, 与盐酸反应,物质3为
与盐酸反应,物质3为 ,乙醚层3含有硝基苯、乙醚,蒸馏可得到乙醚和硝基苯,
,乙醚层3含有硝基苯、乙醚,蒸馏可得到乙醚和硝基苯, ,物质3为
,物质3为 ,分子式为C6H7N,故答案为:
,分子式为C6H7N,故答案为: ; C6H7N;
; C6H7N; 和
和 含有羧基,具有酸性,而
含有羧基,具有酸性,而 含有酚羟基,可与氯化铁发生显色反应,与浓溴水发生取代反应,则可用氯化铁溶液、浓溴水鉴别,
含有酚羟基,可与氯化铁发生显色反应,与浓溴水发生取代反应,则可用氯化铁溶液、浓溴水鉴别, 含有羧基、羟基,可发生缩聚反应生成高分子化合物,反应的方程式为n
含有羧基、羟基,可发生缩聚反应生成高分子化合物,反应的方程式为n
| 一定条件 |
 +(n-1)H2O,
+(n-1)H2O,
| 一定条件 |
 +(n-1)H2O.
+(n-1)H2O.


科目:高中化学 来源: 题型:

| A、用图1所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
| B、用图2所示装置除去CO2中含有的少量HCl |
| C、用图3所示装置制取并收集干燥纯净的NH3 |
| D、用图4所示装置吸收氨气并防止倒吸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 充电 |
| 放电 |
| A、放电时的负极反应为Li-e-=Li+ |
| B、若用该电池电解水,阴极生成3.52gO2,则该电池负极质量减少0.77g |
| C、锂离子电池充电时的阴极反应为Si+4.4e-+4.4Li+=Li4.4Si |
| D、放电时电解质LiPF6水溶液中的Li+移向正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 实验次数 | 初读数(mL) | 末读数(mL) |
| 1 | 0.20 | 21.40 |
| 2 | 0.00 | 21.00 |
| 3 | 1.60 | 26.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:
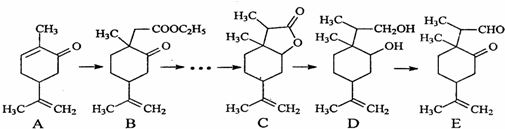
| CH3I |
| 催化剂 |
| LiBH4 |
| THF |
| LiBH4 |
| THF |
| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| D | ||
| A | B | C |
| E |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、3 mol,3mol |
| B、3 mol,5 mol |
| C、6 mol,8 mol |
| D、6 mol,10 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com