
| A、30%和H2O2溶液中加入MnO2可制得O2,MnO2做氧化剂 |
| B、SO2和CO2都属于酸性氧化物,Na2O和Al2O3都属于碱性氧化物 |
| C、在NH4Cl水溶液中,既存在水解平衡,又存在电离平衡 |
| D、O2在放电条件下生成O3属于化学变化,煤干馏得到焦炭属于物理变化 |


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
| ||
| ||
| ||
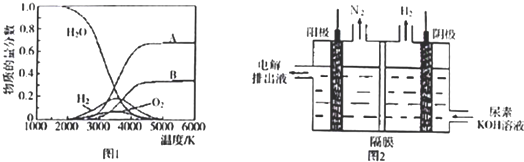
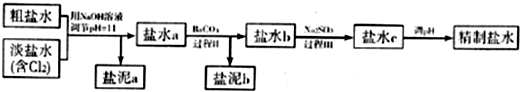
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| A、反应①②都是氧化还原反应 |
| B、反应②是置换反应 |
| C、反应①中Ti02:是氧化剂 |
| D、反应②中每生成1mol Ti转移4 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
| ||

| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
 在汽车上安装催化转化器可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)相互反应生成无毒害物质,减少汽车尾气污染.
在汽车上安装催化转化器可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)相互反应生成无毒害物质,减少汽车尾气污染.
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO) (×10-4mol?L-1) |
10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO) (×10-3mol?L-1) |
3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
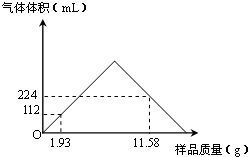 含钡化合物在实验室和工业生产中都有广泛的用途.
含钡化合物在实验室和工业生产中都有广泛的用途.| 500-520℃ |
| 1 |
| 9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将浓度为0.1mol?L-1 HF溶液加水不断稀释过程中,c( H+) 和c ( OH-)都会减小 |
| B、为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的PH.若PH>7,则H2A是弱酸;若PH<7,则H2A是强酸 |
| C、将SO2通入一定量KOH溶液,所得溶液呈中性,该溶液中一定含KHSO3 |
| D、用0.200mol?L-1 NaOH标准溶液滴定浓度均为0.1mol?L-1 的HCl与CH3COOH的混合液,至中性时,溶液中的酸恰好被完全中和 |
查看答案和解析>>
科目:高中化学 来源: 题型:

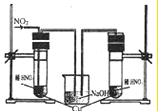
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com