
| W | X | |
| Y | Z |
| A. | X、Y、Z中最简单氢化物稳定性最弱的是Y | |
| B. | Z元素最高价氧化物对应水化物的酸性一定强于Y | |
| C. | X与Y元素形成的两种常见化合物分别溶于水后溶液PH<7 | |
| D. | Z元素单质在化学反应中只表现氧化性 |
分析 W、X、Y、Z四种短周期元素,W的气态氢化物可与其最高价含氧酸生成离子化合物,应是铵盐,则W是N元素,由元素在周期表中的位置可知,X为O元素、Y为S元素、Z为Cl元素,据此解答.
解答 解:W、X、Y、Z四种短周期元素,W的气态氢化物可与其最高价含氧酸生成离子化合物,应是铵盐,则W是N元素,由元素在周期表中的位置可知,X为O元素、Y为S元素、Z为Cl元素.
A.非金属O>S,Cl>S,则其氢化物中H2S最不稳定,故A正确;
B.非金属性Cl>S,氯元素的最高价含氧酸一定比Y的含氧酸酸性强,故B正确;
C.X与Y元素形成的两种常见化合物分别为SO2、SO3,溶于水分别得到亚硫酸、硫酸,溶液的PH<7,故C正确;
D.Cl2与水的反应生成HCl与HClO,硫酸既表现氧化性,也表现了还原性,故D错误;
故选D.
点评 本题考查位置结构性质关系、元素周期律等,难度不大,推断元素是解题的关键,注意整体把握元素周期表的结构,W是推断的突破口.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 各种物质都储存有化学能 | |
| B. | 化学反应一定伴随着能量的变化 | |
| C. | 断开反应物中的化学键要释放出能量 | |
| D. | 化学反应中的能量变化,通常主要表现为热量变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
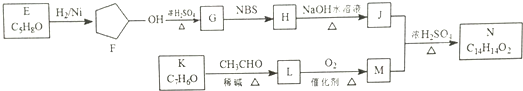
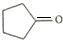 .
. .
.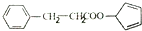 ,请再写出三种五元环上不是含一个双键的同分异构体:
,请再写出三种五元环上不是含一个双键的同分异构体: 、
、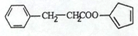 、
、 .
.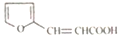 )是一种医治血吸虫病的药呋喃丙胺的原料.请以
)是一种医治血吸虫病的药呋喃丙胺的原料.请以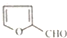 、CH3CH2OH为有机原料合成呋喃.(无机试剂及溶剂任选)
、CH3CH2OH为有机原料合成呋喃.(无机试剂及溶剂任选)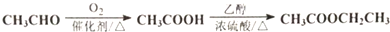
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | (1) | (2) | 分类标准 |
| A | 盐酸、漂白粉、水玻璃、双氧水 | 氨水 | 混合物 |
| B | CH3COOH,H2CO3、HClO、NH3•H2O | HF | 弱电解质 |
| C | 电解反应、盐的水解、煤的干馏、石油裂化 | 钢铁生锈 | 化学变化 |
| D | CO2、SO3、P2O5、SiO2 | Al2O3 | 酸性氧化物 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
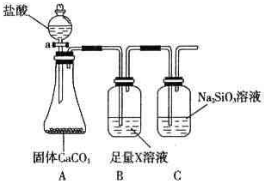
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 碘是人体所必需的因素之一回答以下有关碘的问题:
碘是人体所必需的因素之一回答以下有关碘的问题:| KI起始浓度/mol•L-1 | 0.02 | 0.04 | 0.06 | 0.08 | 0.10 |
| I3-% | 88.98 | 88.04 | 85.28 | 82.26 | 79.23 |
| I42-% | 4.38 | 8.67 | 12.60 | 16.21 | 19.53 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com