
雌黄与浓硝酸反应如下:As2 S3+28HNO3(浓) 2H3As04 +3H2S04+28N02↑+8H2O,
2H3As04 +3H2S04+28N02↑+8H2O,
下列说法正确的是
| A.氧化产物只有H2S04 |
| B.1mol As2S3发生反应,有28 mol电子转移 |
| C.该反应中As2S3既是氧化剂又是还原剂 |
| D.As2S3不可能与氧气反应 |
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江苏省高三12月练习测试化学试卷 题型:填空题
(14分)雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
(1) As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,则氧化剂与氧化产物的物质的量之比为 ▲ 。
(2)上述反应中产生的气体可用 ▲ 吸收。
(3) As2S3和HNO3有如下反应:As2S3+ 10H++ 10NO3— = 2H3AsO4+ 3S+10NO2↑+ 2H2O
若生成48g S,则生成标准状况下的NO2的体积为 ▲ L。若准确测得的实际体积小于理论值(计算值),请分析可能原因 ▲ 。
(4)某课外活动小组设计了以下实验方案验证Ag与浓HNO3反应的过程中可能产生NO。其实验流程图如下:

①测定硝酸的物质的量:
反应结束后,从如图B装置中所得100 mL溶液中取出25.00 mL溶液,用0.1 mol·L-1的NaOH溶液滴定,用酚酞作指示剂,滴定前后的滴定管中液面的位置如上图所示。在B容器中生成硝酸的物质的量为 ▲ 。
②测定NO的体积:
若实验测得NO的体积为112.0 mL(已折算到标准状况),则Ag与浓硝酸反应的过程中
▲ (填“有”或“没有”)NO产生,作此判断的依据是 ▲ 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年安徽省淮北市高三第一次模拟考试化学试卷 题型:选择题
雌黄与浓硝酸反应如下:As2 S3+28HNO3(浓)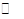 2H3As04 +3H2S04+28N02↑+8H2O,
2H3As04 +3H2S04+28N02↑+8H2O,
下列说法正确的是
A.氧化产物只有H2S04
B.1mol As2S3发生反应,有28 mol电子转移
C.该反应中As2S3既是氧化剂又是还原剂
D.As2S3不可能与氧气反应
查看答案和解析>>
科目:高中化学 来源: 题型:
雌黄与浓硝酸反应如下:As2 S3+28HNO3(浓)![]() 2H3As04 +3H2S04+28N02↑+8H2O,
2H3As04 +3H2S04+28N02↑+8H2O,
下列说法正确的是
A.氧化产物只有H2S04
B.1mol As2S3发生反应,有28 mol电子转移
C.该反应中As2S3既是氧化剂又是还原剂
D.As2S3不可能与氧气反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com