
森林是国民经济的宝贵资源,它不仅提供木材和多种林副产品,而且在保护环境、维持生态平衡方面起着极为重要的作用,试回答:
(1)森林通过什么途径吸收CO2,防止温室效应?
_______________________________________________________________。
(2)木材是重要的化工原料,其主要成分是纤维素,纤维素分子由很多个
________单元构成,在每个单元中含有________个羟基,所以纤维素能发生
________反应,它与浓H2SO4和浓HNO3的混合物发生反应的化学方程式是
________________________________________________________________。
(3)纤维素在浓硫酸的作用下水解的最终产物是________________(填结构简
式)。写出在医学上检验该物质的化学方程式_______________________
_______________________________________________________。
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是()
A. SO2和SiO2 B. CO2和H2O C. NaCl和HCl D. CCl4和KCl
查看答案和解析>>
科目:高中化学 来源: 题型:
木质素是制浆造纸工业的副产物,具有优良的物理化学特点,木质素的一种单体结构简式如图所示.下列说法错误的是( )

|
| A. | 该物质的分子式是C10H12O3,属于芳香烃 |
|
| B. | 该物质可以与FeCl3溶液发生显色反应,也能发生酯化反应 |
|
| C. | 1mol该物质最多能消耗4mol H2 |
|
| D. | 1mol该物质与溴水发生反应,可消耗4mol Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是 ( )。
A.体内葡萄糖的主要作用是氧化,为人体提供热能,还有一部分转化为糖
原,少量的参与机体的构成或发挥其他生理作用
B.人体如果摄入淀粉不足,就会动用体内储备的脂肪、蛋白质提供热能
C.如果摄入淀粉过多,多余的淀粉就会转化为脂肪,储存在皮下
D.淀粉在口腔内,在唾液淀粉酶的作用下全部水解为葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
工业制镜和热水瓶胆镀银时,常用________作________剂,反应时该糖中的________基被氧化成________基,反应的化学方程式为________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列除杂方案错误的是( )
| 选项 | 被提纯的物质 | 杂质 | 除杂试剂 | 除杂方法 |
| A. | CO(g) | CO2(g) | NaOH溶液、 浓H2SO4 | 洗气 |
| B. | NH4Cl(aq) | Fe3+(aq) | NaOH溶液 | 过滤 |
| C. | Cl2(g) | HCl(g) | 饱和食盐水、 浓H2SO4 | 洗气 |
| D. | Na2CO3(s) | NaHCO3(s) | — | 灼烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质应用的说法错误的是( )
A.玻璃容器可长期盛放各种酸
B.纯碱可用于清洗油污
C.浓氨水可检验氯气管道漏气
D.Na2S可除去污水中的Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
氢能源是一种重要的清洁能源。现有两种可产生H2的化合物甲和乙。将6.00 g甲加热至完全分解,只得到一种短周期元素的金属单质和6.72 LH2(已折算成标准状况)。甲与水反应也能产生H2,同时还产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液。化合物乙在催化剂存在下可分解得到H2和另一种单质气体丙,丙在标准状态下的密度为1.25 g/L。请回答下列问题:
(1)甲的化学式是_________;乙的电子式是__________。
(2)甲与水反应的化学方程式是__________________________________-。
(3)气体丙与金属镁反应的产物是_______(用化学式表示)。
(4)乙在加热条件下与CuO反应可生成Cu和气体丙,写出该反应的化学方程式_________。
有人提出产物Cu中可能还含有Cu2O,请设计实验方案验证之_________________________。
(已知Cu2O+2H+==Cu+Cu2++H2O)
(5)甲与乙之间_______(填“可能”或“不可能)发生反应产生H2,判断理由是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
ClO2与Cl2的氧化性相近。在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过题9图1装置(夹持装置略)对其制备、吸收、释放和应用进 行了研究。
行了研究。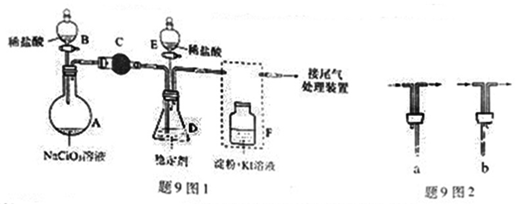
(1)仪器D的名称是。安装F中导管时,应选用题9 图2中的。
图2中的。
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。
为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜(填“快”或“慢”)。
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为,在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是。
(5)已吸收ClO2气体的稳定剂Ⅰ和Ⅱ,加酸后释放ClO2的浓度随时间的变化如题9图3所示,若将其用于水果保鲜,你认为效果较好的稳定剂是,原因是。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com