
| A. | 简单离子半径:D>B | |
| B. | 气态氢化物的稳定性:A>B | |
| C. | B、D两元素可组成阴、阳离子个数比为1:1的化合物 | |
| D. | B、C、D三种元素可组成化学式为DCB2的化合物,其水溶液显碱性 |
分析 A、B、C、D都是短周期元素,原子半径D>C>A>B,其中A、B处在同一周期,A、C处在同一主族,四种元素在周期表中的大致相对位置为: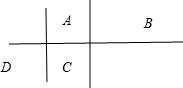 ,A、C处在同一主族,二者质子数相差8,C原子核内质子数等于A、B原子核内质子数之和,故B的质子数为8,则B为O元素;C原子最外层上的电子数是D原子最外层电子数的3倍,C最外层电子数一定小于6,则D最外层电子数只能为1,为Na元素;C为Al元素,A为B元素,据此结合元素周期律知识解答.
,A、C处在同一主族,二者质子数相差8,C原子核内质子数等于A、B原子核内质子数之和,故B的质子数为8,则B为O元素;C原子最外层上的电子数是D原子最外层电子数的3倍,C最外层电子数一定小于6,则D最外层电子数只能为1,为Na元素;C为Al元素,A为B元素,据此结合元素周期律知识解答.
解答 解:A、B、C、D都是短周期元素,原子半径D>C>A>B,其中A、B处在同一周期,A、C处在同一主族,四种元素在周期表中的大致相对位置为: ,A、C处在同一主族,二者质子数相差8,C原子核内质子数等于A、B原子核内质子数之和,故B的质子数为8,则B为O元素;C原子最外层上的电子数是D原子最外层电子数的3倍,C最外层电子数一定小于6,则D最外层电子数只能为1,为Na元素;C为Al元素,A为B元素,
,A、C处在同一主族,二者质子数相差8,C原子核内质子数等于A、B原子核内质子数之和,故B的质子数为8,则B为O元素;C原子最外层上的电子数是D原子最外层电子数的3倍,C最外层电子数一定小于6,则D最外层电子数只能为1,为Na元素;C为Al元素,A为B元素,
A.D的两种为钠离子,B的离子为氧离子,二者含有相同的电子层,钠离子的核电荷数大于氧离子,则离子半径:D<B,故A错误;
B.非金属性A<B,则气态氢化物的稳定性:A<B,故B错误;
C.D为Na、B为O,二者可以形成的混合物为Na2O、Na2O2,两种化合物中阴阳离子的个数比都是1:2,故C错误;
D.B、C、D三种元素组成的DCB2为NaAlO2,偏铝酸钠为强碱弱酸盐,溶液呈碱性,故D正确;
故选D.
点评 本题考查原子结构与元素周期律的应用,题目难度中等,正确推断元素的种类为解答该题的关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
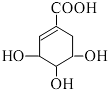
| A. | 分子式为 C7H6O5 | |
| B. | 分子中含有 2 种官能团 | |
| C. | 可发生加成和水解反应 | |
| D. | 该有机物能发生消去反应和催化氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
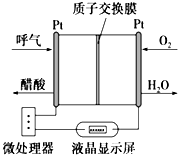 如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.其中电极均为Pt电极.下列说法不正确的是( )
如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.其中电极均为Pt电极.下列说法不正确的是( )| A. | 电流由O2所在的铂电极经外电路流向另一电极 | |
| B. | O2在右侧电极发生还原反应,且该电极附近溶液的pH升高 | |
| C. | 该电池的负极反应式为:CH3CH2OH+3H2O-12e-═2CO2↑+12H+ | |
| D. | 微处理器通过检测电流大小而计算出被测气体中酒精的含量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
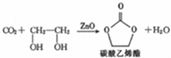
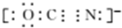 ,Y-的结构式为
,Y-的结构式为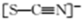 ,Z-的化学式为HF2-.
,Z-的化学式为HF2-.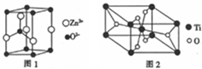
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L 0.1mol/L的NaHS溶液中HS-和S2-离子数之和为0.1NA | |
| B. | 3 mol Fe在足量的水蒸气中完全反应转移9NA个电子 | |
| C. | 2.0 g H218O与D2O的混合物中所含中子数为NA | |
| D. | 1 mol Na2CO3晶体中含离子总数大于3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 44gCO2和N2O的混合物中含有的氧原子数为1.5NA | |
| B. | 2L0.5mol/L亚硫酸氢钠溶液中含有的HSO3-离子数为NA | |
| C. | 氢氧化钠与氯气反应时,生成0.1molNaCl转移的电子数为0.1NA | |
| D. | 一定条件下在密闭容器中2molSO2与2molO2充分反应,最终的气体分子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤的干馏和煤的液化均是物理变化 | |
| B. | 用活性炭为蔗糖脱色和用臭氧漂白纸浆原理相似 | |
| C. | 雾霾是许多细小液体和固体微粒分散到空气中形成的一种气溶胶 | |
| D. | 光导纤维在信息领域应用越来越广泛,光导纤维的主要成分是Si单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液的pH一定等于1 | |
| B. | 阴离子肯定有I-,不能确定有无HCO${\;}_{3}^{-}$ | |
| C. | 阳离子肯定没有Fe3+,一定有Na+ | |
| D. | 该溶液含有的溶质成分可能为HI;或HI和NaI;或NaI和NaOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com