
| A. | 常温下将64g铜片投人过量浓硫酸中(铜片) | |
| B. | 向含有0.2molBa(OH)2和O.lmolNaOH的混合溶液中通人标况下3.36LCO2(CO2) | |
| C. | 向lOmL3mol•L-1的盐酸中加人5.6g铁(铁) | |
| D. | 向5.5gMn02粉末中加人20mL2mol•L-1双氧水(Mn02) |
分析 A、铜与浓硫酸在加热的条件下才发生反应;
B、标况下3.36LCO2(CO2)的物质的量为:$\frac{3.36}{22.4}$=0.15mol,而0.2mol的Ba(OH)2与0.2mol的二氧化碳反应;
C、5.6g铁(铁)是0.1mol,完全反应需要0.2mol的盐酸,而lOmL3mol•L-1的盐酸的物质的量为:0.03mol;
D、5.5gMn02粉末中加人20mL2mol•L-1双氧水(Mn02),二氧化锰是催化剂,反应前后质量不变.
解答 解:A、铜与浓硫酸在加热的条件下才发生反应,所以铜片没有消耗,故A错误;
B、标况下3.36LCO2(CO2)的物质的量为:$\frac{3.36}{22.4}$=0.15mol,而0.2mol的Ba(OH)2与0.2mol的二氧化碳反应,所以二氧化碳完全被消耗,故B正确;
C、5.6g铁(铁)是0.1mol,完全反应需要0.2mol的盐酸,而lOmL3mol•L-1的盐酸的物质的量为:0.03mol,所以铁过量,故C错误;
D、5.5gMn02粉末中加人20mL2mol•L-1双氧水(Mn02),二氧化锰是催化剂,反应前后质量不变,故D错误;
故选B.
点评 本题考查了元素化合物的性质,注意物质浓度对物质性质的影响、可逆反应特点,变价金属铁与硝酸反应量不同产物不同为该题的难点,题目难度中等.


科目:高中化学 来源: 题型:选择题
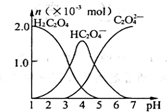 常温下,向10mL 0.2mol•L-1草酸(H2C2O4)溶液中逐滴加入等浓度的NaOH溶液.有关微粒的物质的量与混合溶液的pH有如图关系,下列说法正确的是
常温下,向10mL 0.2mol•L-1草酸(H2C2O4)溶液中逐滴加入等浓度的NaOH溶液.有关微粒的物质的量与混合溶液的pH有如图关系,下列说法正确的是| A. | HC2O4-在溶液中水解程度大于电离程度 | |
| B. | 当V(NaOH)=10 mL,时,溶液中水的电离程度比纯水大 | |
| C. | 当V(NaOH)=15 mL,时,溶液中存在:c(Na+)>c(HC2O4-)>c(C2O42-)>c(OH-)>c(H+) | |
| D. | 当V(NaOH)=20 mL,时,溶液中存在:c(OH-)=c(HC2O4-)+2c(H2C2O4)+c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L 1mol/L的稀硝酸中,氧原子数为3NA | |
| B. | 常温常压下的67.2L氯气与54g铝充分反应,转移电子数为6NA | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电数为0.2NA | |
| D. | 标准状况下,80gSO3,中含3NA心个氧原子,体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 35.7g | B. | 30g | C. | 17g | D. | 9g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molFe与足量的Cl2反应转移的电子数为2NA | |
| B. | 标准状况下,22.4L水中含有的水分子数为NA | |
| C. | 常温、常压下,22gCO2中含有的氧原子数为NA | |
| D. | 0.11mol/LCaCl2溶液中含氧离子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶解、过滤、蒸发、洗涤 | B. | 溶解、蒸发、洗涤、过滤 | ||
| C. | 溶解、过滤、洗涤、干燥 | D. | 溶解、洗涤、过滤、干燥 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com