
【题目】最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程.反应过程的示意图如下: 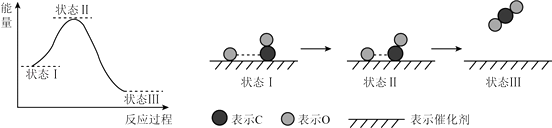
下列说法正确的是( )
A.CO和O生成CO2是吸热反应
B.在该过程中,CO断键形成C和O
C.CO和O生成了具有极性共价键的CO2
D.状态Ⅰ→状态Ⅲ表示CO与O2反应的过程
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】下列实验过程中,溶液的pH增大的是
A. 向NaOH溶液中加水 B. 向NaCl溶液中滴加稀盐酸
C. 向NaOH溶液中滴加稀盐酸 D. 向稀盐酸中滴加NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图所示,有关该有机物的叙述不正确的是( ) 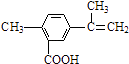
A.在一定条件下,能发生取代、氧化和加聚反应
B.该物质分子中最多可以有11个碳原子在同一平面上
C.1 mol该物质最多可与5 mol H2发生加成反应
D.1 mol该物质完全氧化最多可消耗13 mol氧气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸盐在能源环保领域有广泛用途。用镍 (Ni)、铁作电极电解浓NaOH溶液制备高铁酸钠(Na2FeO4)的装置如图所示。下列说法正确的是
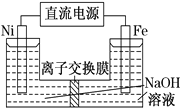
A. 铁是阳极,电极反应为Fe-2e-+2OH-===Fe(OH)2↓
B. 电解一段时间后,镍电极附近溶液的pH减小
C. 每制得1 mol Na2FeO4,理论上可以产生67.2L气体
D. 若离子交换膜为阴离子交换膜,则电解结束后左侧溶液中含有FeO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己烷雌酚的一种合成路线如图: 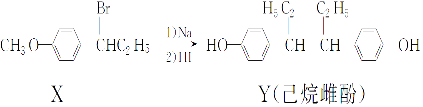
下列叙述正确的是( )
A.在NaOH 水溶液中加热,化合物X 可发生消去反应
B.在一定条件下,化合物Y可与浓溴水发生取代反应
C.用FeCl3溶液不能鉴别化合物X和Y
D.化合物Y中不含有手性碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂—磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,可通过下列反应制备:2Na3PO4+4CuSO4+2NH3H2O═Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)写出基态Cu2+的电子排布式:____________;与Cu同周期的元素中,与铜原子最外层电子数相等的元素还有____________(填元素符号)。
(2)PO43-的空间构型是____________。
(3)与SO42-互为等电子体的2种分子是______。
(4)氨水溶液中各元素原子的电负性从大到小排列顺序为_______________.
(5)氨基乙酸铜(结构简式:H2NCH2COO-Cu-OOC-CH2NH2)分子中碳原子的杂化方式为____________,基态碳原子核外电子占有_________个轨道。
(6)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,则1mol该配合物中含有的π键的物质的量为__________mol。
(7)铜晶体为面心立方最密堆积,配位数为___________,铜的原子半径为127.8pm,NA表示阿伏加德罗常数的值,列出晶体铜的密度计算式(不必化简)__________g/cm-3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学﹣﹣选修5:有机化学基础] 菠萝酯是一种带有浓郁的菠萝香气和香味的食用香料,其合成路线如下(部分反应条件及产物已略去):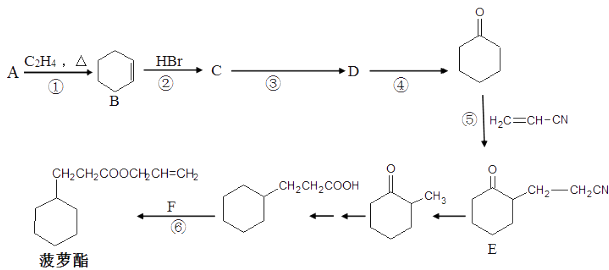
请回答下列问题:
(1)A可用于制备顺丁橡胶(顺式聚1,3﹣丁二烯),顺丁橡胶的链节为 , 若顺丁橡胶的平均相对分子质量为540108,则平均聚合度为 .
(2)F的结构简式为 , 反应④的条件是 .
(3)①一⑥反应中属于取代反应的是 .
(4)下列有关B的说法正确的是(填字母序号). a.元素分析仪可确定B的实验式为C6H10
b.质谱仪可检测B的最大质荷比的数值为82
c.红外光谱仪可测定B中六个碳原子一定在同一平面上
d.核磁共振仪可测定B有两种类型氢原子吸收峰
(5)写出反应③的化学方程式 .
(6)同时满足下列条件的E的同分异构体的数目为种. ①遇氯化铁溶液显紫色 ②苯环上只有2个取代基且处于对位
(7)参照上述合成路线,现仅以A为有机原料,无机试剂任选,设计制备 ![]() 的合成路线. 已知:①反应物分子的环外双键比环内双键更容易被氧化;
的合成路线. 已知:①反应物分子的环外双键比环内双键更容易被氧化;
② ![]() (R,R’代表烃基或氢) .
(R,R’代表烃基或氢) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如下图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是( )

A. 原子半径:W>Z>Y>X
B. 最高价氧化物对应水化物的酸性:X>W>Z
C. 最简单气态氢化物的热稳定性:Y>X>W>Z
D. 元素X、Z、W的最高化合价分别与其主族序数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaOH溶液可用于多种气体的处理.
(1)CO2是温室气体,可用NaOH溶液吸收得到Na2CO3或NaHCO3 . ①Na2CO3俗称纯碱,因CO32﹣水解而使其水溶液呈碱性,写出CO32﹣第一步水解的离子方程式 . 已知25℃时,CO32﹣第一步水解的平衡常数Kh=2×10﹣4mol/L,当溶液中c(HCO3﹣):c(CO32﹣)=20:1 时,溶液的pH= .
②泡沫灭火器中通常装有NaHCO溶液和Al2(SO4)3溶液,请写出这两种溶液混合时的离子反应方程式 .
(2)金属与浓硝酸反应产生的NO2可用NaOH溶液吸收,反应方程式为:2NO2+2NaOH=NaNO3+NaNO2+H2O.含0.2molNaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,溶液B为0.1molL﹣1CH3COONa溶液,则两份溶液中c(NO3﹣)、c(NO2﹣)和c(CH3COO﹣)由大到小的顺序为(已知HNO2的电离常数Ka=7.1×10﹣4molL﹣1 , CH3COOH的电离常数Ka=1.7×10﹣5molL﹣1).可使溶液A和溶液B的 pH相等的方法是 . A.向溶液A中加适量NaOH B.向溶液A中加适量水
C.向溶液B中加适量NaOH D.向溶液B中加适量水
(3)烟气中的SO2会引起酸雨,可利用氢氧化钠溶液吸收.吸收SO2的过裎中,溶液中H2SO3、HSO3﹣、SO32﹣三者所占物质的量分数(a)随pH变化的关系如图所示: 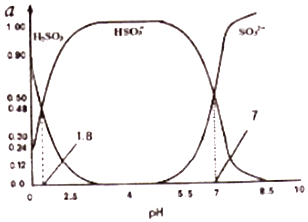
①图中pH=7时,溶液中离子浓度关系正确的是 .
A.c(Na+)>2c(SO32﹣)>c(HSO3﹣)
B.c(Na+)=c(SO32﹣ )+c(HSO3﹣)+c(H2SO3)
C.c(OH﹣)=c(H+)+c(H2SO3)+c(HSO3﹣)
D.c(Na+)>c(HSO3﹣)>c(SO32﹣ )>c(H+)=c(OH﹣)
②利用上图中数据,求反应H2SO3=2H++SO32﹣的平衡常数的数值 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com