
【题目】在方框内填入有机物的结构简式,并回答有关问题:
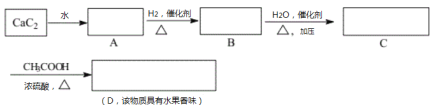
(1)写出A、B、C、D的结构简式:A:___________ B:____________C:___________ D:____________
(2)A→B的化学反应方程式是___________________________,反应类型是___________。
(3) C→D的化学反应方程式是___________________________,反应类型是___________。
(4)B在一定条件下可生成聚合物,其化学方程式是___________________,反应类型是_________。这种塑料会造成白色污染的原因是____________________________。
(5)A在一定条件下也可生成聚合物![]() ,人们发现这种聚合物可以导电,从而具有巨大的应用前景。这一发现在思想观念上给我们的启示是_______________________________________________。
,人们发现这种聚合物可以导电,从而具有巨大的应用前景。这一发现在思想观念上给我们的启示是_______________________________________________。
【答案】CH≡CH CH2=CH2 CH3CH2OH CH3COOC2H5 CH≡CH+H2![]() CH2=CH2 加成反应 CH3COOH+CH3CH2OH
CH2=CH2 加成反应 CH3COOH+CH3CH2OH![]() CH3COOC2H5+H2O 酯化反应 nCH2=CH2
CH3COOC2H5+H2O 酯化反应 nCH2=CH2![]() 加聚反应 不易降解 不能墨守成规等
加聚反应 不易降解 不能墨守成规等
【解析】
CaC2与水反应生成乙炔,则A为CH≡CH,CH≡CH与H2在催化剂、加热条件下生成乙烯,则B为CH2=CH2,CH2=CH2与H2O在催化剂、加热加压条件下生成乙醇,则C为CH3CH2OH,CH3CH2OH与CH3COOH在浓硫酸、加热条件下生成乙酸乙酯,则D为CH3COOC2H5,据此答题。
(1)由分析可知:A为CH≡CH,B为CH2=CH2,C为CH3CH2OH,D为CH3COOC2H5,故答案为:CH≡CH,CH2=CH2,CH3CH2OH,CH3COOC2H5。
(2)由分析可知:A→B的反应为乙炔与氢气在催化剂、加热条件下发生加成反应生成乙烯,反应方程式为:CH≡CH+H2![]() CH2=CH2,故答案为:CH≡CH+H2
CH2=CH2,故答案为:CH≡CH+H2![]() CH2=CH2,加成反应。
CH2=CH2,加成反应。
(3)由分析可知:C→D的反应为乙酸与乙醇在浓硫酸、加热条件下发生酯化反应生成乙酸乙酯,反应方程式为:CH3COOH+CH3CH2OH![]() CH3COOC2H5+H2O,故答案为:CH3COOH+CH3CH2OH
CH3COOC2H5+H2O,故答案为:CH3COOH+CH3CH2OH![]() CH3COOC2H5+H2O,酯化反应。
CH3COOC2H5+H2O,酯化反应。
(4)乙烯在一定条件下可以发生加聚反应生成聚乙烯,反应方程式为:nCH2=CH2![]() ,聚乙烯塑料在自然界中不易降解,会造成白色污染,故答案为:nCH2=CH2
,聚乙烯塑料在自然界中不易降解,会造成白色污染,故答案为:nCH2=CH2![]() ,加聚反应,不易降解。
,加聚反应,不易降解。
(5)乙炔在一定条件下可以发生加聚反应生成聚乙炔,这种聚合物可以导电,具有巨大的应用前景,这一发现在思想观念上给我们的启示是不能墨守成规等,故答案为:不能墨守成规等。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】碳、氮、氧、氟、钙、铜等元素的化合物广泛存在于自然界,回答下列问题:
(1) 将乙炔(C2H2)通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀。1个乙炔分子中σ键数目为___________,基态Cl原子的核外电子排布式为__________,[Cu(NH3)4] 2+中Cu 2+的配位数为___________。
(2)NF3是微电子工业中优良的等离子刻蚀气体。元素第一电离能N___________F(填“>”“<”或“=”), NF3中氮原子的杂化轨道类型为____________________,NF3分子的空间构型___________。
(3)氮的氧化物中与CO2互为等电子体的分子为___________(写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率,请回答下列问题。
(1)①工业合成氨反应:N2+3H2![]() 2NH3是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1molN2完全反应生成NH3可放出92kJ热量。如果将10molN2和足量H2混合,使其充分反应,放出的热量___(填“大于”、“小于”或“等于”)920kJ。
2NH3是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1molN2完全反应生成NH3可放出92kJ热量。如果将10molN2和足量H2混合,使其充分反应,放出的热量___(填“大于”、“小于”或“等于”)920kJ。
②已知断开1molN![]() N键吸收的能量为945.6kJ,形成1molN﹣H键放出的能量为391kJ,根据化学方程式N2+3H2
N键吸收的能量为945.6kJ,形成1molN﹣H键放出的能量为391kJ,根据化学方程式N2+3H2![]() 2NH3,生成标准状况下44.8LNH3时放出的能量为92.4kJ,则断开1molH﹣H键吸收的能量是___。
2NH3,生成标准状况下44.8LNH3时放出的能量为92.4kJ,则断开1molH﹣H键吸收的能量是___。
(2)某实验小组同学进行如图1所示实验,以检验化学反应中的能量变化。请根据你掌握的反应原理判断,②中的温度___(填“升高”或“降低”)。反应过程___(填“①”或“②”)的能量变化可用图2表示。
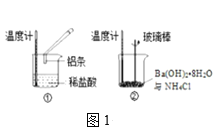
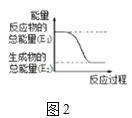
(3)已知化学反应A2(g)+B2(g)═2AB(g)的能量变化如图2所示,该反应是___(填“吸热”或“放热”)反应。
(4)用CH3OH和O2组合形成的质子交换膜燃料电池的结构如图3所示:

①则d电极是___(填“正极”或“负极”),c电极的电极反应式为___。
②若线路中转移2mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为___L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.碳元素广泛存在于自然界中,对人类生命和生活具有重要意义。含碳化合物在工业生产和国防建设中有广泛的应用。
(1)碳元素原子核外有_____个未成对电子,最外层有_____种能量不同的电子。CH4 分子的空间构型为_____,是_____分子。(填“极性”或“非极性”)
(2)碳和硅是同主族元素,下列能说明二者非金属性相对强弱的是_____(填编号)
a.CH4的稳定性比SiH4强 b.SiH4的沸点比CH4高
c.碳酸是强酸,硅酸是弱酸 d.碳原子半径比硅原子小
II.氮化硅(Si3N4)是一种重要的陶瓷材料,可用石英与焦炭在800℃氮气气氛下合成:3SiO2(s)+6C(s)+2N2(g)![]() Si3N4(s)+6CO(g)
Si3N4(s)+6CO(g)
(1)该反应的平衡常数表达式K_____。已知平衡常数:K(800℃)>K(850℃),则正反应是__________反应(填“放热”或“吸热”)
(2)任写两种能提高二氧化硅转化率的措施_____、_____。
(3)一定温度下,在2 L密闭容器内,充入一定量的反应物,5分钟时达到平衡,测得容器内气体增加了0.4mol,用CO表示该反应时间内的反应速率为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在指定环境中,下列各组离子一定可以大量共存的是
A.某无色溶液:Fe2+、NO![]() 、SO
、SO![]() 、Na+
、Na+
B.使紫色石蕊试液变红的溶液:NH![]() 、Mg2+、Cl-、K+
、Mg2+、Cl-、K+
C.加入铝粉放出氢气的溶液:Na+、Cl-、NH![]() 、NO3-
、NO3-
D.使无色酚酞试液显红色的溶液:S2-、K+、HCO![]() 、Al3+
、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 热化学方程式中,化学式前面的化学计量数既可表示微粒数,又可表示物质的量
B. 书写热化学方程式时,不仅要写明反应热的符号和数值,还要注明各物质的聚集状态
C. 热化学方程式中,如果没有注明温度和压强,则表示在标准状况下测得的数据
D. 凡是化合反应都是放热反应,分解反应都是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钒和钛金属的性能都很优越,在航空航天领域用途广泛。回答下列问题:
(1)钛元素基态原子的电子排布式为______________,未成对电子数为_______________个。
(2)[TiO(H2O2)2]2+配离子呈黄色。提供中心原子孤电子对的成键原子是_____________(填元素符号),中心原子的化合价为_____________;配体之一H2O2中氧原子杂化类型为__________,H2O2分子中氧原子的价层电子对互斥模型是______________。
(3)单质钒及钛都是由______________键形成的晶体,己知金属钛是六方最密堆积,金属钒是体心立方堆积,则__________(填“钛”,或“钒”)的空间利用率较大。
(4)碳化钒主要用于制造钒钢及碳化物硬质合金添加剂,其晶胞结构如图所示。
 (小球为V原子)
(小球为V原子)
①晶胞中碳原子与钒原子的数量比为____________。
②该晶胞中与碳原子距离最近且相等的碳原子个数为_____________。
③若合金的密度为dg· cm-3,晶胞参数α=______nm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行可逆反应,A与B反应生成C,其反应速率分别用υ(A)、υ(B)、υ(C)(molL﹣1s﹣1)表示,且υ(A)、υ(B)、υ(C)之间有如下所示的关系:υ(B)=3υ(A); 3υ(C)=2υ(B)。则此反应可表示为( )
A. 2A+3B![]() 2CB. A+3B
2CB. A+3B![]() 2C
2C
C. 3A+B![]() 2CD. A+B
2CD. A+B![]() C
C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用右图所示装置进行下列实验,实验结果与预测的现象不一致的是
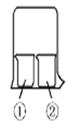
①中的物质 | ②中的物质 | 预测①中现象 | |
A | 淀粉碘化钾溶液 | 浓硝酸 | 无明显现象 |
B | 酚酞溶液 | 浓盐酸 | 无明显现象 |
C | 氯化铝溶液 | 浓氨水 | 有白色沉淀 |
D | 湿润红纸条 | 饱和氯水 | 红纸条褪色 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com