
已知:2H2(g) +O2(g) = 2H2O(g) ΔH =-483.6 kJ/mol
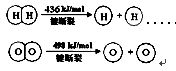
下列说法不正确的是
A.该反应原理可用于设计氢氧燃料电池
B.破坏1 mol H—O 键需要的能量是463.4 kJ
C.H2O(g)=H2(g) + 1/2O2(g) ΔH = +241.8 kJ/mol
D.H2(g) 中的H—H 键比 H2O(g) 中的H—O 键牢固
科目:高中化学 来源: 题型:
X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是 ( )
A.元素Y、Z、W具有相同电子层结构的离子,其半径依次增大
B.元素X不能与元素Y形成化合物
C.元素Y、R分别与元素X形成的化合物的热稳定性: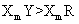
D.元素W、R的最高价氧化物的水化物都是强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
下列日常生活中的现象与氧化还原反应无关的是
A.铜铸塑像上出现铜绿[Cu2(0H)2C03] B.用石膏点豆腐
C.不良商贩用硫黄熏蒸法制作“白豆芽” D.自来水厂用氯气对水进行消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中,一定条件下进行如下反应:
NO(g) + CO(g) 
 N2(g) + CO2(g);△H=-373.2 kJ/mol ,达到平衡后,为提高该反应的速率和NO的转化率,采取的措施正确的是
N2(g) + CO2(g);△H=-373.2 kJ/mol ,达到平衡后,为提高该反应的速率和NO的转化率,采取的措施正确的是
A. 加催化剂 B. 减小反应容器体积
C. 升高温度 D. 增大NO浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
0.100 mL 6 mol·L-1 H2SO4跟过量锌粉反应,在一定温度下,为了减缓反应速率,但又不影响生成氢气的总量,可向反应物中加入适量下列物质中的:①硫酸钠固体 ②水 ③硫酸钾溶液 ④硝酸钾溶液 ⑤醋酸钠固体 ⑥硫酸铜固体
A. ②③⑤ B. ①④⑤ C. ②③⑥ D. ③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
请回答下列问题:
(1)在一定温度下,下列叙述是可逆反应A(g)+3B(g) 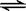 2C(g)达到平衡的标志的是
2C(g)达到平衡的标志的是
①C的生成速率与C的分解速率相等;
②单位时间生成amol A,同时生成3amol B;
③A、B 、C的浓度不再变化;
、C的浓度不再变化;
④A、B、C的分子数目比为1:3:2 ;
⑤混合气体的总压强不再变化;
⑥混合气体的物质的量不再变化;
⑦单位时间消耗amol A,同时生成3amol B;
⑧单位时间内生成a mol C,同时生成 mol B
mol B
(2)在稀氨水中存在下述电离平衡NH3+H2O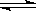 NH3 ·H2O
NH3 ·H2O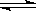 NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?(填“增大”、“减小”或“不变”);平衡移动方向如何?(填“正向移动”或“逆向移动”)
NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?(填“增大”、“减小”或“不变”);平衡移动方向如何?(填“正向移动”或“逆向移动”)
| 加入的物质 | 少量NH4Cl | 少量KOH溶液 |
| c(OH-)的变化 | ||
| 平衡移动方向 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于仪器使用的说法正确的是( )
A.滴定管装滴定液时应先用滴定液润洗
B.锥形瓶用作反应容器时一定不能加热
C.蒸馏时温度计水银球可以高于蒸馏烧瓶支管口
D.振荡分液漏斗时应关闭玻璃塞和活塞
查看答案和解析>>
科目:高中化学 来源: 题型:
下述实验设计能够达到目的的是( )
| 编号 | 实验目的 | 实验设计 |
| A | 证明盐酸酸性比醋酸强 | 用同一电路测等体积的盐酸、醋酸溶液的导电性 |
| B | 证明H2CO3酸性比H2SiO3强 | 将CO2通入Na2SiO3溶液中 |
| C | 证明钠的金属活动性比铜强 | 向CuCl2溶液中投入金属钠 |
| D | 证明溶液中含有I- | 向溶液中加入淀粉 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com