
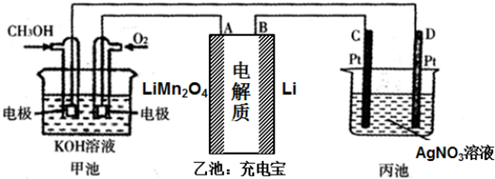
分析 (1)甲装置中能发生自发的氧化还原反应,属于原电池,负极上燃料失电子;
(2)a.A与正极相连为阳极,阳极上LiMn2O4失电子;
b.B与负极相连为阴极;
c.电解时,阳离子向阴极移动;
(3)D与负极相连为阴极,阴极上银离子得电子生成Ag,根据电子守恒计算.
解答 解:(1)甲装置中能发生自发的氧化还原反应,属于原电池,碱性条件下,负极上甲醇失电子生成碳酸根离子和水,则电极方程式为:CH3OH-6e-+8OH-=CO32-+6H2O;
故答案为:CH3OH-6e-+8OH-=CO32-+6H2O;
(2)a.A与正极相连为阳极,阳极上LiMn2O4失电子,则阳极的电极方程式为:LiMn2O4-xe-═Li1-xMn2O4+xLi+,故a正确;
b.B与通入甲醇的一极相连,即与负极相连为阴极,阴极上发生得电子的还原反应,故b错误;
c.A与正极相连为阳极,电解时,阳离子向阴极移动,即乙池中Li+向B极移动,故c错误;
故答案为:a;
(3)当甲池中消耗标准状况下224mL O2 时,即消耗氧气为$\frac{0.224L}{22.4L/mol}$=0.01mol,则转移电子为0.04mol,D与负极相连为阴极,阴极上银离子得电子生成Ag,转移0.04mol电子时生成0.04mol银,则银的质量为0.04mol×108g/mol=4.32g;
故答案为:4.32.
点评 本题考查化学电源新型电池和电解原理的应用,题目难度中等,本题注意根据电池总反应式正确判断电极反应,并能书写电极反应式是解答该题的关键.


科目:高中化学 来源: 题型:选择题
| A. | 将2 mol NO和2 mol O2混合,充分反应后体系中原子总数为8NA | |
| B. | 将100 mL 0.1 mol•L-1的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒0.01NA | |
| C. | CO2通过Na2O2使其增重a g时,反应中转移的电子数为$\frac{a}{56}$NA | |
| D. | 100 g质量分数为9.8%的H2SO4水溶液中含氧原子数目为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
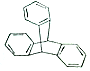 2016年诺贝尔化学奖由法国、美国及荷兰的三位化学家共同获得,以表彰他们在“分子马达”研究方面的成就.最初的“分子马达”的关键组件是三叠烯(如图),下列有关三叠烯的说法正确的是( )
2016年诺贝尔化学奖由法国、美国及荷兰的三位化学家共同获得,以表彰他们在“分子马达”研究方面的成就.最初的“分子马达”的关键组件是三叠烯(如图),下列有关三叠烯的说法正确的是( )| A. | 分子式为C20H14 | B. | 属于苯的同系物 | ||
| C. | 能与溴水发生加成反应 | D. | 分子中所有原子可能在同一平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3+、Cu2+、NO3-、S2- | B. | Fe2+、H+、Cl-、NO3- | ||
| C. | Fe3+、K+、Cl-、I- | D. | Fe2+、Fe3+、Cu2+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④>①=②>③ | B. | ①>④>②>③ | C. | ④>①>③>② | D. | ④>②>①>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑤ | B. | ①②⑤ | C. | ②③⑥ | D. | ③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe(OH)2、Fe(OH)3;Fe3O4 | B. | Fe(OH)2;FeO | ||
| C. | Fe(OH)2、Fe(OH)3;Fe2O3 | D. | Fe2O3;Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,36g18O2中所含的中子数为16NA | |
| B. | 1mol乙烯分子中含有共用电子对数为6NA | |
| C. | 电解饱和食盐水时,阳极上生成22.4L气体时转移的电子数为2NA | |
| D. | 标准状况下,2.24LCl2溶于水达到饱和,可得到HClO分子的数目是0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com