
”¾ĢāÄæ”æÄæĒ°¹ś¼ŹÉĻŹ¹ÓƵĔ°ŗ£Ė®µ»Æ”±Ö÷ŅŖ¼¼ŹõÖ®Ņ»ŹĒÕōĮ󣬽«ŗ£Ė®±ä³ÉÕōĘū£¬ÕōĘū¾¹żĄäČ“µĆµ½µĖ®£¬Ź£ÓąµÄČÜŅŗæÉÓĆĄ“ĢįČ”ĀČ»ÆÄĘ”¢ĀČ»ÆĆ¾µČ¶ąÖÖ¹¤ŅµŌĮĻ£®¹¤ŅµÉĻÓƵē½āČŪČŚNaCl»ņMgCl2µÄ·½·Ø·Ö±šÖʱø½šŹōÄĘŗĶĆ¾£¬Ķ¬Ź±µĆµ½ĀČĘų£®
£Ø1£©Čō½šŹōÄĘ³¤ĘŚ±©Ā¶ŌŚæÕĘųÖŠ£¬×īÖÕ×Ŗ»ÆĪŖ £¬ Č”Ņ»¶ØĮæµÄøĆĪļÖŹČÜÓŚĖ®ÅäÖĘ³É±„ŗĶČÜŅŗ£¬ĶØČėCO2ĘųĢåŗó·¢ĻÖČÜŅŗ±ä»ė×Ē£¬Š“³ö·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ £®
£Ø2£©Čō½šŹōÄĘ×Å»š£¬²»ÄÜÓĆøɱłĆš»šĘ÷Ćš»š£¬ŌŅņŹĒ£ØÓĆ»Æѧ·½³ĢŹ½±ķŹ¾£© £®
Čō½šŹōĆ¾×Å»š£¬Ņ²²»ÄÜÓĆøɱłĆš»šĘ÷Ćš»š£¬ŌŅņŹĒ£ØÓĆ»ÆѧŹ½±ķŹ¾£©
£Ø3£©½üÄźĄ“ÓŠČĖĢį³öĮĖŅ»ÖÖĄūÓĆĀČ¼ī¹¤Ņµ²śĘ·¼°ĀČ»ÆÄĘŃ»·ÖĪĄķŗ¬¶žŃõ»ÆĮņ·ĻĘų²¢»ŲŹÕ¶žŃõ»ÆĮņµÄ·½·Ø£¬øĆ·½·ØµÄĮ÷³ĢČēĻĀ£ŗ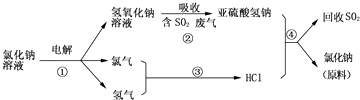
Š“³ö·“Ó¦¢ŚµÄ»Æѧ·½³ĢŹ½£»
Š“³ö·“Ó¦¢ÜµÄ»Æѧ·½³ĢŹ½ £®
ĀČĘųÅÅ·Å»įĪŪČ¾»·¾³£¬æÉÓĆNaOHČÜŅŗĄ“ĪüŹÕCl2 £¬ Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ £®
”¾“š°ø”æ
£Ø1£©Na2CO3£»Na2CO3+CO2+H2O=2NaHCO3”ż
£Ø2£©2Na+O2 ![]() Na2O2 £¬ 2Na2O2+2CO2=2Na2CO3+O2£»2Mg+CO2
Na2O2 £¬ 2Na2O2+2CO2=2Na2CO3+O2£»2Mg+CO2 ![]() 2MgO+C
2MgO+C
£Ø3£©NaOH+SO2=NaHSO3£»NaHSO3+HCl=NaCl+SO2”ü+H2O£»Cl2+2NaOH=NaCl+NaClO+H2O
”¾½āĪö”æ½ā£ŗ£Ø1£©ĒŠæŖ½šŹōÄĘÖĆÓŚæÕĘųÖŠ£¬ĒŠæŚæŖŹ¼³ŹŅų°×É«£ØÄʵÄÕęĆęÄ棩”ś±ä°µ£ØÉś³ÉNa2O£©”ś±ä°×É«¹ĢĢå£ØÉś³ÉNaOH£©”ś³ÉŅŗ£ØNaOH³±½ā£©”ś½įæé£ØĪüŹÕCO2³ÉNa2CO310H2O£©”ś×īŗó±ä³ÉNa2CO3·ŪÄ©£Ø·ē»Æ£©£¬ÓŠ¹Ų·“Ó¦ČēĻĀ£ŗ4Na+O2=2Na2O”¢Na2O+H2O=2NaOH”¢2NaOH+CO2=Na2CO3+H2O”¢Na2CO3+10H2O=Na2CO310H2O”¢Na2CO310H2O=Na2CO3+10H2O£¬Č”Ņ»¶ØĮæµÄøĆĪļÖŹČÜÓŚĖ®ÅäÖĘ³É±„ŗĶČÜŅŗ£¬ĶØČėCO2ĘųĢåŗó·¢ĻÖČÜŅŗ±ä»ė×Ē£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗNa2CO3+CO2+H2O=2NaHCO3”ż£¬
ĖłŅŌ“š°øŹĒ£ŗNa2CO3£»Na2CO3+CO2+H2O=2NaHCO3”ż£»£Ø2£©Čō½šŹōÄĘ×Å»š£¬²»ÄÜÓĆøɱłĆš»šĘ÷Ćš»š£¬ŅņĪŖÄĒČ¼ÉÕÉś³É¹żŃõ»ÆÄĘ£¬¹żŃõ»ÆÄĘŗĶ¶žŃõ»ÆĢ¼·“Ӧɜ³ÉĢ¼ĖįÄĘŗĶŃõĘų£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2Na+O2 ![]() Na2O2 £¬ 2Na2O2+2CO2=2Na2CO3+O2 £¬ Ć¾ŗĶ¶žŃõ»ÆĢ¼ĘųĢå·¢Éś·“Ӧɜ³ÉŃõ»ÆĆ¾ŗĶĢ¼£¬×Å»šŹ±²»ÄÜÓĆCO2Ćš»š£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2Mg+CO2
Na2O2 £¬ 2Na2O2+2CO2=2Na2CO3+O2 £¬ Ć¾ŗĶ¶žŃõ»ÆĢ¼ĘųĢå·¢Éś·“Ӧɜ³ÉŃõ»ÆĆ¾ŗĶĢ¼£¬×Å»šŹ±²»ÄÜÓĆCO2Ćš»š£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2Mg+CO2 ![]() 2MgO+C£¬
2MgO+C£¬
ĖłŅŌ“š°øŹĒ£ŗ2Na+O2 ![]() Na2O2 £¬ 2Na2O2+2CO2=2Na2CO3+O2 £»2Mg+CO2
Na2O2 £¬ 2Na2O2+2CO2=2Na2CO3+O2 £»2Mg+CO2 ![]() 2MgO+C£»£Ø3£©¶žŃõ»ÆĮņĪŖĖįŠŌĘųĢ壬æÉÓėĒāŃõ»ÆÄĘ·“Ӧɜ³ÉŃĒĮņĖįÄĘŗĶĖ®£¬»Æѧ·½³ĢŹ½ĪŖ£ŗSO2+NaOH=NaHSO3 £¬ ŅņČõĖįµÄĖįŹ½ŃĪÄÜÓėĒæĖį·“Ó¦£ŗNaHSO3+HCl=NaCl+SO2”ü+H2O£¬ĀČĘųÅÅ·Å»įĪŪČ¾»·¾³£¬æÉÓĆNaOHČÜŅŗĄ“ĪüŹÕCl2 £¬ ·“Ӧɜ³ÉĀČ»ÆÄĘ”¢“ĪĀČĖįÄĘŗĶĖ®£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗCl2+2NaOH=NaCl+NaClO+H2O£¬
2MgO+C£»£Ø3£©¶žŃõ»ÆĮņĪŖĖįŠŌĘųĢ壬æÉÓėĒāŃõ»ÆÄĘ·“Ӧɜ³ÉŃĒĮņĖįÄĘŗĶĖ®£¬»Æѧ·½³ĢŹ½ĪŖ£ŗSO2+NaOH=NaHSO3 £¬ ŅņČõĖįµÄĖįŹ½ŃĪÄÜÓėĒæĖį·“Ó¦£ŗNaHSO3+HCl=NaCl+SO2”ü+H2O£¬ĀČĘųÅÅ·Å»įĪŪČ¾»·¾³£¬æÉÓĆNaOHČÜŅŗĄ“ĪüŹÕCl2 £¬ ·“Ӧɜ³ÉĀČ»ÆÄĘ”¢“ĪĀČĖįÄĘŗĶĖ®£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗCl2+2NaOH=NaCl+NaClO+H2O£¬
ĖłŅŌ“š°øŹĒ£ŗSO2+NaOH=NaHSO3£»NaHSO3+HCl=NaCl+SO2”ü+H2O£»Cl2+2NaOH=NaCl+NaClO+H2O£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ·Ö×ÓŹ½ĪŖC4H9ClµÄĶ¬·ÖŅģ¹¹ĢåÓŠ£Ø £©
A.1ÖÖ
B.2ÖÖ
C.3ÖÖ
D.4ÖÖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫ĢśŗĶŃõ»ÆĢśµÄ»ģŗĻĪļ5.44g¼ÓČė50mL 3.2molL©1µÄŃĪĖį£¬Ē”ŗĆĶźČ«·“Ó¦£¬µĪČėKSCNČÜŅŗŗó²»ĻŌŗģÉ«£®ČōŗöĀŌČÜŅŗĢå»żµÄ±ä»Æ£¬ŌņŌŚĖłµĆČÜŅŗÖŠFe2+µÄÅضČŌ¼ĪŖ£Ø £©
A.0.2molL©1
B.0.4molL©1
C.0.8molL©1
D.1.6molL©1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»ÖÖ¹ā»Æѧµē³ŲµÄ½į¹¹ČēĶ¼ĖłŹ¾£¬µē³Ų×Ü·“Ó¦ĪŖ£ŗAgCl(s)£«Cu£«(aq)===Ag(s)£«Cu2£«(aq)£«Cl£(aq)£¬ĻĀĮŠ¹ŲÓŚøƵē³ŲŌŚ¹¤×÷Ź±µÄĖµ·ØÖŠÕżČ·µÄŹĒ

A. Éś³É108 gŅų£¬×ŖŅʵē×ÓøöŹżĪŖ1 mol
B. Cu£«ŌŚøŗ¼«·¢ÉśŃõ»Æ·“Ó¦
C. Agµē¼«»īĘĆ£¬AgŹ§µē×Ó·¢ÉśŃõ»Æ·“Ó¦
D. Cl£ÓÉøŗ¼«ĒØŅʵ½Õż¼«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æK2Cr2O7ČÜŅŗÖŠ“ęŌŚĘ½ŗā£ŗCr2O72-£Ø³ČÉ«£©+H2O![]() 2CrO42-£Ø»ĘÉ«£©+2H+”£ÓĆK2Cr2O7ČÜŅŗ½ųŠŠĻĀĮŠŹµŃé£ŗ½įŗĻŹµŃ飬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
2CrO42-£Ø»ĘÉ«£©+2H+”£ÓĆK2Cr2O7ČÜŅŗ½ųŠŠĻĀĮŠŹµŃé£ŗ½įŗĻŹµŃ飬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ

A. ¢ŁÖŠČÜŅŗ³ČÉ«¼ÓÉī£¬¢ŪÖŠČÜŅŗ±ä»Ę
B. ¢ŚÖŠCr2O72-±»C2H5OH»¹Ō
C. ¶Ō±Č¢ŚŗĶ¢ÜæÉÖŖK2Cr2O7ĖįŠŌČÜŅŗŃõ»ÆŠŌĒæ
D. ČōĻņ¢ÜÖŠ¼ÓČė70%H2SO4ČÜŅŗÖĮ¹żĮ棬ČÜŅŗ±äĪŖ³ČÉ«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©³£ĪĀĻĀ£¬ŌŚ200 mLĒāŃõ»Æ±µČÜŅŗÖŠŗ¬ÓŠ1”Į10-3molµÄ±µĄė×Ó£¬½«“ĖČÜŅŗÓėpH£½3µÄŃĪĖį»ģŗĻ£¬Ź¹Ęä»ģŗĻČÜŅŗµÄpH£½7£¬Ó¦Č”ĒāŃõ»Æ±µČÜŅŗŗĶŃĪĖįµÄĢå»żÖ®±ČŹĒ_________”£
£Ø2£©25”ꏱ£¬ĄūÓĆpHŹŌÖ½²āµĆ0.1molL-1“×ĖįČÜŅŗµÄpHŌ¼ĪŖ3£¬ŌņæÉŅŌ¹ĄĖć³ö“×ĖįµÄµēĄė³£ŹżŌ¼ĪŖ_______£»Ļņ10mL“ĖČÜŅŗÖŠ¼ÓČėÉŁĮæ±ł“×Ėį£¬ŗöĀŌČܽā¹ż³ĢÖŠČÜŅŗĪĀ¶ČŗĶĢå»żµÄĪ¢Š”±ä»Æ£¬ČÜŅŗÖŠc£ØH£«£©/c£ØCH3COOH£©µÄÖµ½«_____£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°ĪŽ·ØČ·¶Ø”±£©”£
£Ø3£©25 ”ꏱ£¬pH=3µÄNH4Al(SO4)2ÖŠ2c(SO42-)£c(NH4+)£3c(Al3£«)£½______£ØČ”½üĖĘÖµ£©
£Ø4£©ŹŅĪĀŹ±£¬Ļņ100mL0.1mol”¤L£1NH4HSO4ČÜŅŗÖŠµĪ¼Ó0.1mol”¤L£1NaOHČÜŅŗ£¬ČÜŅŗpHÓėNaOHČÜŅŗĢå»żµÄ¹ŲĻµĒśĻßČēĶ¼ĖłŹ¾£ŗŹŌ·ÖĪöĶ¼ÖŠa”¢b”¢c”¢dĖÄøöµć£¬Ė®µÄµēĄė³Ģ¶Č×ī“óµÄŹĒ________µć£»ŌŚbµć£¬ČÜŅŗÖŠø÷Ąė×ÓÅضČÓɓ󵽊”µÄÅÅĮŠĖ³ŠņŹĒ__________________________

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÖ¤Ć÷ijČÜŅŗÖ»ŗ¬ÓŠFe2+¶ų²»ŗ¬ÓŠFe3+µÄŹµŃé·½·ØŹĒ
A£®ĻȵĪ¼ÓĀČĖ®£¬ŌŁµĪ¼ÓKSCNČÜŅŗŗóĻŌŗģÉ«
B£®ĻȵĪ¼ÓKSCNČÜŅŗ£¬²»ĻŌŗģÉ«£¬ŌŁµĪ¼ÓĀČĖ®ŗóĻŌŗģÉ«
C£®µĪ¼ÓNaOHČÜŅŗ£¬²śÉś°×É«³Įµķ
D£®Ö»ŠčµĪ¼ÓKSCNČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ŌÓŚŅŌĻĀµÄ·“Ó¦¹ż³Ģ£¬Ņ»¶ØŅŖ¼ÓČėŃõ»Æ¼Į²ÅÄܹ»ŹµĻֵďĒ
A. O2”śH2O B. SO2”śSO42”Ŗ
C. H2SO4”śCuSO4 D. HNO3”śNO2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ ĻĀĮŠĪļÖŹŌŚĖ®ÖŠČܽāŠŌ×īŗƵďĒ£Ø £©
A.CO2B.NH3C.SO2D.CH4
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com