
| A. | b=2 | |
| B. | 两次平衡的平衡常数相同 | |
| C. | A与B的平衡转化率之比为1:2 | |
| D. | 第二次平衡时,C的浓度为0.4 mol•L-1 |
分析 A.达到平衡体系中再加入1molC(g),重新达到平衡后A、B、C的体积分数不变,说明压强不影响化学平衡,则反应前后气体的总计量数相等,即:b+1=3;
B.由于温度不变,化学平衡常数不变;
C.根据加入A、B的物质的量与反应计量数之比都是1:2分析;
D.压强不影响化学平衡,反应前后气体总物质的量、各物质的百分含量不变,重新达到平衡时C的物质的量为:(1+2+1)mol×10%=0.4mol,然后根据c=$\frac{n}{V}$计算第二次平衡时C的浓度.
解答 解:A.在此平衡体系中加入1molC(g),再次达到平衡后,A、B、C的体积分数不变,说明压强不影响化学平衡,则b+1=3,即b=2,故A正确;
B.由于温度不变,则化学平衡常数不变,所以两次平衡的平衡常数相同,故B正确;
C.由于加入A、B的物质的量与反应计量数之比都是1:2,则A与B的平衡转化率相等,故C错误;
D.由于压强不影响化学平衡,反应前后气体总物质的量、各物质的百分含量不变,则重新达到平衡时C的物质的量为:(1+2+1)mol×10%=0.4mol,所以第二次平衡时,C的浓度为$\frac{0.4mol}{1L}$=0.4 mol•L-1,故D正确;
故选C.
点评 本题考查了化学平衡的计算,题目难度中等,正确判断计量数b的数值为解答关键,注意掌握化学平衡及其影响因素,试题培养了学生的分析能力及灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 放电时电解质溶液的密度减小 | B. | 放电时K+向Cd极区移动 | ||
| C. | 充电时阳极Cd元素被氧化 | D. | 充电时阴极附近的pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 氟 | 氯 | 溴 | 碘 | |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
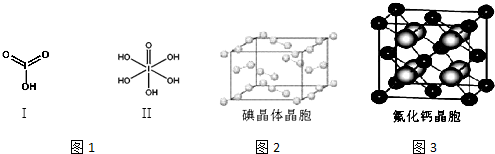
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 +NaOH$\stackrel{H_{2}O}{→}$
+NaOH$\stackrel{H_{2}O}{→}$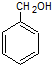 +NaCl,反应类型为取代反应.
+NaCl,反应类型为取代反应. .
. .
.
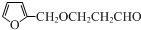

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 进行蒸发操作时,当溶液中出现较多固体时即可停止加热 | |
| B. | 进行蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 乙醇中含有少量水可加入生石灰再蒸馏制得无水乙醇 | |
| B. | 将无水乙醇和浓硫酸按体积比3:1混合,加热至170℃制取乙烯 | |
| C. | 蔗糖水解用浓硫酸作催化剂 | |
| D. | 油脂皂化反应后,反应混合物中加入食盐可将肥皂分离出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:S2->Cl->Ca2+ | B. | 还原性:I->Br->Cl- | ||
| C. | 热稳定性:HCl>H2S>H2Se | D. | 酸性:HClO4<HBrO4<HIO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com