
| A. | 增大氧气浓度,平衡向正方向移动,K值不变 | |
| B. | 平衡时SO2气体的转化率为50% | |
| C. | 该条件下反应放出0.5QkJ的热量 | |
| D. | 降低温度,正反应速率比逆反应速率减小的程度小 |
分析 依据反应前后气体物质的量变化可知反应前后气体物质的量减小为反应的氧气物质的量;结合化学反应三段式列式计算,设二氧化硫起始量为x;
2SO2(g)+O2(g)$?_{加热}^{催化剂}$ 2SO3(g)+QkJ
起始量(mol) x 1 0
变化量(mol) 0.25 0.5 0.25
平衡量(mol) x-0.25 0.5 0.25
依据化学平衡移动原理分析判断.
解答 解:A.增大压强浓度,增大反应物浓度,平衡正向进行,但温度不变,平衡常数不变,故A正确;
B.二氧化硫的起始量不知不能计算转化率,故B错误;
C.依据反应放热,1mol氧气反应放热QKJ,反应了0.5mol氧气,放热0.5QKJ,故C正确;
D.降低温度反应速率减小,正逆反应速率减小,反应是放热反应,平衡正向进行,正向反应速率减小的少,故D正确;
故选B.
点评 本题考查了化学平衡影响因素和反应热量变化的分析判断,掌握基础是关键,题目难度中等.


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:选择题
| A. | 氮气和氢气不再发生反应时的状态 | |
| B. | 体系中的总压强不变时的状态 | |
| C. | 氮气的浓度与氢气的浓度之比为1:3时 | |
| D. | 混合物的密度保持不变时的状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| B. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 过滤时,玻璃棒的末端应轻轻靠在三层滤纸处 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
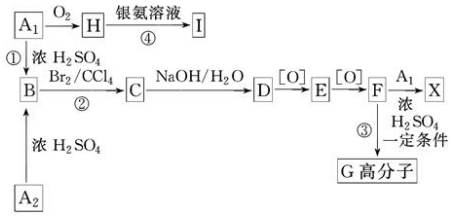
 .
. .
. .
. 、
、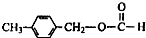
 、
、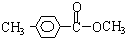 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向水中滴入少量稀盐酸,平衡逆向移动,Kw 减小 | |
| B. | 将水加热,Kw增大,pH<7 | |
| C. | 向水中通入少量HCl气体,平衡逆向移动,c(H+ )降低 | |
| D. | 向水中加入少量固体硫酸钠,c(H+ )和Kw 均不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 在一定条件下,在容积不变的密闭容器内进行反应:2NO+2CO?N2+2CO2 △H<0.曲线a表示NO的转化率与反应时间的关系,若改变初始条件,使反应过程按照曲线b进行,可采取的措施是( )
在一定条件下,在容积不变的密闭容器内进行反应:2NO+2CO?N2+2CO2 △H<0.曲线a表示NO的转化率与反应时间的关系,若改变初始条件,使反应过程按照曲线b进行,可采取的措施是( )| A. | 加催化剂 | B. | 降低温度 | C. | 增大NO的浓度 | D. | 缩小容器体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl和NaOH反应的中和热△H=-57.3 kJ•mol-1,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ•mol-1 | |
| B. | CO(g)燃烧热283.0 kJ•mol-1,2CO2(g)═2CO(g)+O2(g)的△H=+2×283.0 kJ•mol-1 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将称量NaOH固体时在烧杯中溶解后立即转移到容量瓶中 | |
| B. | 向容量瓶中加水定容时俯视 所配溶液浓度偏高 | |
| C. | 配制NaOH溶液不需用到量筒 | |
| D. | 定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:W>Z>Y | |
| B. | W的最高价氧化物对应水化物的酸性强于Z的最高价氧化物对应水化物的酸性 | |
| C. | X与Z形成的简单化合物比X与W形成的简单化合物稳定 | |
| D. | X与Y形成的化合物一定只含极性键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com