
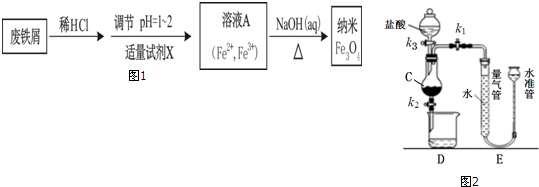
���� ��м��ϡ�����ܽ�õ��Ȼ�������Һ��������ҺpH�������Լ�X������������ΪFe2+������Fe3+�������ǹ����������ˮ�ȣ��ټ���NaOH��Һ�����ȵõ�����Fe3O4��
��1��ʢ�����������Ϊ��Һ©����
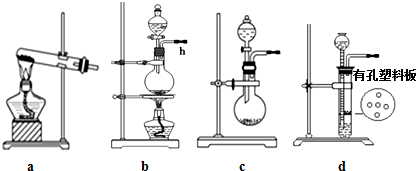
��2����a������������ˮ�����Ȼ�̼����CCl4�ӷ���
b��������ѹ��ˮ��Һ��ȸߣ����ɲⶨ���������
c�������DZ�֤װ����ѹǿ��������ѹ��ȣ����������¶������������ȴ��������С��
�ڲ������Dz������������������Ҫװ��C��Fe��ȫ��Ӧ��
��3���Ʊ���ҺA���Լ�X�ǽ���������ΪFe2+������Fe3+����Ҫѡ�����ǿ�����Ե����ʣ�
��4��Fe2+��Fe3+�ڼ��ԡ����������·�Ӧ�õ�Fe3O4������ˮ���ɣ��Ʊ��з�ֹ�������ӱ�����������
��5���������ӽ�����������Ϊ�ⵥ�ʣ����������Һ����ɫ���ζ��յ�ʱ��ɫ��ȥ��
�ڸ��ݹ�ϵʽ��Fe3O4��2Fe3+��I2��2S2O32-���㣮
��� �⣺��м��ϡ�����ܽ�õ��Ȼ�������Һ��������ҺpH�������Լ�X������������ΪFe2+������Fe3+�������ǹ����������ˮ�ȣ��ټ���NaOH��Һ�����ȵõ�����Fe3O4��
��1��ʢ�����������Ϊ��Һ©����
�ʴ�Ϊ����Һ©����
��2����a������������ˮ�����Ȼ�̼����Ӱ����������������CCl4�ӷ�����Ⱦ��������a����
b��������ѹ��ˮ�ܵ�ˮ������������������ѹ��ˮ��Һ��ȸߣ����ɲⶨ������������ᵼ��ʵ��ʧ�ܣ���b����
c�������DZ�֤װ����ѹǿ��������ѹ��ȣ����������¶������������ȴ��������С��Ӧ�ָ����£���c��ȷ��
��ѡ��c��
�ڲ������Dz������������������Ҫװ��C��Fe��ȫ��Ӧ������C�й�����ȫ��ʧ������C�в��������ݣ�˵����Ӧ��ȫ��
�ʴ�Ϊ������C�й�����ȫ��ʧ������C�в��������ݣ�
��3���Ʊ���ҺA���Լ�X�ǽ���������ΪFe2+������Fe3+����Ҫѡ�����ǿ�����Ե����ʣ���������ˮ��������������ᣬ�����ӿ���������������
��ѡ��abd��
��4��Fe2+��Fe3+�ڼ��ԡ����������·�Ӧ�õ�Fe3O4������ˮ���ɣ���Ӧ���ӷ���ʽΪ��Fe2++2Fe3++8OH-$\frac{\underline{\;\;��\;\;}}{\;}$Fe3O4+4H2O���� N2�����£���ֹFe2+������
�ʴ�Ϊ��Fe2++2Fe3++8OH-$\frac{\underline{\;\;��\;\;}}{\;}$Fe3O4+4H2O���� N2�����£���ֹFe2+��������
��5���������ӽ�����������Ϊ�ⵥ�ʣ����������Һ����ɫ����Na2S2O3��Һ�ζ��ζ��ⵥ�ʣ��ζ��յ�������ǣ���Һ��ɫ��ȥ���Ұ���Ӳ���ɫ��
�ʴ�Ϊ����Һ��ɫ��ȥ���Ұ���Ӳ���ɫ��
������Ʒ��Fe3O4����������Ϊa����
Fe3O4��2Fe3+��I2��2S2O32-
232g 2mol
ma g V��10-3L��c mol/L��$\frac{100mL}{10mL}$
����232g��ma g=2mol��V��10-3L��c mol/L��$\frac{100mL}{10mL}$
���a=$\frac{116cV}{m}$%
�ʴ�Ϊ��$\frac{116cV}{m}$%��
���� ���⿼�������Ʊ�ʵ���붨���ⶨʵ�飬�ؼ��Ƕ�ԭ�������⣬���������������������ζ��й�ϵʽ���㣬��������Ԫ�ػ��������ʣ���Ŀ������ѧ������������֪ʶǨ������������


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | sp2�ӻ�����γɦҼ���δ�ӻ���2p����γɦм� | |
| B�� | sp2�ӻ�����γɦм���δ�ӻ���2p����γɦҼ� | |
| C�� | C��H֮���γɵ���s-p �Ҽ���C��C֮��Ħм���δ�μ��ӻ���2p����γɵ� | |
| D�� | C��C֮���γɵ���sp2-sp2�Ҽ���C��H֮����δ�μ��ӻ���2p����γɵĦм� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��֪���±�Ϊ25��ʱijЩ����ĵ���ƽ�ⳣ����
��֪���±�Ϊ25��ʱijЩ����ĵ���ƽ�ⳣ����| CH3COOH | HClO | H2CO3 |
| Ka=1.8��10-5 | Ka=3.0��10-8 | Ka1=4.4��10-7Ka2=4.7��10-11 |
| A�� | 25��ʱ����ͬŨ�ȵ�CH3COONa��Һ�ļ��Դ���NaClO��Һ | |
| B�� | ��NaClO��Һ��ͨ������������̼�����ӷ���ʽΪ2ClO-+CO2+H2O�T2HClO+CO${\;}_{3}^{2-}$ | |
| C�� | ͼ�� I����CH3COOH��Һ��ϡ�� | |
| D�� | ͼ����a�������Ũ�ȴ���b�������Ũ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���Ϸ�ʽ��mol�� | H2��������� | ||||
| ���� | CO��g�� | H2O��g�� | CO2��g�� | H2��g�� | |
| ����һ | 1 | 3 | 0 | 0 | a% |
| ���϶� | 0 | 1.2 | 0.6 | 0.6 | b% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �����£���ijŨ��NaOH��Һ�ζ�һԪ��HA�ĵζ�������ͼ��ʾ��������Ϊ����NaOH�������������Ϊ���û��Һ��pH���������ж���ȷ����
�����£���ijŨ��NaOH��Һ�ζ�һԪ��HA�ĵζ�������ͼ��ʾ��������Ϊ����NaOH�������������Ϊ���û��Һ��pH���������ж���ȷ����| A�� | HA��Ũ��Ϊ1��10-4mol•L-1 | B�� | ʵ��ʱ��ѡ������ָʾ�� | ||
| C�� | pH=7ʱ����Һ��c��Na+����c��A-�� | D�� | V=10mL�����ǡ���к� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com