
选用下列试剂和电极:稀 H2 SO4、Fe2(SO4)3溶液、铁棒、铜棒、铂棒,组成如图所示的原电池装置(只有两个电极),观察到电流计Ⓖ的指针均明显偏转,则其可能的组合共有 ( )。

A.6种 B.5种
C.4种 D.3种
科目:高中化学 来源: 题型:
科学家发现某药物M能治疗心血管疾病是因为它在人体内能释放出一种“信使分子”D,并阐明了D在人体内的作用原理。
请回答下列问题:
(1)已知M的相对分子质量为227,由C、H、O、N四种元素组成,C、H、N的质量分数依次为15.86%、2.20%和18.50%,则M的分子式是____________。D是双原子分子,相对分子质量为30,则D的分子式是______________________________。
(2)油脂A经如图所示的途径可得到M。

图中②的提示为:

反应①的化学方程式是
________________________________________________________________________;
反应②的化学方程式是
(3)C是B和乙酸在一定条件下反应生成的化合物,相对分子质量为134,写出C所有可能的结构简式: ________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
火力发电厂释放出大量二氧化碳,对燃煤废气进行脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。将CO2转化为甲醇是一种新型脱碳技术,其反应为CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH。
(1)取五份等体积的CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图Ⅰ所示,则上述CO2转化为甲醇的反应的ΔH________0(填“>”、“<”或“=”)。

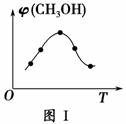
(2)如图Ⅱ是在恒温密闭容器中,压强为p1时H2的体积分数随时间t的变化曲线,请在图中画出该反应在p2(p2>p1)时H2的 体积分数随时间t的变化曲线。
(3)在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2,进行上述反应。测得CO2和CH3OH(g)的物质的量浓度随时间的变化如图Ⅲ所示。

则0~10 min内,氢气的平均反应速率为________;该温度下,反应的平衡常数为________(保留三位有效数字);10 min后,向该容器中再充入1 mol CO2和3 mol H2,则再次达到平衡时CH3OH(g)的体积分数________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学发现在炽热的煤炭上洒少量水,煤炉中会产生淡蓝色的火焰,炉火更旺。因此该同学得出结论“煤炭燃烧时加少量水,可使煤炭燃烧时放出更多的热量”。已知:煤炭的燃烧热为 393.15 kJ · mol-1 ,氢气的燃烧热为 242 kJ· mol-1 ,一氧化碳的燃烧热为 283 kJ · mol-1 。下列有关说法正确的是
A.表示氢气燃烧热的热化学方程式为 2H2(g)+ O2(g)===2H2O (l) ΔH= -242 kJ · mol-1
B.表示CO 燃烧热的热化学方程式为 2CO(g)+ O2(g)===2CO2 (g) ΔH= - 566 kJ · mol-1
C.“炉火更旺”是因为少量的固体煤炭转化为可燃性气体
D.因 242 kJ·mol-1 +283 kJ· mol-1 >393.15 kJ·mol-1 ,故该同学的结论是对的
查看答案和解析>>
科目:高中化学 来源: 题型:
化学反应过程中一定伴随着能量变化,某同学通过如下实验进行探究。
Ⅰ.探究化学反应中的能量变化。通过如下实验测出,烧杯中的温度降低。
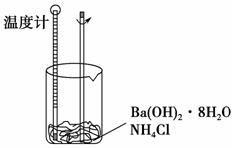
(1)Ba(OH)2·8H2O跟NH4Cl的反应的化学方程式:
________________________________________________________________。
(2)从反应热的角度分析,该反应属于________(填“吸热”或“放热”)反应;从氧化还原角度分析,该反应属于
________(填“氧化还原”或“非氧化还原”)反应;从基本反应类型上分析,该反应属于________反应。
Ⅱ.测定稀硫酸和氢氧化钠溶液反应的中和热(实验装置如图所示)。
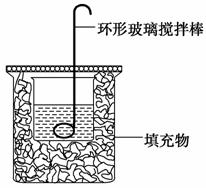
(1)图中尚缺少的一种仪器是________。
(2)实验时环形玻璃搅拌棒的运动方向是________。
a.上下运动 b.左右运动
c.顺时针运动 d.逆时针运动
(3)写出反应的热化学方程式为_______________________________________
________________________________________________________________________(中和热为57.3 kJ·mol-1)。
(4)该同学每次分别取0.50 mol·L-1 50 mL NaOH溶液和0.50 mol·L -130 mL硫酸进行实验,通过多次实验测定中和热ΔH= -53.5 kJ·mol-1,与57.3 kJ·mol-1有偏差,产生偏差的原因不可能是________(填字母)。
a.实验装置保温、隔热效果差
b.用量筒量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定硫酸溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
有关电化学知识的描述正确的是 ( )。
A.理论上说,任何能自发进行的氧化还原反应都可设计成原电池
B.某原电池反应为Cu+2AgNO3===Cu(NO3)2+2Ag,装置中的盐桥内可以是含琼脂的KCl饱和溶液
C.因为铁的活泼性强于铜,所以将铁、铜用导线连接后放入浓硝酸中组成原电池,必是铁作负极,铜作正极,其负极反应式为Fe-2e-===Fe2+
D.由Al、Mg与氢氧化钠溶液组成的原电池,其负极反应式为Mg-2e-+
2OH-===Mg(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生活、生产有着密切关系,下列叙述中正确的是 ( )。
A.钢铁发生析氢腐蚀时,H+得电子释放出H2,钢铁被腐蚀
B.钢铁发生吸氧腐蚀时,OH-失电子释放出O2,钢铁被腐蚀
C.船底镶嵌锌块,锌发生还原反应而被消耗,以保护船体
D.外加电源的正极连接在海水中的钢铁闸门上,可保护闸门
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家预言超级原子的发现将会重建周期表,2005年1月美国科学家在《Science》上发表论文,宣布发现了A1的超原子结构A113和A114,并在质谱仪检测到稳定的A113I一等,Al13、Al14的性质很像现行周期表中的某主族元素,己知这类超原子当具有40个价电子时最稳定(例Al原子具有3个价电子)。下列说法不正确的是
A. Al14有42个价电子,且与IIA族元素性质相似
B. Al13有39个价电子,且与卤素性质类似
C. Al13在气相中与HI反应可生成H Al13I,且化学
方程式为 AI13+HI=H AI13I
D. Al13原子中A1原子间是通过离子键结合的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com