
【物质结构与性质】(15分)
根据元素周期表中第四周期元素的相关知识,回答下列问题:
(1)第四周期元素的基态原子的电子排布中4s轨道上只有1个电子的元素有_______种;
写出Cu+的核外电子排布式_________。
(2)按电子排布,可将周期表里的元素划分成五个区域,第四周期元素中属于s区的元素有___________种,属于d区的元素有________种。
(3)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为________;CaO的焰色反应为砖红色,许多金属或它们的化合物都可以发生焰色反应,其原因是________。

(4)由叠氮化钾(KN3)热分解可得纯 ,下列有关说法正确的是________(填选项字母)。
,下列有关说法正确的是________(填选项字母)。
A.NaN3与KN3结构类似,前者晶格能较小
B.晶体钾的晶胞结构如右图所示,每个晶胞中分摊2个钾原子
C.氮的第一电离能大于氧
D.氮气常温下很稳定,是因为氮的电负性小
(5)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂。O2在其催化作用下,可将CN-氧化成CNO-。CN-的电子式为________,CNO-的中心原子的杂化方式为____________。
(6)在CrCl3溶液中,一定条件下存在组成为 (n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:
(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:
将含0.0015mol 的溶液,与R-H完全交换后,中和生成的需浓度为
的溶液,与R-H完全交换后,中和生成的需浓度为
0.1200 mol/LNaOH溶液25.00 mL,则该配离子的化学式为____________。
(1) 3 (1分) 1s22s22p63s23p63d10 (1分)
(2) 2 (1分) 8(1分)
(3) 6 (1分) 激发态的电子从能量高的轨道跃迁到能量较低的轨道时,以一定波长光的形式释放能量。 (2分,给分点:电子跃迁、释放能量)
(4) B C (2分,各1分,错选不得分)
(5) 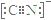 (2分) sp杂化 (2分)
(2分) sp杂化 (2分)
(6) [CrCl(H2O)5]2+(2分)
【解析】
试题分析:(1)4s轨道上只有1个电子的元素有K、Cr、Cu三种元素;Cu原子序数为29,核外电子排布式为:1s22s22p63s23p63d104s1,Cu+失去最外层电子,即失去了4s轨道的电子,故答案为:3;1s22s22p63s23p63d10;
(2)s区包括第ⅠA、ⅡA族,第四周期只有两种元素位于这两族;d区包括元素周期表从第三列到第十列,共8种元素;故答案为:2;8;
(3)观察该晶体属于NaCl型,其配位数为6,当电子受到激发,再从激发态跃迁的基态时释放能量,发出特定波长的光,故答案为:6、激发态的电子从能量高的轨道跃迁到能量较低的轨道时,以一定波长光的形式释放能量;
(4)A.离子半径小,晶格能越大,钠离子半径小于钾离子,故A错误;
B.根据均摊法计算,钾原子位于顶点和体心,每个晶胞含钾原子为8×1/8+1=2,故B正确;
C.氮原子价电子排布式为2s22p3,2p轨道半充满,较为稳定,第一电离能大于氧原子,故C正确;
D.氮气分子内形成氮氮三键,所以其化学性质稳定,并不是因为电负性小,故D错误;
故答案为:BC;
(5)C原子最外层四个电子,形成四对共用电子对,N原子最外层有五个电子,形成三对共用电子对,CN-得到一个电子,可写出电子式为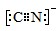 ;该离子与CO为等电子体,与CO杂化类型一致,CO的价电子对数=4/2=2,为sp杂化;
;该离子与CO为等电子体,与CO杂化类型一致,CO的价电子对数=4/2=2,为sp杂化;
(6)c(H+)=c(NaOH)=0.1200mol?L-1×25.00mL×10-3=0.003mol,根据方程式,和0.0015mol[CrCln(H2O)6-n]x+,x=2,所以离子中配体Cl-个数为1,可写出离子式:[CrCl(H2O)5]2+.
考点:考查物质结构与性质,涉及核外电子排布规律、电离能、杂化理论、分子结构、晶胞结构、配位键等相关知识。


科目:高中化学 来源:2013-2014浙江省五校高三第二次联考理综化学试卷(解析版) 题型:填空题
(14分)为回收利用废钒催化剂(含有V2O5、VOSO4及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺,主要流程如下:

部分含钒物质在水中的溶解性如下:
物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
回答下列问题:
⑴工业由V2O5冶炼金属钒常用铝热剂法,写出该反应的化学方程式 。
⑵滤液中含钒的主要成分为 (写化学式)。
⑶该工艺中反应③的沉淀率(又称沉钒率)是回收钒的关键之一,该步反应的离子方程式 ;沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH4Cl加入质量与料液中V2O5的质量比)和温度。根据下图判断最佳控制氯化铵系数和温度为 、 。
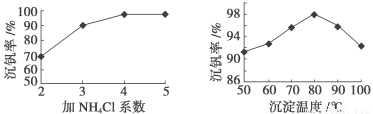
⑷用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应②后溶液中含钒量,反应的离子方程式为□VO2+ +□H2C2O4+□_____ =□VO2++□CO2↑+□H2O,试将其配平。
⑸全矾液流电池的电解质溶液为VOSO4溶液,电池的工作原理为VO2+ +V2++2H+  VO2++H2O+V3+,电池充电时阳极的电极反应式为 。
VO2++H2O+V3+,电池充电时阳极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省高二下学期期中考试化学试卷(解析版) 题型:选择题
165℃、1×105Pa下,两气态有机物以任意比例混合,1L该混合物与9LO2混合,充分燃烧后所得气体体积仍为10L,下列各组混合烃中符合此条件的是( )
A.CH4、C2H6 B.CH4、C3H6 C.CH3OH、C3H4 D.CH4、C3H4
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省豫东、豫北十所名校高三阶段性测试理综化学试卷(解析版) 题型:填空题
(15分)
M、N、O、P、Q是元素周期表中原子序数依次递增的前四周期元素。M原子最外层电子数为内层电子数的3倍;N的焰色反应呈黄色;O的氢化物是一种强酸,其浓溶液可与M、Q的化合物反应生成O的单质;P是一种金属元素,其基态原子中有6个未成对电子。请回答下列问题:
(1)元素Q的名称为__________,P的基态原子价层电子排布式为__________ 。
(2)O的氢化物的沸点比其上一周期同族元素的氢化物低,是因为__________________________.
(3)M、O电负性大小顺序是__________(用元素符号表示),O的最高价含氧酸根的空间构型为__________,其中心原子的杂化类型为___________。
(4)M、N形成的化合物的晶胞如图所示,该晶胞的化学式为__________ ,其中M离子的配位数为__________,该晶体类型为___________。
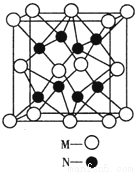
(5)该晶胞的边长为a×10 cm,则距离最近的M、N离子间的距离为
cm,则距离最近的M、N离子间的距离为
__________cm。
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省豫东、豫北十所名校高三阶段性测试理综化学试卷(解析版) 题型:选择题
T℃时,CaCO3和CaF2的Ksp分别为1.0 ×10-10。和4.0 ×10-12。下列说法正确的是
A.T℃时,两饱和溶液中c(Ca2+ ):CaCO3>CaF2
B.T℃时,两饱和溶液等体积混合,会析出CaF2固体
C.T℃时,CaF2固体在稀盐酸中的Ksp比在纯水中的Ksp大
D.T℃时,向CaCO3悬浊液中加NaF固体,可能析出CaF2固体
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省濮阳市高二下学期升级考试化学试卷(解析版) 题型:填空题
(6分)现有浓度为0.lmol/L的五种电解质溶液:①Na2CO3 ②NaHCO3 ③NaAlO2④CH3COONa⑤NaOH
已知:
(1)上述五种溶液的pH由大到小的顺序为________。(填序号)
(2)将五种溶液稀释相同的倍数时,其pH变化最大的是________。(填序号)
(3)在上述五种溶液中分别加入AlCl3溶液后,能产生无色气体的是_______:(填序号)
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省濮阳市高二下学期升级考试化学试卷(解析版) 题型:选择题
家用炒菜铁锅用水清洗放置后,出现红棕色的锈斑,在此变化过程中不发生的化学反应是
A.4Fe(OH)2+2H2O+O2═4Fe(OH)3
B.2Fe+2H2O+O2═2Fe(OH)2
C.2H2O+O2+4e-═4OH-
D.Fe-3e-═Fe3+
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省濮阳市高三第二次模拟考试理综化学试卷(解析版) 题型:简答题
水是一种重要的自然资源,是人类赖以生存不可缺少的物质。水质优劣直接影响人体健康。请回答下列问题:
(l)天然水中溶解的气体主要有____、____ ______(填化学式)。
(2)检验蒸馏水的纯度时,最简单易行的方法是测定水的____。
(3)水的净化与软化的区别是:水的净化是用混凝剂(如明矾等)使____,而水的软化是 。
(4)通过施加一定压力使水分子透过半透膜而将大分子或离子截留,从而使水得以净化的方法称为____;电渗析法净化水时,使离子通过半透膜的推动力是____。
(5)某天然水中。c(Ca2+)=1.2×10-3mol/L,c(Mg2+)=6×10-4mol/L,c(HCO3-)=8×10-4mol/L,
要软化10  这种天然水,需先加入Ca(OH)2_______g,再加入Na2CO3_______g。
这种天然水,需先加入Ca(OH)2_______g,再加入Na2CO3_______g。
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省洛阳市高三年级第三次考试理综化学试卷(解析版) 题型:推断题
(15分)铜是过渡金属元素,可以形成多种化合物。
(1)CuCl的盐酸溶液能够与CO发生反应:CuCl+CO+H2O=Cu(CO)Cl·H2O
①电负性:C ______O(填“>”或“=”或“<”)。②CO常温下为气体,固态时属于 晶体。
(2)Cu+与NH3形成的配合物可表示成[Cu(NH3)n]+,该配合物中,Cu+的4s轨道及4p通过sp杂化接受NH3提供的电子对。 [Cu(NH3) n]+ 中Cu+ 与n个氮原子的空间结构呈 型,n= 。
(3)CuCl2溶液与乙二胺(H2N—CH2—CH2—NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写):
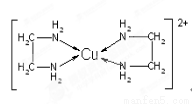
请回答下列问题:
①该配离子[Cu(En)2]2+中的中心原子的基态外围电子排布式为 。
②乙二胺分子中氮原子轨道的杂化类型为 ,乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是 。
③该配离子[Cu(En)2]2+中存在的作用力类型有 (填字母);
A配位键 B极性键 C离子键
D非极性键 E.氢键 F.金属键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com