
| A. | 金刚石和石墨互称同位素 | B. | 甲烷和异丁烷互称同系物 | ||
| C. | 医用消毒酒精中乙醇的浓度为95% | D. |  和 和 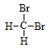 互称同分异构体 互称同分异构体 |
分析 A.同种元素的不同原子之间互为同位素,同位素的研究对象为原子;
B.结构相似、分子间相差1个或n个CH2原子团的化合物之间互为同系物;
C.医用消毒酒精中乙醇的浓度为75%;
D.甲烷为正四面体结构,二溴甲烷不存在同分异构体.
解答 解:A.金刚石和石墨为C元素的不同单质,二者互为同素异形体,故A错误;
B.甲烷和异丁烷结构相似,分子间相差3个CH2原子团,二者互为同系物,故B正确;
C.乙醇浓度过大,使细胞壁脱水形成一层膜阻止进一步渗入,医用消毒酒精中乙醇的浓度为75%,故C错误;
D. 和
和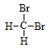 结构、分子组成完全相同,为同一种物质,故D错误;
结构、分子组成完全相同,为同一种物质,故D错误;
故选B.
点评 本题考查较为综合,涉及同位素、同系物、同分异构体等知识,题目难度不大,明确概念为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
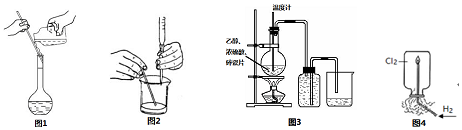
| A. | 如图1,向容量瓶中转移溶液 | |
| B. | 图2,用标准浓度的NaOH溶液滴定未知浓度的盐酸 | |
| C. | 图3,实验室用浓硫酸和乙醇共热制乙烯 | |
| D. | 图4,验证H2在Cl2中燃烧的实验现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴乙烷与氢氧化钠醇溶液共热,将产生的气体通入酸性高锰酸钾溶液中,溶液褪色,则可证明有乙烯产生 | |
| B. | 乙醇与钠的反应可以用启普发生器的简易装置来控制反应的发生和停止,实验室制乙炔 则不能使用该装置 | |
| C. | 检验淀粉在酸性条件下是否水解及水解的程度且只取一次水解液,可以先碱化水解 液,再加入银氨溶液并水浴加热,最后加入碘溶液 | |
| D. | 检验 3-氯丙炔中的氯原子,可以将其与氢氧化钠醇溶液共热后,加入足量稀硝酸酸化 后,再加入硝酸银溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{b-a}{2a-b}$ | B. | $\frac{a-b}{2b-a}$ | C. | $\frac{2a-b}{b-a}$ | D. | $\frac{2a+b}{b+a}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇分子的球棍模型为 | B. | 一氯甲烷的电子式为 | ||
| C. | 乙酸的结构简式:C2H4O2 | D. | 分子组成为C5H12的有机物有3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 原子半径(nm) | 0.075 | 0.110 | 0.152 | 0.071 | 0.186 | 0.099 |
| 最高价态 | +5 | +5 | +1 | 0 | +1 | +7 |
| 最低价态 | -3 | -3 | 0 | -1 | 0 | -1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com