
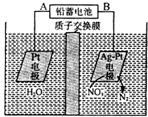
| A. | 铅蓄电池的A极为正极,电极材料为PbO2 | |
| B. | 铅蓄电池放电时负极质量增加 | |
| C. | 该电解池的阴极反应为:2NO3-+12H++10e-═N2↑十6H2O | |
| D. | 若电路中流过2 mol电子,则阳极室溶液质量减少32g(忽略气体的溶解) |
分析 铅蓄电池的正极材料为PbO2,负极为Pb,电解法处理含硝(NO3-)废水时,NO3-在阴极得电子生成氮气,阳极氢氧根离子失电子生成氧气,则Ag-Pt电极为阴极,所以B为负极,A为正极,据电子守恒和原子守恒解答.
解答 解:A、B为负极,A为正极,铅蓄电池的正极材料为PbO2,故A正确;
B、铅蓄电池的负极为铅失电子生成硫酸铅,硫酸铅是难溶电解质,所以负极质量增加,故B正确;
C、NO3-在阴极得电子生成氮气,阴极电极反应式为2NO3-+12H++10e-=N2+6H2O,故C正确;
D、阳极氢氧根离子失电子生成氧气式,阳极电极反应式为4OH--4e-=O2+2H2O,电路中流过2 mol电子,阳极生成0.5mol氧气,所以阳极室溶液质量减少32g/mol×0.5mol=16g,故D错误;
故选D.
点评 本题考查了原电池原理和电解原理的应用,注意根据得失电子来判断阴阳极上发生的反应,注意电子守恒在计算中的应用,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3-CH═CH-CH3 二丁烯 | B. | 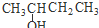 2-羟基丁烷 2-羟基丁烷 | ||
| C. | CH3OOCC2H5 乙酸乙酯 | D. | CH3CH(CH3)CH2COOH 3-甲基丁酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
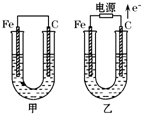 甲、乙两池电极材料都是铁棒与碳棒,两池中均为饱和NaCl溶液,请回答下列问题:
甲、乙两池电极材料都是铁棒与碳棒,两池中均为饱和NaCl溶液,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯与溴水混合振荡,水层颜色变浅 | |
| B. | 乙炔与氢气反应变成乙烷 | |
| C. | 乙烯与水在一定条件下反应制取乙醇 | |
| D. | 乙烯与HCl在一定条件下反应制取氯乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
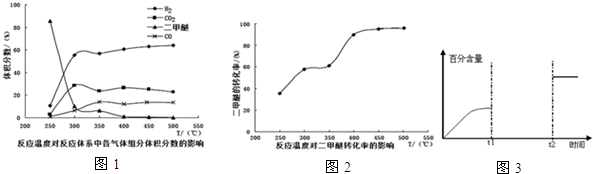
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molCO2的质量为44g/mol | |
| B. | H2SO4的摩尔质量为98 | |
| C. | 标准状况下,气体摩尔体积约为22.4L | |
| D. | O2的相对分子质量为32 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com