
 、②
、② 、③
、③ 、④
、④ ,设B的原子序数为x,当位置为①时,A的原子序数为x-1,C的原子序数为:x+8,则x+x-1+x+8=31,解得:x=8,则B为O元素、C为S元素、A为N元素;当位置关系为②时,A的原子序数为x+1、C的原子序数为x+8.则:x+x+1+x+8=31,3x=22,不符合;当位置关系为③时,C的原子序数为x-8、A的原子序数为x-1,则:x+x-8+x-1=31,3x=40,不符合条件;当位置关系为④时,A的原子序数为x+1、C的原子序数为x-8,则:x+x+1+x-8=31,3x=38,不符合条件,所以只有①满足条件,据此进行解答.
,设B的原子序数为x,当位置为①时,A的原子序数为x-1,C的原子序数为:x+8,则x+x-1+x+8=31,解得:x=8,则B为O元素、C为S元素、A为N元素;当位置关系为②时,A的原子序数为x+1、C的原子序数为x+8.则:x+x+1+x+8=31,3x=22,不符合;当位置关系为③时,C的原子序数为x-8、A的原子序数为x-1,则:x+x-8+x-1=31,3x=40,不符合条件;当位置关系为④时,A的原子序数为x+1、C的原子序数为x-8,则:x+x+1+x-8=31,3x=38,不符合条件,所以只有①满足条件,据此进行解答. 、②
、② 、③
、③ 、④
、④ ,设B的原子序数为x,当位置为①时,A的原子序数为x-1,C的原子序数为:x+8,则x+x-1+x+8=31,解得:x=8,则B为O元素、C为S元素、A为N元素;当位置关系为②时,A的原子序数为x+1、C的原子序数为x+8.则:x+x+1+x+8=31,3x=22,不符合;当位置关系为③时,C的原子序数为x-8、A的原子序数为x-1,则:x+x-8+x-1=31,3x=40,不符合条件;当位置关系为④时,A的原子序数为x+1、C的原子序数为x-8,则:x+x+1+x-8=31,3x=38,不符合条件,所以只有①满足条件,
,设B的原子序数为x,当位置为①时,A的原子序数为x-1,C的原子序数为:x+8,则x+x-1+x+8=31,解得:x=8,则B为O元素、C为S元素、A为N元素;当位置关系为②时,A的原子序数为x+1、C的原子序数为x+8.则:x+x+1+x+8=31,3x=22,不符合;当位置关系为③时,C的原子序数为x-8、A的原子序数为x-1,则:x+x-8+x-1=31,3x=40,不符合条件;当位置关系为④时,A的原子序数为x+1、C的原子序数为x-8,则:x+x+1+x-8=31,3x=38,不符合条件,所以只有①满足条件, ;C为S元素,其离子为硫离子,硫离子的核电荷数为16,其核外电子总数为18,硫离子结构示意图为:
;C为S元素,其离子为硫离子,硫离子的核电荷数为16,其核外电子总数为18,硫离子结构示意图为: ,
, ;
; ;
; ,
, .
.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 以下表及图中分别表示物质间的从属关系,其中不正确的是( )
以下表及图中分别表示物质间的从属关系,其中不正确的是( )| X | Y | Z | H | |
| A | 分散系 | 胶体 | 溶液 | 烟 |
| B | 电解质 | 酸 | 碱 | 含氧酸 |
| C | 氧化物 | 酸性氧化物 | 碱性氧化物 | 非金属氧化物 |
| D | 元素周期表的纵列 | 主族 | 副族 | 卤族 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①、②、③、⑤、⑥ |
| B、②、③、⑤、⑥ |
| C、②、③、⑤、⑥、⑦ |
| D、②、③、④、⑥、⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 常用于制备药物和合成高分子材料.(1)化合物Ⅰ的分子式为
常用于制备药物和合成高分子材料.(1)化合物Ⅰ的分子式为
 +CH3COOH→
+CH3COOH→ .聚合物可用于制备
.聚合物可用于制备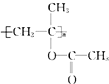
查看答案和解析>>
科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸有脱水性 |
| B | 将盐酸滴入Na2CO3溶液中 | 有气泡产生 | 氯的非金属性比碳强 |
| C | 向某溶液中加入浓NaOH溶液并加热,在试管口用湿润的红色石蕊纸检验 | 试纸变蓝 | 原溶液中含有NH4+ |
| D | SO2通入Ba(NO3)2溶液中 | 不会产生白色沉淀 | BaSO3溶于酸 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 下表中各组物质之间不能通过一步反应实现如图的是( )
下表中各组物质之间不能通过一步反应实现如图的是( ) | 甲 | 乙 | 丙 | |
| A | NaHCO3 | Na2CO3 | NaCl |
| B | SiO2 | HSiO3 | Na2SiO3 |
| C | Cl2 | HCl | CuCl2 |
| D | AlCl3 | Al(OH)3 | Al2O3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4HCO3溶于过量的浓KOH溶液中:NH4++HCO3-+2OH-=CO32-+NH3↑+2 H2O |
| B、向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH -=2 Al(OH)3↓+3BaSO4↓ |
| C、向FeBr2溶液中通入足量氯气:2Fe2++Cl2=2 Fe3++2 Cl- |
| D、醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com