
t℃时,某平衡体系中含有X、Y、Z、W四种物质,此温度下发生反应的平衡常数表达式为K= 。有关该平衡体系的说法正确的是( )
。有关该平衡体系的说法正确的是( )
A.当混合气体的平均相对分子质量保持不变时,反应达平衡
B.增大压强,各物质的浓度不变
C.升高温度,平衡常数K增大
D.增加X的量,平衡既可能正向移动,也可能逆向移动
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
汽车排放出的尾气主要是一氧化碳、一氧化氮、碳氢化合物等污染物。其中一氧化氮在空气中会生成二氧化氮,二氧化氮存在着一个可逆过程:2NO2(g)  N2O4(g) ΔH=Q kJ/mol。若将一定量的NO2(g)充入到一定温度下的某容积可变的密闭容器中,建立化学平衡,下列说法正确的是( )
N2O4(g) ΔH=Q kJ/mol。若将一定量的NO2(g)充入到一定温度下的某容积可变的密闭容器中,建立化学平衡,下列说法正确的是( )
A.若容积为某一固定值,当体系的压强不再发生变化时说明达到化学平衡状态
B.若上述可逆反应达化学平衡状态后,给平衡体系加压(缩小容积,其他条件不变),则容器内气体的平均摩尔质量将减小
C.若上述可逆反应达到化学平衡状态后,升高温度(其他条件不变)体系颜色加深,则Q>0
D.对于上述可逆过程给平衡体系减压(增大容积,其他条件不变),可以提高N2O4的产率
查看答案和解析>>
科目:高中化学 来源: 题型:
乳酸CHCH3OHCOOH是人体生理活动的一种代谢产物,以下是采用化学方法对乳酸进行加工处理的过程,其中A、H、G为链状高分子化合物

请回答下列问题:
(1)写出C、D的结构简式:C:________________;D:________________。
(2)从下述三个有机反应类型中选择② ⑥所属的类型(填代号):②________,⑥________。
A.取代反应 B.加成反应 C.消去反应
(3)写出下列反应的化学方程式
①_________________________________________________;
⑤_________________________________________________。
(4)作为隐形眼镜的制作材料,对其性能的要求除具有良好的光学性能外,还应具有良好的透气性和亲水性。一般采用E的聚合物G而不是D的聚合物H来制作隐形眼镜,其主要理由是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.凡是放热反应都是自发的,凡是吸热反应都是非自发的
B.自发反应一定是熵增大,非自发反应一定是熵减小或不变
C.自发反应在恰当条件下才能实现
D.自发反应在任何条件下都能实现
查看答案和解析>>
科目:高中化学 来源: 题型:
相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)  2NH3(g) ΔH=-92.6 kJ/mol。实验测得起始、平衡时的有关数据如下表:
2NH3(g) ΔH=-92.6 kJ/mol。实验测得起始、平衡时的有关数据如下表:
| 容器 编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量:23.15 kJ |
| ② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
下列叙述错误的是( )
A.容器①、②中反应的平衡常数相等
B.平衡时,两个容器中NH3的体积分数均为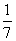
C.容器②中达平衡时放出的热量Q=23.15 kJ
D.若容器①体积为0.5 L,则平衡时放出的热量小于23.15 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
美国Bay等工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如下图:

(1)此流程的第Ⅱ步反应为:CO(g)+H2O(g)H2(g)+CO2(g),该反应的化学平衡常数表达式为K=________;反应的平衡常数随温度的变化如下表。
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
从上表可以推断:此反应是________(填“吸”“放”)热反应。
在830℃下,若开始时向恒容密闭容器中充入CO与H2O均为1 mol,则达到平衡后CO的转化率为__________。
(2)此流程的第 Ⅱ步反应CO(g)+H2O(g)
Ⅱ步反应CO(g)+H2O(g)  H2(g)+CO2(g),在830℃,以下表的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有__________(填实验编号)。
H2(g)+CO2(g),在830℃,以下表的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有__________(填实验编号)。
| 实验编号 | n(CO) | n(H2O) | n(H2) | n(CO2) |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 0.5 | 2 | 1 | 1 |
(3)在一个不传热的固定容积的容器中,判断此流程的第Ⅱ步反应达到平衡的标志是________(填序号)。
①体系的压强不再发生变化 ②混合气体的密度不变
③混合气体的平均相对分子质量不变 ④各组分的物质的量浓度不再改变 ⑤体系的温度不再发生变化
⑥v(CO2正)=v(H2O逆)
 (4)右图表示此流程的第Ⅱ步反应在时刻t1达到平衡、在时刻t2分别因改变某个条件而发生变化的情况:图中时刻t2发生改变的条件是__________(写出两种)。
(4)右图表示此流程的第Ⅱ步反应在时刻t1达到平衡、在时刻t2分别因改变某个条件而发生变化的情况:图中时刻t2发生改变的条件是__________(写出两种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是 ( )
A.Cl2通入水中:Cl2 + H2O = 2H+ + Cl- + ClO-
B.双氧水中加入稀硫酸和KI溶液:H2O2 + 2H+ + 2I- = I2 + 2H2O
C.浓硝酸中加入过量铁粉并加热:Fe+3NO +6H+
+6H+ Fe3++3NO2↑+3H2O
Fe3++3NO2↑+3H2O
D.Fe(OH)3溶于HI溶液:Fe(OH)3+3H+= Fe3++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子因发生氧化还原反应而不能大量共存的是
A.H+、Fe2+、Cr2O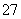 、SO
、SO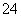
B.Ca2+、H+、SO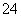 、HCO
、HCO
C.Na+、Cu2+、Cl-、S2-
D.Fe3+、K+、SCN-、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com