
 �����γɶ����������NO��NO2��N2O4�ȣ�NO2��N2O4�����ת����
�����γɶ����������NO��NO2��N2O4�ȣ�NO2��N2O4�����ת����| ʱ�䣨s�� | 0 | 20 | 40 | 60 | 80 |
| n��NO2��/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n��N2O4��/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
| ��c |
| ��t |
| [N2O4] |
| [NO2]2 |
| ������������� |
| ������������ʵ��� |
| ��c |
| ��t |
| ||
| 20s |
| 0.08 |
| 2 |
| 0.4 |
| 2 |
| 0.04 |
| 0.12��0.12 |
| c-0.04 |
| 0.12 |
| ������������ |
| �����������ʵ��� |
| 0.04mol��92g/mol+0.12mol��46g/mol |
| 0.04mol+0.12mol |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �����γɶ����������NO��NO2��N2O4�ȣ�
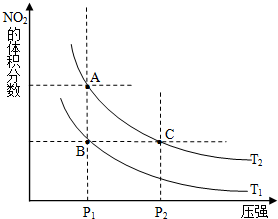
�����γɶ����������NO��NO2��N2O4�ȣ� 2NO2��g�������¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ����
2NO2��g�������¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ����| ʱ�䣨s�� | 0 | 20 | 40 | 60 | 80 |
| n��NO2��/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n��N2O4��/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
 N2O4��ƽ�ⳣ��K��
N2O4��ƽ�ⳣ��K���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �����γɶ����������NO��NO2��N2O4�ȣ�NO2��N2O4�����ת����
�����γɶ����������NO��NO2��N2O4�ȣ�NO2��N2O4�����ת����| ʱ�䣨s�� | 0 | 20 | 40 | 60 | 80 |
| n��NO2��/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n��N2O4��/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����γɶ����������NO��NO2��N2O4�ȡ���֪NO2��N2O4�Ľṹʽ�ֱ���![]() ��
�� ��ʵ����N��N������167kJ��mol��1��NO2�е�������ƽ������466 kJ��mol��1��N2O4�е�������ƽ������Ϊ438.5 kJ��mol��1��
��ʵ����N��N������167kJ��mol��1��NO2�е�������ƽ������466 kJ��mol��1��N2O4�е�������ƽ������Ϊ438.5 kJ��mol��1��
��1��д��N2O4ת��ΪNO2���Ȼ�ѧ����ʽ_________________________
��2���Է�ӦN2O4(g)![]() 2NO2(g)�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ����������������
2NO2(g)�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ����������������

A��A��C����ķ�Ӧ���ʣ�A��C
B��B��C����������ƽ����Է���������B��C
C��A��C�����������ɫ��A�Cdz
D����״̬B��״̬A�������ü��ȵķ���
��3����100��ʱ����0.400mol��NO2�������2 L��յ��ܱ������У�ÿ��һ��ʱ��ͶԸ������ڵ����ʽ��з������õ����±����ݣ�
| ʱ�䣨s�� | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
�������������£��ӷ�Ӧ��ʼֱ��20 sʱ������������ƽ����Ӧ����Ϊ_____mol��(L��s)-1��
��n3 ���� n4���>������<����=�������÷�Ӧ��ƽ�ⳣ��K��ֵΪ �������¶Ⱥ�Ӧ2NO2![]() N2O4��ƽ�ⳣ��K�� �����������С�����䡱����
N2O4��ƽ�ⳣ��K�� �����������С�����䡱����
��������ͬ����������������������N2O4���壬Ҫ�ﵽ����ͬ����ƽ��״̬��N2O4����ʼŨ����_____________mol��L��1��
�ܼ�����������´ﵽƽ����������ƽ����Է�������Ϊ____________�����������С�����һλ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011������ʡ��������ѧУ����������ģ�⿼�ԣ����ۣ���ѧ���� ���ͣ������
�����γɶ����������NO��NO2��N2O4�ȡ���֪NO2��N2O4�Ľṹʽ�ֱ��� ��
�� ��ʵ����N��N������167kJ��mol��1��NO2�е�������ƽ������466 kJ��mol��1��N2O4�е�������ƽ������Ϊ438.5 kJ��mol��1��
��ʵ����N��N������167kJ��mol��1��NO2�е�������ƽ������466 kJ��mol��1��N2O4�е�������ƽ������Ϊ438.5 kJ��mol��1��
��1��д��N2O4ת��ΪNO2���Ȼ�ѧ����ʽ_________________________
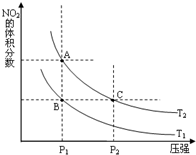
��2���Է�ӦN2O4(g) 2NO2(g)�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ����������������
2NO2(g)�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ����������������
A��A��C����ķ�Ӧ���ʣ�A��C
B��B��C����������ƽ����Է���������B��C
C��A��C�����������ɫ��A�Cdz
D����״̬B��״̬A�������ü��ȵķ���
��3����100��ʱ����0.400mol��NO2�������2 L��յ��ܱ������У�ÿ��һ��ʱ��ͶԸ������ڵ����ʽ��з������õ����±����ݣ�
| ʱ�䣨s�� | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
 N2O4��ƽ�ⳣ��K�� �����������С�����䡱����
N2O4��ƽ�ⳣ��K�� �����������С�����䡱�����鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com