
【题目】下列元素中,原子半径最大的是
A.NaB.AlC.KD.Cl
科目:高中化学 来源: 题型:
【题目】将氯气和空气(不参与反应)混合通入含水8%的碳酸钠中可以制备Cl2O气体,同时生成CO2。已知Cl2O易溶于水并与水反应生成HClO,现用下列装置制备 Cl2O,并用水吸收Cl2O(不含Cl2)制备次氯酸溶液。

(1)各装置的连接顺序为→→→C→_____________;
(2)写出 A 中反应的化学方程式_______________________________;
(3)装置 C 的作用是_____________;
(4)制备 Cl2O 的氧化还原反应中,Cl2的作用是_____________;
(5)已知次氯酸可被H2O2、FeCl2等物质还原成Cl-。测定E中次氯酸溶液的物质的量浓度的实验方案为:取20.00 mL次氯酸溶液,加入足量的_____________,再加入足量的_____________,过滤,洗涤沉淀,在真空干燥箱中干燥,用电子天平称量沉淀质量为a g,则E中次氯酸的浓度为_____________mol·L-1。 (可选用的试剂:H2O2溶液、FeCl2溶液、AgNO3溶液)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁四种易溶于水的物质,分别由NH4+、Ba2+、Mg2+、H+、OH-、Cl-、CO32-、SO42-中的不同阳、阴离子各一种组成已知:
①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;
②0.1mol/L乙溶液中c(H+)>0.1mol/L;
③向丙容器中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成。
(1)甲是_____________,乙是_____________,丙是_____________,丁是_____________。
(2)50mL含Na2SO4、Na2CO3的混合溶液中加入过量的甲溶液,得到14.51g白色沉淀,向白色沉淀中加入过量的稀HNO3充分反应后,沉淀减少到4.66g,并有气体产生。
①写出产生气体的离子方程式:______________________________;
②混合溶液中Na+的物质的量的浓度是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如图中四个图像的说法正确的是
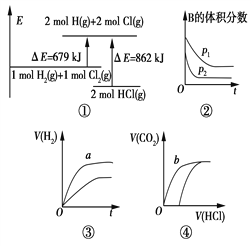
注:图中,E表示能量,p表示压强,t表示时间,y表示体积。
A. ①表示化学反应H2(g)+Cl2(g)===2HCl(g)的能量变化,则该反应的反应热ΔH=183 kJ/mol
B. ②表示其他条件不变时,反应4A(g)+3B(g) ![]() 2C(g)+6D在不同压强下B的体积分数随时间的变化,则D一定是非气体。
2C(g)+6D在不同压强下B的体积分数随时间的变化,则D一定是非气体。
C. ③表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示HCl溶液。
D. ④表示10 mL 0.1 mol/L Na2CO3和NaHCO3两种溶液中,分别滴加0.1 mol/L盐酸,产生CO2的体积随盐酸体积的变化,则b表示Na2CO3溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )

A. HA为强酸 B. 该混合液pH=7
C. 图中X表示HA,Y表示OH-,Z表示H+ D. 该混合溶液中:c(A—)+ c(Y)=c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿魏酸是用于治疗心脑血管疾病及白细胞减少等症药品的基本原料。下面是以石炭酸为原料制备阿魏酸的一种合成路线:
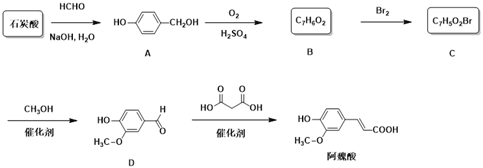
(1)由石炭酸生成A和A生成B的反应类型分别为____、______。
(2)阿魏酸有顺式和反式两种结构,其顺式结构的结构简式为________。
(3)C中官能团名称为__________。
(4)由B生成C的化学反应方程式为___________________。
(5)芳香化合物E是D的同分异构体,0.1 mol E能与饱和碳酸氢钠溶液反应放出4.4g CO2,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为2∶2∶1∶3,写出符合要求的E的结构简式____________。
(6)由谷维素(![]() )也可制备阿魏酸,请设计简单的合成路线并写出相应的化学反应方程式_________。
)也可制备阿魏酸,请设计简单的合成路线并写出相应的化学反应方程式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“飘尘”是物质燃烧时产生的粒子漂浮物,颗粒很小(直径小于10-7m),不易沉降(可漂浮数小时或数年),它与空气中SO2、O2接触时,SO2部分转化为SO3,使空气酸度增加,形成酸雨。
(1)飘尘所起的主要作用是____。
A.氧化剂 B.催化剂 C.吸附剂 D.还原剂
(2)与雨水形成酸雨,试写出这两个化学反应式:_____________。
(3)汽车排放的尾气、硝酸厂和化肥厂的废气含有氮氧化物,全世界每年排放量约5×107kgNO2溶于水生成___________酸。
(4)酸雨可导致下列哪种危害____。
A.腐蚀建筑物 B.导致树木枯萎
C.造成洪涝灾害 D.恶化人类环境
(5)人体中纯净的胃液是一种强酸性液体,pH在0.9---1.5之间。氢氧化铝是一种治疗胃酸过多的胃药主要成分,目前这种胃药已不常用,主要原因是____。
A.它不能中和胃酸 B.它的疗效太差
C.长期摄入铝元素不利于身体健康 D.它不易溶于胃酸
(6)制造焊锡时,把铅加入锡的主要原因是____。
A.增加抗腐蚀能力 B.降低熔点
C.增加延展性 D.增加硬度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com