
现有A、B、C、D、E、F六种短周期元素,原子序数依次增大。已知A与D、C与E分别同主族,D、E、F同周期;A、B的最外层电子 数之和与C的最外层电子数相等,A与C形成的化合物常温下均为液态,A分别与E、F形成的气体分子电子总数相等。
数之和与C的最外层电子数相等,A与C形成的化合物常温下均为液态,A分别与E、F形成的气体分子电子总数相等。
请回答下列问题:
(1)元素B在周期表中的位置是_____________________,元素D的原子结构示意图为____ ____。
(2)A2C比A2E沸点高的原因是________________________________________________。
(3)在一定条件下,A、C的单质和A、C、D形成的离子化合物的水溶液可构成电池,该电池正极的电极反应式为________________________,负极的电极反应式为______________________,该电池在放电过程中,电解质溶液的pH将________(填“增大”、“减小”或“不变”)。
(4)化合物B2A4和B2C4的液体曾被用作火箭推进剂,燃烧反应的生成物是一种气态单质和一种化合物,它们对环 境无污染。1 mol B2A4与B2C4完全反应生成两种气体时放出热量516.8 kJ,则该反应的热化学方程式为________________________________________________________________。
境无污染。1 mol B2A4与B2C4完全反应生成两种气体时放出热量516.8 kJ,则该反应的热化学方程式为________________________________________________________________。
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
下列涉及有机物的说法正确的是( )
A.乙烯和聚乙烯都能发生加聚反应
B.汽油、煤油、柴油和植物油都是碳氢化合物
C.乙烯、苯都可与溴水发生加成反应
D.2己烯能使KMnO4(H+)溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
乙醇燃料电池中采用磺酸类质子溶剂,在一定温度下供电,电池总反应为C2H5OH+3O2===2CO2+3H2O,电池示意图如图。下列说法中错误的是 ( )
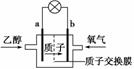
A.电池工作时,质子向电池的正极迁移
B.电池工作时,电流由b极沿导线流向a极
C.a极上发生的电极反应是C2H5OH+3H2O+12e-===2CO2+12H+
D.b极上发生的电极反应是4H++O2+4e-===2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能作为实验判断依据的是
A.钠和镁分别与冷水反应,判断金属活动性强弱
B.铁投入CuSO4溶液中,能置换出铜,钠投入CuSO4溶液中不能置换出铜,判断钠与铁的金属活动性强弱
C.酸性H2CO3<HCl,判断氯与碳的非金属活动性强弱
D.Br2与I2分别与足量的H2反应的难易,判断溴与碘的非金属活动性强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是稀硫酸与某金属反应的实验数据:
| 实验序号 | 金属质量 | 金属状态 | c(H2SO4) /mol·L-1 | V(H2SO4) /mL | 溶液温度/℃ | 金属消失的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 丝 | 0.5 | 50 | 20 | 34 | 500 |
| 2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
| 3 | 0.10 | 丝 | 0.7 | 50 | 20 | 36 | 250 |
| 4 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
| 5 | 0.10 | 粉末 | 0.8 | 50 | 20 | 36 | 25 |
| 6 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 125 |
| 7 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 | 50 |
| 8 | 0.10 | 丝 | 1.1 | 50 | 20 | 34 | 100 |
| 9 | 0.10 | 丝 | 1.1 | 50 | 30 | 44 | 40 |
分析上述数据,回答下列问题:
(1)实验4和5表明,________________对反应速率有影响,______________反应速率越快,能表明同一规律的实验还有__________(填实验序号);
(2)实验1、3、4、6、8表明反应物浓度对反应速率产生影响,能表明同一规律的实验还有______________(填实验序号);
(3)本实验中影响反应速率的其他因素还有________,其实验序号是6和________,8和__________。
(4)实验中的所有反应,反应前后溶液的温度变化值(约15℃)相近,推测其原因:____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质的性质和该性质的应用均正确的是
A.铜的金属活泼性比铁的差,可在海轮外壳上装若干铜块以减缓其腐蚀
B.二氧化硅不与任何酸反应,可用石英制造耐酸容器
C.常温下浓硫酸能与铝发生钝化,可在常温下用铝制贮藏贮运浓硫酸
D. 二氧化氯具有还原性,可用于自来水的杀菌消毒
| |
查看答案和解析>>
科目:高中化学 来源: 题型:
现有A、B、C、D、E、F、G、H八种短周期主族元素,原子序数依次增大。已知A与E、D与G分别同主族;E、F、G、H同周期;A分别与C、D可形成含有10个电子的共价化合物M、N;B的最外层电子数是其电子层数的2倍;D是地壳中含量最多的元素;F位于B的前一主族。请回答下列问题:
(1)元素B在周期表中的位置 ,M的空间构型是 。
(2)A、D、E三种元素组成一种常见化合物,W与该化合物的阴离子具有相同的原子种类和数目且不带电,W的电子式为 ,工业上利用某一个反应可同时生产该化合物和H的单质,写出该反应的化学方程式 。
(3)E、F元素的最高价氧化物对应的水化物之间反应的离子方程式 。
(4)M、N均能结合H+,其中结合H+能力较强的是 (填化学式)。N结合H+所形成的微粒中心原子采用 杂化。其键角比N中的键角大,原因为 。
(5)E分别与D、G形成摩尔质量相等的化合物X、Y,其中Y的水溶液显碱性的原因是
(用离子方程式表示)。常温下7.8 g X与水反应放出Q kJ热量(Q>0),写出该反应的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于乙醇的说法中正确的是( )
A.乙醇结构中有—OH,所以乙醇溶解于水,可以电离出OH-而显碱性
B.乙醇燃烧生成二氧化碳和水,说明乙醇具有氧化性
C.乙醇与钠反应可以产生氢气,所以乙醇显酸性
D.乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com