
【题目】常温下,将等浓度的NaOH溶液分别滴加到等pH、等体积的HA、HB两种弱酸溶液中,溶液的pH与粒子浓度比值的对数关系如图所示。下列叙述错误的是( )

A. a点时,溶液中由水电离的c(OH-)约为1×10-10 mol·L-1
B. 电离平衡常数:Ka(HA)< Ka(HB)
C. b点时,c(B-)=c(HB)>c(Na+)>c(H+)>c(OH-)
D. 向HB溶液中滴加NaOH溶液至pH=7时:c(B-)> c(HB)
【答案】B
【解析】
A. a点时,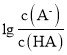 =0,c(A-)=c(HA),溶液为酸和盐的溶合溶液,pH=4,抑制水的电离,溶液中由水电离的c(OH-)约为1×10-10 mol·L-1,选项A正确;
=0,c(A-)=c(HA),溶液为酸和盐的溶合溶液,pH=4,抑制水的电离,溶液中由水电离的c(OH-)约为1×10-10 mol·L-1,选项A正确;
B. 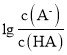 =0,c(A-)=c(HA),电离平衡常数:Ka(HA)=
=0,c(A-)=c(HA),电离平衡常数:Ka(HA)=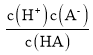 =
=![]() =10-4mol/L;
=10-4mol/L;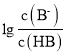 =0,c(B-)=c(HB),电离平衡常数:Ka(HB)=
=0,c(B-)=c(HB),电离平衡常数:Ka(HB)=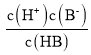 =
=![]() =10-5mol/L,Ka(HA)> Ka(HB),选项B错误;
=10-5mol/L,Ka(HA)> Ka(HB),选项B错误;
C. b点时,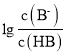 =0,c(B-)=c(HB),pH=5,c(B-)=c(HB)>c(Na+)>c(H+)>c(OH-),选项C正确;
=0,c(B-)=c(HB),pH=5,c(B-)=c(HB)>c(Na+)>c(H+)>c(OH-),选项C正确;
D. 向HB溶液中滴加NaOH溶液至pH=7时,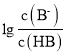 >0,c(B-)> c(HB),选项D正确。
>0,c(B-)> c(HB),选项D正确。
答案选B。


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
【题目】如图两种化合物的结构或性质描述正确的是
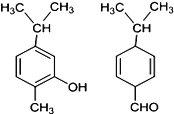
A. 两种化合物均是芳香烃
B. 两种化合物可用红外光谱区分,但不能用核磁共振氢谱区分
C. 两种化合物分子中共平面的碳原子数相同
D. 两种化合物互为同分异构体,均能与溴水反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用两支惰性电极插入50mLAgNO3溶液中,通电电解。当电解液的PH值从6.0变为3.0时(设电解时阴极没有氢气析出,且电解液在电解前后体积变化可以忽略),电极上析出银的质量大约是:
A. 27mg B. 54mg C. 108mg D. 216mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示的三个烧杯中均盛有足量的氯化铜溶液。请按要求回答下列问题:
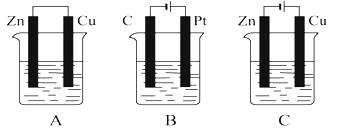
(1)![]() 、
、![]() 、
、![]() 三个装置中不属于电解池的是______。
三个装置中不属于电解池的是______。
(2)![]() 池中
池中![]() 是______极,
是______极,![]() 池中
池中![]() 移向______极(填“
移向______极(填“![]() ”或“
”或“![]() ”)。
”)。
(3)![]() 池中
池中![]() 电极上发生反应__________(填“氧化”或“还原”)
电极上发生反应__________(填“氧化”或“还原”)
(4)![]() 池中
池中![]() 电极上的电极反应为______,反应过程中
电极上的电极反应为______,反应过程中![]() ______(填“变大”“变小”或“不变”)
______(填“变大”“变小”或“不变”)
(5)![]() 池中总反应的化学方程式为______
池中总反应的化学方程式为______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】采用湿法冶金工艺回收废旧光盘中的金属Ag(其他金属因微量忽略不计),其流程如下:
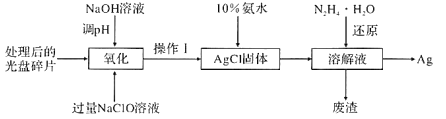
回答下列问题:
(1)①“操作I”为_____,在实验室进行此操作需要用到的玻璃仪器有_____。
②在实验室利用“操作I”的装置洗涤难溶物的操作方法是_______。
(2)若NaClO溶液与Ag反应的产物有AgCl和O2,则该反应的化学方程式为____若以稀HNO3代替NaClO溶液,其缺点是___(写出一条即可)。
(3)已知Ag2O在酸性条件下能将有毒气体甲醛(HCHO)氧化成CO2,科学家据此原理将上 述过程设计为一种电化学装置,以回收电极材料中的金属Ag。则此电池的正极反应式为_____。
(4)已知室温时,Ksp(Ag2SO4)=1.4×10-5,Ksp(AgCl)=1.8×10-10。计算反应Ag2SO4(s)+2Cl-(aq) ![]() 2AgCl(s)+SO42- (aq)的平衡常数K=_____。(保留两位有效数字)
2AgCl(s)+SO42- (aq)的平衡常数K=_____。(保留两位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备叔丁基苯(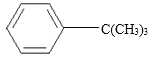 )的反应和有关数据如下:
)的反应和有关数据如下:
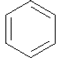 +ClC(CH3)3
+ClC(CH3)3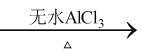
 +HCl
+HCl
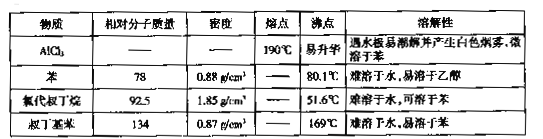
I.如图是实验室制备无水AlCl3,可能需要的装置:
(1)检查B装置气密性的方法是_______。
(2)制备无水AlCl3的装置依次合理的连接顺序为__________(埴小写字母),其中E装置的作用是________。
(3)实验时应先加热圆底烧瓶再加热硬质玻璃管,其原因是________。
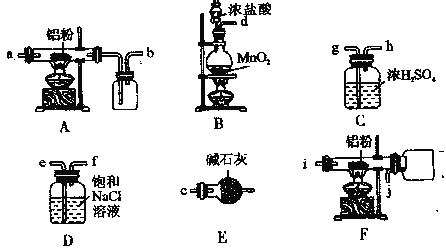
Ⅱ.如图是实验室制备叔丁基苯的装置(夹持装置略):
在三颈烧瓶中加入50 mL的苯和适量的无水AlCl3,由恒压漏斗滴加氯代叔丁烷10mL,一定温度下反应一段时间后,将反应后的混合物洗涤分离,在所得产物中加入少量无水MgSO4固体,静置,过滤,蒸馏得叔丁基苯20g。
(4)使用恒压漏斗的优点是_______;加入无水MgSO4固体的作用是________。
(5)洗涤混合物时所用的试剂有如下三种,正确的顺序是________。(填序号)
①5%的Na2CO3溶液 ②稀盐酸 ③H2O
(6)本实验中叔丁基苯的产率为______。(保留3位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物I是一种抗脑缺血药物,合成路线如下:
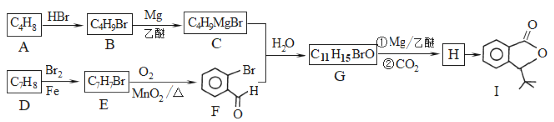
已知:
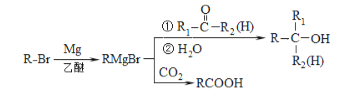
回答下列问题:
(1)按照系统命名法,A的名称是_____;写出A发生加聚反应的化学方程式:__________。
(2)反应H→I的化学方程式为________;反应E→F的反应类型是______。
(3)写出符合下列条件的G的所有同分异构体的结构简式:________
①遇FeCl3溶液发生显色反应 ②核磁共振氢谱有4组峰
(4)α,α-二甲基苄醇(![]() )是合成医药、农药的中间体,以苯和2-氯丙烷为起始原料制备α,α-二甲基苄醇的合成路线如下:
)是合成医药、农药的中间体,以苯和2-氯丙烷为起始原料制备α,α-二甲基苄醇的合成路线如下:

该合成路线中X的结构简式为____,Y的结构简式为________;试剂与条件2为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究电化学原理与应用有非常重要的意义。
(1)锌锰电池(俗称干电池) 是一种一次电池,生活中应用广泛。
①锌锰电池负极上的电极反应式为:______________________________。
②与普通(酸性)锌锰电池相比较,碱性锌锰电池的优点是____________________(回答一条即可)。
(2)铅蓄电池是最常见的二次电池:Pb+PbO2+2H2SO4 ![]() 2PbSO4+2H2O。
2PbSO4+2H2O。
①充电时阴极反应为:________________________________________。
②用铅蓄电池为电源进行电解饱和食盐水实验(石墨棒为阳极,铁为阴极,食盐水500mL,温度为常温),当电路中有0.05mol电子转移时,食盐水的PH为______(假设溶液体积不变,产物无损耗)。
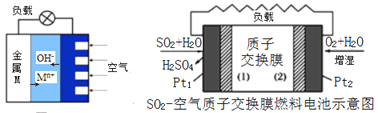
(3)如图是金属(M)-空气电池的工作原理,我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,电池反应为:___________________________ 。二氧化硫—空气质子交换膜燃料电池实现了制硫酸、发电、环保三位一体的结合,原理如图所示。Pt2上的电极反应式为:_______________________________________ 。
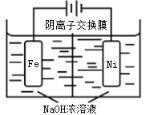
(4)高铁酸钠(Na2FeO4)易溶于水,是一种新型多功能水处理剂,可以用电解法制取:Fe+2H2O+2OH![]() FeO42+3H2↑,工作原理如图所示。装置通电后,铁电极附近生成紫红色的FeO42,镍电极有气泡产生。电解一段时间后,c(OH)降低的区域在_____________(填“阴极室”或“阳极室”);阳极反应为:___________________________。
FeO42+3H2↑,工作原理如图所示。装置通电后,铁电极附近生成紫红色的FeO42,镍电极有气泡产生。电解一段时间后,c(OH)降低的区域在_____________(填“阴极室”或“阳极室”);阳极反应为:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(s)+3B(g)![]() 2C(g)+D(g)经2min后,B的浓度减少了0.6mol·L-1。下列说法正确的是( )
2C(g)+D(g)经2min后,B的浓度减少了0.6mol·L-1。下列说法正确的是( )
A.用A表示的化学反应速率是0.4mol·L-1·min-1
B.分别用B、C、D表示化学反应速率,其比是3∶2∶1
C.在2min末的反应速率用B表示是0.3mol·L-1·min-1
D.在这2min内B和C两物质的浓度都减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com