
 ;该物质遇水剧烈反应,产生有刺激性气味的混合气体X和Y,同时还有固体单质产生,是已知X能使品红溶液褪色的气体,Y在标准状态下的密度为1.63g/L,该混合气体相对于H2的密度为21,上述过程对应的化学方程式为2S2Cl2+2H2O=SO2↑+4HCl+3S↓;某研究小组同学为确定干燥的X和Y混合气体中Y的存在,设计方案如下:把干燥的X和Y与干燥的NH3混合,出现白烟,则证明有Y气体,你认为此方案正确(填“正确”或“不正确”),理由是干燥的二氧化硫不与氨气反应,但干燥的氯化氢与氨气反应生成白烟.
;该物质遇水剧烈反应,产生有刺激性气味的混合气体X和Y,同时还有固体单质产生,是已知X能使品红溶液褪色的气体,Y在标准状态下的密度为1.63g/L,该混合气体相对于H2的密度为21,上述过程对应的化学方程式为2S2Cl2+2H2O=SO2↑+4HCl+3S↓;某研究小组同学为确定干燥的X和Y混合气体中Y的存在,设计方案如下:把干燥的X和Y与干燥的NH3混合,出现白烟,则证明有Y气体,你认为此方案正确(填“正确”或“不正确”),理由是干燥的二氧化硫不与氨气反应,但干燥的氯化氢与氨气反应生成白烟. 分析 原子序数依次增大的A、B、C、D、E五种位于不同短周期的元素,只有C为金属元素,焰色反应呈黄色,则C为Na;
由(4)中C、D可以形成化合物C2D,则D为-2价,处于ⅥA族,原子序数大于Na,故D为S元素,化合物C2D溶液在空气中长期放置会变质生成丙C2D2,故丙为Na2S2;由于E的原子序数大于硫,故E为Cl;
由(2)中B和D形成的化合物甲其相对分子质量在170~190之间,且D的质量分数约为70%,则甲分子中S原子数目:$\frac{190×70%}{32}$>N(S)>$\frac{170×70%}{32}$,则N(S)=4,则Mr(甲)=$\frac{4×32}{70%}$≈183,B原子相对原子质量为$\frac{183-4×32}{4}$≈14,故B为N元素,则甲为N4S4;
由(3)A和B形成的化合物乙为B4A4,在一定条件下可以电离出两种离子,其中一种为10e-的离子,则A为H元素,乙为N4H4;
(5)D和E形成的化合物丁中所有原子均满足8电子稳定结构,S原子最外层需要2个电子,Cl原子最外层需要1个电子,则D为S2Cl2;
该物质遇水剧烈反应,产生有刺激性气味的混合气体X和Y,同时还有固体单质产生,固体单体为S,X能使品红溶液褪色的气体,Y在标准状态下的密度为1.63g/L,Mr(Y)=1.63×22.4=36.5,则X为SO2、Y为HCl,该混合气体相对于H2的密度为21,混合气体平均相对分子质量为42,由十字交叉法可知,SO2、HCl的物质的量之比为(42-36.5):(64-42)=1:4,进而配平书写化学方程式;
干燥的二氧化硫不与氨气反应,但干燥的氯化氢与氨气反应.
解答 解:原子序数依次增大的A、B、C、D、E五种位于不同短周期的元素,只有C为金属元素,焰色反应呈黄色,则C为Na;
由(4)中C、D可以形成化合物C2D,则D为-2价,处于ⅥA族,原子序数大于Na,故D为S元素,化合物C2D溶液在空气中长期放置会变质生成丙C2D2,故丙为Na2S2;由于E的原子序数大于硫,故E为Cl;
由(2)中B和D形成的化合物甲其相对分子质量在170~190之间,且D的质量分数约为70%,则甲分子中S原子数目:$\frac{190×70%}{32}$>N(S)>$\frac{170×70%}{32}$,则N(S)=4,则Mr(甲)=$\frac{4×32}{70%}$≈183,B原子相对原子质量为$\frac{183-4×32}{4}$≈14,故B为N元素,则甲为N4S4;
由(3)A和B形成的化合物乙为B4A4,在一定条件下可以电离出两种离子,其中一种为10e-的离子,则A为H元素,乙为N4H4;
由(5)D和E形成的化合物丁中所有原子均满足8电子稳定结构,S原子最外层需要2个电子,Cl原子最外层需要1个电子,则D为S2Cl2.
(1)由上述分析可知,E为Cl元素,处于周期表中第三周期ⅦA族,故答案为:第三周期ⅦA族;
(2)由上述分析可知,甲的化学式为:N4S4,故答案为:N4S4;
(3)乙为N4H4,在一定条件下可以电离出两种离子,其中一种为10e-的离子,应为NH4+,另外的阴离子为N3-,故电离方程式为:N4H4=NH4++N3-,
故答案为:N4H4=NH4++N3-;
(4)化合物Na2S溶液在空气中长期放置会变质生成Na2S2,反应中S元素化合价升高,只能是氧元素化合价降低,应有NaOH生成,反应方程式为:4Na2S+O2+2H2O=4NaOH+2Na2S2,
故答案为:4Na2S+O2+2H2O=4NaOH+2Na2S2;
(5)D和E形成的化合物丁中所有原子均满足8电子稳定结构,S原子最外层需要2个电子,Cl原子最外层需要1个电子,则D为S2Cl2,分子中S原子之间形成1对共用电子对,S原子与Cl之间形成1对共用电子对,电子式为: ;
;
该物质遇水剧烈反应,产生有刺激性气味的混合气体X和Y,同时还有固体单质产生,固体单体为S,X能使品红溶液褪色的气体,Y在标准状态下的密度为1.63g/L,Mr(Y)=1.63×22.4=36.5,则X为SO2、Y为HCl,该混合气体相对于H2的密度为21,混合气体平均相对分子质量为42,由十字交叉法可知,SO2、HCl的物质的量之比为(42-36.5):(64-42)=1:4,反应方程式为:2S2Cl2+2H2O=SO2↑+4HCl+3S↓;
干燥的二氧化硫不与氨气反应,但干燥的氯化氢与氨气反应生成白烟,故实验方案正确,
故答案为: ;2S2Cl2+2H2O=SO2↑+4HCl+3S↓;干燥的二氧化硫不与氨气反应,但干燥的氯化氢与氨气反应生成白烟.
;2S2Cl2+2H2O=SO2↑+4HCl+3S↓;干燥的二氧化硫不与氨气反应,但干燥的氯化氢与氨气反应生成白烟.
点评 本题考查元素化合物推断,注意充分利用问题中的信息进行分析解答,涉及物质均不是中学常见物质,题目问题的设计也没有承前启后性,增大题目难度,侧重考查学生综合运用知识的能力,难度较大.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 丙烷和丁烷互为同系物 | |
| B. | 丙烯和丁烯互为同系物 | |
| C. | 丙烷和丁烷中碳元素的质量分数相同 | |
| D. | 丙烯和丁烯中碳元素的质量分数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
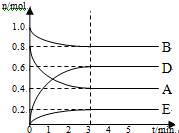 某温度T℃下,在某个固定容积为2.0L的密闭容器内,在时按右图所示发生反应:其中A、B、D为气体,E为固体.
某温度T℃下,在某个固定容积为2.0L的密闭容器内,在时按右图所示发生反应:其中A、B、D为气体,E为固体.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH均为4的H2SO4、NH4Cl溶液中,水的电离程度相同 | |
| B. | 等pH的NaOH溶液与NH3•H2O 稀释后pH的变化如右图所示,则曲线I表示的是NaOH溶液的稀释 | |
| C. | 1mol/LNa2CO3溶液中存在:c(Na+)=2c(CO32- )+2c(HCO3-) | |
| D. | 向某温度的氨水中通入盐酸,则氨水的电离常数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
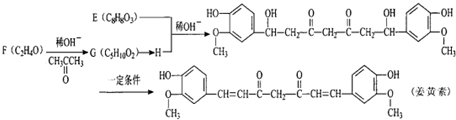
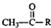 $\stackrel{稀OH-}{→}$
$\stackrel{稀OH-}{→}$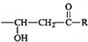
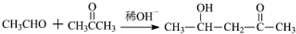 ,G→H的反应类型为氧化反应
,G→H的反应类型为氧化反应 ;将F滴人新制Cu(OH)2悬浊液,加热,观察到的现象是出现红色沉淀
;将F滴人新制Cu(OH)2悬浊液,加热,观察到的现象是出现红色沉淀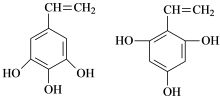
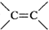
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将草木灰和硫铵混合使用,相当于施用了氮和钾的复合肥料,提高了肥料利用率 | |
| B. | 铝制容器不能长期盛装酸性或碱性食品,但可用于长期盛放腌制食品 | |
| C. | 氟里昂(CCl2F2)或NOx都可以破坏臭氧层,从而导致了“温室效应” | |
| D. | 大量使用含磷洗涤剂,可导致水体富营养化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 欲粗略测定某未知浓度的醋酸溶液中醋酸的电离常数Ka,应做的实验和所需的试剂(或试纸)为:中和滴定实验、pH试纸 | |
| B. | 将0.1mol/L的NaOH溶液与0.5mol/L的CuSO4溶液等体积混合制得氢氧化铜悬浊液,用于检验麦芽糖是还原性糖 | |
| C. | 在密闭容器中加入1.5mol H2和0.5mol N2充分反应可得到NH3分子数为NA | |
| D. | 标准状况下,33.6L二氯甲烷中含有氯原子的数目为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com