
| ���� | NaF | NaClO | Na2CO3 |
| pH | 7.5 | 9.7 | 11.6 |
| A�� | �����ϱ���������NaClO��Һ��ͨ��CO2��CO2+H2O+2ClO���T2HClO+CO32- | |
| B�� | ������ NaClO��Һ��ͨHF������ǡ����ȫ��Ӧʱ��c��Na+����c��F-����c��HClO�� | |
| C�� | ����ͬ�¶��£�ͬŨ�ȵ���������Һ�ĵ�������˳��H2CO3��HClO��HF | |
| D�� | ����CO2ͨ��0.1mol•L-1Na2CO3��Һ������Һ���ԣ�����Һ��2c��CO32-��+c ��HCO3-��=0.1 mol•L-1 |
���� ��Ũ�ȵ���Һ�У��ε�ˮ������Խǿ��������Һ��pHԽ��Ӧ���������Խ�����������ԣ�HF��H2CO3��HClO��HCO3-��
A������ǿ�������Ʊ��������ģ�
B��NaClO��Һ��ͨHF��������HClO��NaF��
C����ͬŨ��ʱ����Խǿ����Һ������Ũ��Խ��������Խǿ��
D�����ݵ���غ�������غ������
��� �⣺��Ũ�ȵ���Һ�У��ε�ˮ������Խǿ��������Һ��pHԽ��Ӧ���������Խ�����������ԣ�HF��H2CO3��HClO��HCO3-��
A��������NaClO��Һ��ͨ��CO2����HClO��̼�����ƣ��䷴Ӧ���ӷ���ʽΪ��CO2+H2O+ClO-�THClO+HCO3-����A����
B��NaClO��Һ��ͨHF��������HClO��NaF��HClO������������Һ�в��ֵ��룬����c��Na+����c��F-����c��HClO������B��ȷ��
C����ͬŨ��ʱ����Խǿ����Һ������Ũ��Խ��������Խǿ�����ԣ�HF��H2CO3��HClO����������ͬ�¶��£�ͬŨ�ȵ���������Һ�ĵ�������˳��HF��H2CO3��HClO����C����
D����Һ�����ԣ������c��H+��=c��OH-�����κε������Һ�ж����ڵ���غ�������غ㣬���ݵ���غ��2c��CO32-��+c��HCO3-��=c��Na+��=0.2mol•L-1����ѡD����
��ѡB��
���� ���⿼�����ε�ˮ�⡢����ϵĶ����жϼ���ҺpH�ļ��㣬��Ŀ�Ѷ��еȣ�ע��������Һ���������ҺpH�Ĺ�ϵ�����㷽��������������ѧ���ķ�����������ѧ����������


 �����ܿ����ϵ�д�
�����ܿ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
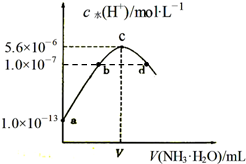 �����£���20mLijŨ�ȵ�������Һ�е���0.1mol•L-1��ˮ����Һ��ˮ�����������Ũ������백ˮ������仯��ͼ�����з�����ȷ���ǣ�������
�����£���20mLijŨ�ȵ�������Һ�е���0.1mol•L-1��ˮ����Һ��ˮ�����������Ũ������백ˮ������仯��ͼ�����з�����ȷ���ǣ�������| A�� | ��ͼ��֪ϡ�����Ũ��Ϊ0.1 mol•L-1 | |
| B�� | b����ҺpH=7 | |
| C�� | c����ʾ��Һ�У�c��SO42-����c��NH4+����c��H+����c��OH-�� | |
| D�� | d����ʾ��Һ�У�c��NH4+��=2c��SO42-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
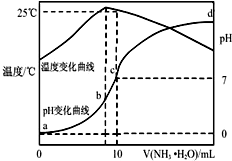 ��ij�¶�ʱ����nmol•L-1��ˮ����10mL1.0mol•L-1�����У���ҺpH���¶�����백ˮ����仯������ͼ��ʾ�������й�˵����ȷ���ǣ�������
��ij�¶�ʱ����nmol•L-1��ˮ����10mL1.0mol•L-1�����У���ҺpH���¶�����백ˮ����仯������ͼ��ʾ�������й�˵����ȷ���ǣ�������| A�� | a��Kw=1.0��10-14 | |
| B�� | 25��ʱNH4Clˮ�ⳣ��Ϊ����n-1����10-7mol•L-1����n��ʾ�� | |
| C�� | b�㣺c��NH4+����c��Cl-����c��H+����c��OH-�� | |
| D�� | ˮ�ĵ���̶ȣ�b��c��a��d |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
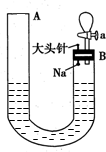 ��ͼ���й�����ˮ��Ӧ����������ʵ��װ�ã�ʵ�鿪ʼʱ������ڼ�����з�̪��ˮ��ʹˮλ�ﵽB�˹ܿڣ�Ȼ��Ѹ�������������ε���ͷ�룬��ʱNa����ˮ�У��ش��������⣺
��ͼ���й�����ˮ��Ӧ����������ʵ��װ�ã�ʵ�鿪ʼʱ������ڼ�����з�̪��ˮ��ʹˮλ�ﵽB�˹ܿڣ�Ȼ��Ѹ�������������ε���ͷ�룬��ʱNa����ˮ�У��ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
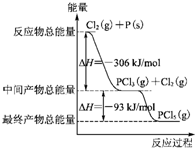 ����P��s����Cl2������Ӧ����PCl3��PCl5����Ӧ���̺�������ϵ����ͼ��ʾ��ͼ�еġ�H��ʾ����1mol��������ݣ�������ͼ�ش��������⣺
����P��s����Cl2������Ӧ����PCl3��PCl5����Ӧ���̺�������ϵ����ͼ��ʾ��ͼ�еġ�H��ʾ����1mol��������ݣ�������ͼ�ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͨ��CO2 | B�� | ͨ��NH3 | C�� | ��ȴĸҺ | D�� | ����ʳ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
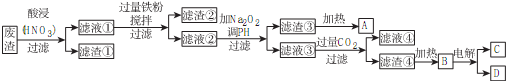
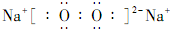 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1 mol/L NaHCO3��Һ��0.1 mol/L NaOH��Һ�������ϣ�������Һ�У�c��Na+����c��CO32-����c��HCO3-����c��OH-�� | |
| B�� | 20 mL 0.1 mol/L CH3COONa��Һ��10 mL 0.1 mol/L HCl��Һ��Ϻ���Һ�����ԣ�������Һ�У�c��CH3COO-����c��Cl-����c��CH3COOH����c��H+�� | |
| C�� | �����£�pH=2��������pH=12�İ�ˮ�������ϣ�������Һ�У�c��Cl-��+c��H+����c��NH4+��+c��OH-�� | |
| D�� | 0.1 mol/L CH3COOH��Һ��0.1 mol/L NaOH��Һ�������ϣ�������Һ�У�c��OH-����c��H+��+c��CH3COOH�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
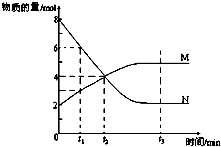 һ���¶��£�ij�ݻ�Ϊ2L���ܱ������ڣ�ijһ��Ӧ��M��g����N��g�������ʵ����淴Ӧʱ��仯��������ͼ����ͼ��ʾ��
һ���¶��£�ij�ݻ�Ϊ2L���ܱ������ڣ�ijһ��Ӧ��M��g����N��g�������ʵ����淴Ӧʱ��仯��������ͼ����ͼ��ʾ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com