
| 放电 |
| 充电 |
| A、放电时电解质溶液显强酸性 |
| B、充电时阳板反应为Ni(OH)2+2OH--2e-=NiO2+2H2O |
| C、放电时正极附近溶液pH减小 |
| D、充电时阴极附近溶液的碱性保持不变 |
| 放电 |
| 充电 |


科目:高中化学 来源: 题型:
| 实验序号 | 甲 | 乙 | 丙 |
| 盐酸体积/mL | 30.0 | 30.0 | 30.0 |
| 合金质量/mg | 255 | 385 | 459 |
| 气体体积/mL | 280 | 336 | 336 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3COONa(固体) |
| B、NH4Cl(固体) |
| C、CuSO4(溶液) |
| D、Ba(OH)2(固体) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原电池中,负极上发生的反应是氧化反应 |
| B、原电池中,电流从负极流向正极 |
| C、铜锌原电池中放电时,溶液中的阴离子向负极移动,阳离子向正极移动 |
| D、碱性锰锌电池是一次电池,铅蓄电池是二次电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:
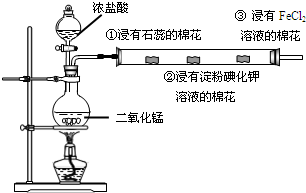
查看答案和解析>>
科目:高中化学 来源: 题型:
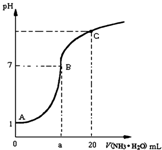 25℃时,在20mL的盐酸中,逐滴加入0.2mol?L-1的氨水,溶液的pH与氨水体积关系如图所示,则下列说法正确的是( )
25℃时,在20mL的盐酸中,逐滴加入0.2mol?L-1的氨水,溶液的pH与氨水体积关系如图所示,则下列说法正确的是( )| A、滴加前盐酸的物质的量浓度为0.1 mol?L-1 |
| B、B点的横坐标a=10 |
| C、A、B间的任一点,溶液都有c(Cl-)>c(NH4+)>c (H+)>c(OH-) |
| D、如果将氨水换为NaOH溶液,则滴加20mL时溶液的pH一定小于C点的pH |
查看答案和解析>>
科目:高中化学 来源: 题型:
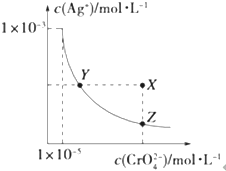 在t℃时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如图所示.又知AgCl的Ksp=1.8×10-10.下列说法不正确的是( )
在t℃时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如图所示.又知AgCl的Ksp=1.8×10-10.下列说法不正确的是( )| A、t℃时,Ag2CrO4的Ksp为1×10-11 |
| B、饱和Ag2CrO4溶液中加入K2CrO4能使溶液由Y点变为X点 |
| C、t℃时,Y点和Z点时Ag2CrO4的Ksp相等 |
| D、t℃时,将0.01mol?L-1AgNO3溶液滴入20mL0.01mol?L-1KCl和0.01mol?L-1K2CrO4的混合溶液中,Cl-先沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH相同的三种溶液,物质的量浓度最小的是HCl |
| B、物质的量浓度相同的三种溶液,pH最小的是H2SO4 |
| C、含溶质的物质的量相同的三种溶液与过量镁粉反应,CH3COOH产生的H2最多 |
| D、相同pH、相同体积的三种溶液用NaOH溶液完全中和时,消耗NaOH溶液一样多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 如图装置可测定反应速率 |
| B、配制FeCl2溶液时,需加入少量铁粉和稀盐酸 |
| C、用碱式滴定管盛装KMnO4溶液滴定FeSO4溶液 |
| D、分别加热蒸干灼烧NaAlO2溶液和AlCl3溶液,最终都能得到Al2O3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com